Статьи
10-летние результаты ПСА-скрининга в британском исследовании CAP
Практическая целесообразность ПСА-скрининга — тема, вызывающая жаркие дискуссии среди специалистов. Крупные рандомизированные исследования в Европе (the European Randomized Study of Screening for Prostate Cancer (ERSPC), с участием 162 243 мужчин) и в США (the Prostate, Lung, Colorectal, and Ovarian Cancer Screening (PLCO) trial с участием 76 693 человек) дали неоднозначные результаты. Наряду с доказательствами снижения смертности от рака предстательной железы (РПЖ) при проведении ПСА-скрининга (0,71 летальный исход на 1000 скринированных, P=0,04) исследователи также обнаружили гипердиагностику клинически незначимых форм заболевания, приводящую к чрезмерному лечению, что, в свою очередь, ведет к развитию осложнений, ухудшающих качество жизни (недержание мочи, эректильная дисфункция).
Все это приводит к достаточно большим расхождениям в имеющихся клинических рекомендациях различных экспертных сообществ. Так, например, в 2017 году, опираясь на данные системных обзоров, существенно пересмотрены американские рекомендации US Preventive Services Task Force, согласно которым ПСА-скрининг может назначаться лишь в «индивидуальном порядке» мужчинам в возрасте 55–69 лет, после предварительного информирования о потенциальных рисках и осложнениях.
Другую стратегию выбрала Европейская ассоциация урологов (EAU). Согласно ее рекомендациям, скрининговое определение уровня ПСА должно быть предложено мужчинам из групп повышенного риска развития РПЖ: мужчинам в возрасте >50 лет, мужчинам в возрасте >45 лет при наличии семейного анамнеза РПЖ, мужчинам с уровнем ПСА>1 нг/мл в возрасте 40 лет или >2 нг/мл в возрасте 60 лет. Риск- адаптированная стратегия EAU предусматривает определение ПСА каждые 2 года у мужчин из групп риска, каждые 8 лет — у мужчин, не относящихся к группам риска. В ряде стран (например, Великобритании) не приняты программы скрининга РПЖ и проводится лишь ранняя диагностика заболевания.
6 марта 2018 г. в журнале JAMA были опубликованы результаты нового рандомизированного исследования The Cluster Randomized Trial of PSA Testing for Prostate Cancer (CAP), в котором оценивали отдаленные десятилетние результаты малоинтенсивного ПСА-скрининга и стандартного (нескринингового) обследования у мужчин в возрасте 50–69 лет.
КРУПНЕЙШЕЕ ИССЛЕДОВАНИЕ СКРИНИНГА
Британское исследование CAP стало крупнейшим на данный момент. В нем приняли участие полмиллиона мужчин в возрасте 50–69 лет, наблюдавшихся в 573 медицинских центрах Великобритании с 2001 по 2016 годы.
В группе скрининга (n=189 386) мужчинам предлагалось однократное определение уровня ПСА. При обнаружении высокого уровня (>3 нг/мл) выполнялась стандартизированная (10-точечная под ТРУЗИ-контролем) трансректальная биопсия предстательной железы. В контрольной группе (n=219 439) скрининг не проводился, обследование назначалось по стандартам NHS, т.е. при наличии симптомов заболевания.
Группы были хорошо сбалансированы по исходным характеристикам: возрасту на момент начала наблюдения (58,5 и 58,6 лет), социоэкономическим условиям (86 % мужчин проживало в городах), частоте сопутствующих заболеваний — сахарного диабета (0,6 % и 0,5 %), ожирения (8,0 % и 7,8 %), ишемической болезни сердца (4,1 % и 3,9 %).
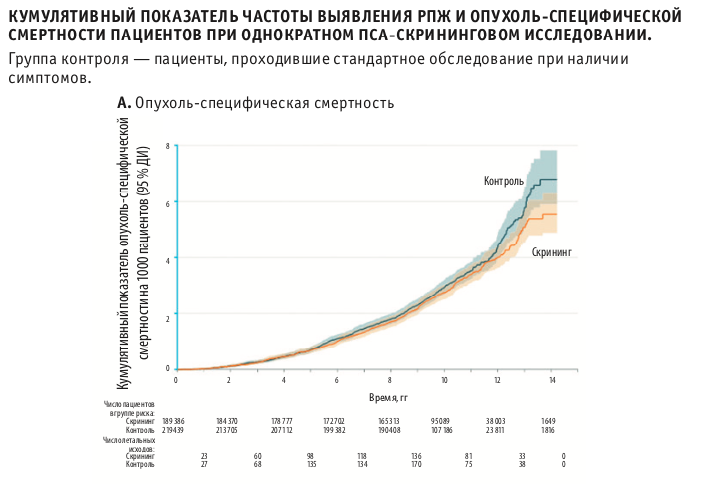
Частота выявляемости рака предстательной железы была выше в группе скрининга, чем в контрольной группе (4,3 % против 3,6 %, отношение рисков (ОР) 1,19, Р<0,001), однако даже при медиане наблюдения в 10 лет в отношении главной цели исследования — показателя опухоль-специфической смертности — различий между группами не было получено (0,30 против 0,31 на 1000 человеко-лет, ОР=0,96, P=0,5).
Примечательно, что из 189 386 мужчин, включенных в группу скрининга, лишь 36 % согласились на проведение ПСА-анализа (для сравнения, в европейском исследовании ERSPC этот показатель достигал 59–69 %). У 11 % мужчин, сдавших тест, был выявлен повышенный уровень ПСА>3 нг/мл и взята биопсия предстательной железы. Частота отказов от ПСА-тестирования не зависела от возраста или социального статуса.
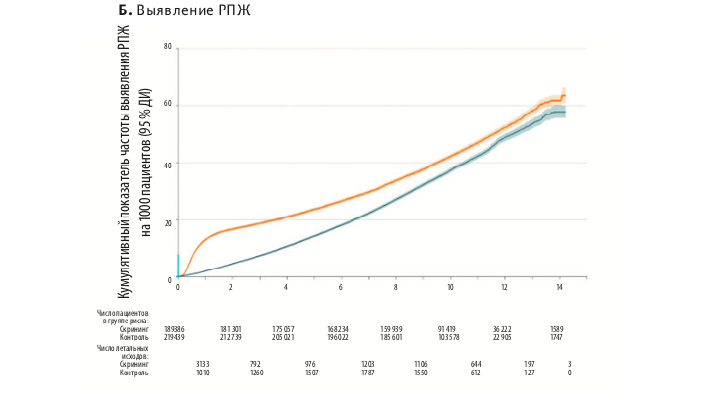
При выделении только пациентов, сдавших ПСА-тест, 10-летний показатель выявляемости РПЖ возрос до 6,2 % (или 6,24 случая на 1000 человеко-лет), в то время как среди отказавшихся выявляемость РПЖ была еще ниже, чем даже в контрольной группе (3,0 % против 3,6 %, или 3,18 против 3,80 на 1000 человеко- лет). Определение уровня ПСА приводило к более ранней диагностике РПЖ: как по возрасту на момент обнаружения заболевания (медиана в группе сдавших ПСА-анализ — 65,3 лет, в контрольной группе — 67,7 лет), так и по длительности наблюдения до подтверждения диагноза (1,2 лет и 6,2 лет соответственно).
Рост заболеваемости РПЖ в группе скрининга (+0,65 на 1000 человеко- лет, P<0,001) обеспечивается преимущественно за счет большей частоты обнаружения высокодифференцированных опухолей с индексом Глисона 6 (P<0,001) и локализованных стадий заболевания (различие 6,97 на 1000 мужчин, P<0,001).
Еще одна особенность заключается в динамике выявляемости РПЖ. Максимальное различие заболеваемости между группами было зафиксировано в первые 18 месяцев наблюдения: 10,42 против 2,18 в контрольной группе на 1000 человеко-лет (ОР=8,25, P<0,001). В последующем прослеживается обратная тенденция: снижение выявляемости РПЖ в группе скрининга (до 3,36 на 1000 человеко-лет) и умеренный рост в контрольной группе (до 4,11 на 1000 человеко-лет, ОР= -0,75, P<0,001).
Отдельную группу представляют мужчины, у которых выявляется РПЖ при нормальном уровне ПСА <3 нг/мл. В среднем, ПСА- негативный РПЖ обнаруживался через 7,9 лет с момента начала наблюдения и составил 28 % от числа всех выявленных случаев заболевания.
БЕЗ ВЛИЯНИЯ НА ОПУХОЛЬ-СПЕЦИФИЧЕСКУЮ СМЕРТНОСТЬ
Главной целью в исследовании CAP было сравнение опухоль- специфической смертности в группе скрининга и стандартного обследования. Как известно, по данным исследования ERSPC было подтверждено снижение смертности в случае ПСА-скрининга (ОР=0,80, P=0,04), однако для профилактики 1 случая опухоль- специфической смерти оказалось необходимым скрининговое обследование 1410 мужчин и дополнительное лечение 48 больных РПЖ.
В исследовании CAP к медиане наблюдения 10 лет достоверных различий в опухоль-специфической смертности между группами получено не было: 549 мужчин скончалось от РПЖ в группе скрининга и 647 — в контрольной группе (стандартизированные показатели 0,30 и 0,31 на 1000 человеко-лет соответственно, ОР = 0,96, P=0,50). Подгрупповой анализ не показал влияния ПСА- тестирования на показатель летальности ни в зависимости от возраста (P=0,14), ни в зависимости от социоэкономического статуса (P=0,22). В пользу адекватной рандомизации в исследовании говорит отсутствие достоверных различий в общей смертности (25 459 и 28 306 смертей соответственно в группе скрининга и контрольной, ОР=0,99, P=0,49).
К сожалению, авторы исследования отметили низкую пользу ПСА- скрининга в обнаружении «летального» РПЖ. Так, у значительного числа скончавшихся от РПЖ определялся «нормальный» уровень ПСА<3,0 нг/мл, реже отсутствовала биопсия предстательной железы или была верификация только доброкачественной гиперплазии. Еще одной потенциальной причиной необнаружения «летального» РПЖ может быть использование стандартной 10-точечной биопсии предстательной железы. По современным данным, для повышения точности диагностики перед биопсией простаты целесообразно проведение мультипараметрической МРТ малого таза.
В ПОЛЬЗУ РАННЕЙ ДИАГНОСТИКИ
При интерпретации результатов исследования CAP (2001–2016 гг.) необходимо учитывать, что аналогичные исследования (ERSPC и PLCO) проводились существенно раньше — в 1993–2003 и 1993–2001 гг. соответственно. У пациентов в 1990-х и 2010-х были заведомо разные возможности как в лекарственном, так и в хирургическом лечении. Так, только в 2005 г. появился первый препарат с доказанной эффективностью для больных кастрационно- резистентным раком предстательной железы (доцетаксел), позднее появились химиотерапия II линии, новые препараты гормональной терапии с направленным воздействием (абиратерон, энзалутамид). В 2000-х широкое распространение получили малоинвазивные и роботизированные техники оперативных вмешательств.
В последние годы была выделена новая группа пациентов — больные с олигометастатическим опухолевым процессом после предшествующего радикального лечения, так как выполнение сальважных методов хирургического или лучевого лечения позволяет отсрочить время начала гормональной терапии у отобранных пациентов.
Среди сильных сторон дизайна исследования отмечают четкую стандартизацию диагностического обследования в контрольной и скрининговой группе. Все мужчины, у которых в исследовании CAP был диагностирован РПЖ (при уровне ПСА<19,9 нг/мл), были включены в протокол исследования The Prostate Testing for Cancer and Treatment (ProtecT) и имели возможность получения современных стандартов лечения — опции радикальной простатэктомии, лучевой терапии или активного наблюдения. При медиане наблюдения в ProtecT 10 лет опухолево-специфическая смертность составила до 1 % и не отличалась в разных группах лечения.
Определенные успехи были достигнуты в предупреждении гипердиагностики РПЖ, в сравнении с более ранними исследованиями ERSPC и PLCO. Как и предполагалось, сокращение частоты ПСА- тестирования с трехкратного (через 1, 2 и 4 года в ERSPC и PLCO) до однократного (в CAP исследовании) способствовало увеличению возраста пациентов на момент обнаружения РПЖ, стадии заболевания и доли низкодифференцированных форм. В то же время не исключено, что повторное ПСА-тестирование (интенсивный скрининг) способствует снижению канцер-специфической смертности от РПЖ. Впервые эта гипотеза была выдвинута на основании сравнительного анализа данных из разных центров исследования ERSPC: при проведении более частого ПСА-анализа не только закономерно повышалась диагностика клинически незначимых форм РПЖ, но и снижалась смертность от заболевания. Британское исследование CAP косвенно подтвердило данную гипотезу, не обнаружив достоверного снижения опухолево-специфичес- кой смертности при однократном ПСА-скрининге, в сравнении с контрольной группой.
Возможно, 10-летний период наблюдения является слишком малым для формирования окончательных выводов о ПСА- скрининге. Больше половины летальных исходов от РПЖ было зарегистрировано в течение первых 7 лет наблюдения, когда ПСА- скрининг наиболее вероятно еще не оказал эффекта. Кумулятивный показатель летальности показал разную динамику в контрольной и группе скрининга после 12 лет наблюдения. Авторы исследования продолжают работу и планируют публикацию данных о 15-летней общей, опухоль-специфической смертности, оценке качества жизни и анализе «затраты — эффективность». В настоящий момент исследователи рекомендуют воздержаться от проведения популяционного ПСА-скрининга и взамен использовать стратегию ранней диагностики РПЖ с применением новых методов лучевой диагностики (мпМРТ), таргетной биопсии (фьюжн-биопсии), новых биомаркеров крови и, в перспективе, генетического анализа.


















