Статьи
30 лет первой аллогенной трансплантации гемопоэтических стволовых клеток у ребенка в России
Трансплантация гемопоэтических стволовых клеток (ТГСК) — это уникальный высокотехнологичный метод лечения ряда тяжелых, неизлечимых другими способами заболеваний у детей и взрослых. Речь идет об онкологических, злокачественных и доброкачественных заболеваниях системы крови, наследственных болезнях, при которых после курса цитостатических препаратов и/или лучевой терапии для обеспечения иммунологической толерантности и приживления реципиенту вводят гемопоэтические стволовые клетки донора с целью замещения кроветворения.
ПОЛВЕКА В АКТИВЕ
История развития трансплантации гемопоэтических стволовых клеток (ТГСК) в мире насчитывает более 50 лет. Первая успешная аллогенная трансплантация костного мозга/гемопоэтических стволовых клеток (ТКМ/ТГСК) была произведена в 1968 году в США группой Роберта Гуда (Robert A. Good) мальчику с тяжелой формой врожденного иммунодефицита. В трех поколениях семьи этого пациента насчитывалось 11 случаев данного заболевания с летальным исходом. В 1990 году Д. Томас (Donnall Thomas) из США получил Нобелевскую премию по медицине за разработку и внедрение ТКМ.
 В Россию ТКМ пришла несколько позже — в начале 1990‑х. Тогда в Москве, Ленинграде и других городах страны в специализированных отделениях детской гематологии и онкологии, опираясь на общемировой опыт, начали использовать современные протоколы химиотерапии (ХТ). Тогда же в СССР были предприняты первые попытки применения ТКМ от родственного донора у взрослых пациентов. В 1987 году в ленинградском НИИ онкологии им. Н.Н. Петрова открыли первое отделение ТКМ под руководством профессора Бориса Владимировича Афанасьева. Трансплантация была центром его научных и клинических интересов. Тридцать лет назад, а именно 17 декабря 1991 года, сотрудниками этого нового отделения ТКМ на базе городской больницы № 31 им. Я.М. Свердлова была выполнена первая успешная аллогенная ТКМ у ребенка. Ее зарегистрировали как первую ТКМ из СССР в Европейской группе по трансплантации костного мозга (European group for Blood and Marrow Transplantation — EBMT). Успехи в развитии этого направления в Санкт-Петербурге неразрывно связаны с неоценимой помощью ведущих специалистов Европы и США, в первую очередь директора Центра трансплантации костного мозга Гамбургского университета — профессора А. Цандера (Axel Zander), а также профессоров Т. Бюхнера, Г-Й. Кольба, Д. Хёльтцера (Thomas Büchner, Hans-Jochem Kolb, Dieter Hoelzer) из Германии, Р. Гейла (Robert Gale) из США, Г. Вагемакера (Gerard Wagemaker) из Нидерландов и многих других (рис. 1, 2).
В Россию ТКМ пришла несколько позже — в начале 1990‑х. Тогда в Москве, Ленинграде и других городах страны в специализированных отделениях детской гематологии и онкологии, опираясь на общемировой опыт, начали использовать современные протоколы химиотерапии (ХТ). Тогда же в СССР были предприняты первые попытки применения ТКМ от родственного донора у взрослых пациентов. В 1987 году в ленинградском НИИ онкологии им. Н.Н. Петрова открыли первое отделение ТКМ под руководством профессора Бориса Владимировича Афанасьева. Трансплантация была центром его научных и клинических интересов. Тридцать лет назад, а именно 17 декабря 1991 года, сотрудниками этого нового отделения ТКМ на базе городской больницы № 31 им. Я.М. Свердлова была выполнена первая успешная аллогенная ТКМ у ребенка. Ее зарегистрировали как первую ТКМ из СССР в Европейской группе по трансплантации костного мозга (European group for Blood and Marrow Transplantation — EBMT). Успехи в развитии этого направления в Санкт-Петербурге неразрывно связаны с неоценимой помощью ведущих специалистов Европы и США, в первую очередь директора Центра трансплантации костного мозга Гамбургского университета — профессора А. Цандера (Axel Zander), а также профессоров Т. Бюхнера, Г-Й. Кольба, Д. Хёльтцера (Thomas Büchner, Hans-Jochem Kolb, Dieter Hoelzer) из Германии, Р. Гейла (Robert Gale) из США, Г. Вагемакера (Gerard Wagemaker) из Нидерландов и многих других (рис. 1, 2).
Развитие метода ТГСК требовало квалифицированной организационной работы, направленной на расширение спектра оказания высокотехнологичной медицинской помощи (ВМП), обеспечение всех видов сопроводительной терапии у детей и взрослых. Это стало возможным только в условиях работы в alma mater профессора Б.В. Афанасьева — Первом медицинском институте им. академика И.П. Павлова (ныне Первый Санкт-Петербургский государственный медицинский университет им. академика И.П. Павлова).
При поддержке его ректора — академика РАН, профессора Н.А. Яицкого — здесь в 1997 году был создан Центр гематологии. В 2000 году в ПСПбГМУ им. акад. И.П. Павлова открыта первая в России университетская клиника ТКМ. С этого времени в стране была начата программа по широкому внедрению аллогенной ТКМ от неродственного донора у детей и взрослых, сделаны первые шаги по созданию единой базы данных (регистра) неродственных доноров костного мозга.
В 2007 году в ПСПбГМУ им. акад. И.П. Павлова открылся Институт детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой (ныне НИИ ДОГиТ им. Р.М. Горбачевой), построенный по инициативе ПСПбГМУ им. акад. И.П. Павлова и Фонда М.С. Горбачева при финансовой поддержке Националь‑ ного резервного банка. Инициатором создания института и первым его директором был профессор Б.В. Афанасьев. В 2013 году под его руководством в рамках реализации программы по аллогенной ТГСК в НИИ ДОГиТ им. Р.М. Горбачевой ПСПбГМУ им. И.П. Павлова разработана, внедрена и результативно используется автоматизированная информационная система поиска доноров (Bone Morrow Donor Search). Она позволяет успешно искать и активировать российских доноров для пациентов института и других клиник России, специализирующихся в области трансплантации.
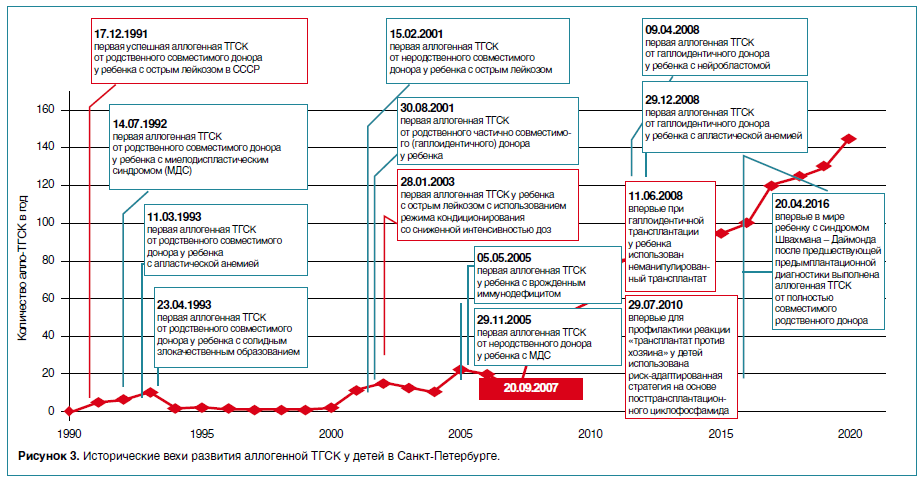
Развитие аллогенной ТГСК у детей в Санкт-Петербурге связано с целым рядом важных событий (рис. 3).
МИССИЯ ВЫПОЛНИМА
Ежегодно в клинике института детям выполняют до 190 ТГСК всех видов — аутологичных, от родственных и неродственных доноров с разной степенью совместимости (полностью, частично совместимых, гаплоидентичных). Используют различные источники гемопоэтических стволовых клеток (костный мозг, периферическая кровь). В клинике внедрены режимы кондиционирования раз‑ личной интенсивности: миелоаблативные, сниженной токсичности и интенсивности, немиелоаблативные.
В программной терапии пациентов с рецидивами заболеваний и первичной резистентностью к ХТ используют таргетные препараты, иммунотерапию. Разрабатывают и внедряют новые методы профилактики и лечения ранних и поздних осложнений аллогенной ТГСК. Перечисленные факторы позволили существенно улучшить долгосрочные результаты лечения злокачественных и незлокачественных заболеваний системы крови у детей (особое место среди них занимает острый лимфобластный лейкоз — ОЛЛ), солидных опухолей, ряда наследственных заболеваний.
Представленный двадцатилетний опыт НИИ ДОГиТ им. Р.М. Горбачевой убедительно демонстрирует, что даже у пациентов из группы неблагоприятного прогноза при своевременно выполненной аллогенной ТГСК независимо от типа донора результаты лечения приближаются к таковым у пациентов группы более благоприятного прогноза.
На фоне успехов в области аллогенной ТГСК у детей увеличивается когорта пациентов с продолжительной выживаемостью без прогрессирования. И этим детям необходимо обеспечить полноценное мультидисциплинарное наблюдение на протяжении всей жизни. Повышается значение преемственности на всех этапах наблюдения, внедрения различных реабилитационных программ. После выздоровления пациенты полностью социально адаптируются, получают образование, взрослеют, создают семьи, у них появляются собственные дети.
Под руководством профессора Б.В. Афанасьева НИИ ДОГиТ им. Р.М. Горбачевой стал крупнейшим в России и Европе центром по оказанию ВМП методом ТКМ детям, подросткам и взрослым с различными вариантами лейкозов, депрессиями кроветворения, солидными опухолями, включая опухоли центральной нервной системы (ЦНС) у детей, и наследственными заболеваниями. За годы работы в клинике выполнено более 4500 трансплантаций гемопоэтических стволовых клеток у детей и взрослых.
НИИ ДОГиТ им. Р.М. Горбачевой интегрирован в работу международного специализированного сообщества, является членом Европейской группы по трансплантации костного мозга (ЕВМТ), Национальной программы доноров США (Marrow National Donor Program). Созданный профессором Б.В. Афанасьевым коллектив специалистов известен как команда CIC 725 ЕВМТ. В 2018 году за выдающийся вклад в развитие ТГСК в Санкт-Петербурге и России профессор Б.В. Афанасьев награжден Премией высших клинических достижений ЕВМТ.
За прошедшие 30 лет со времени первой успешной аллогенной ТГСК у ребенка в нашей стране в области детской гематологии/онкологии сделано очень много. Достигнутые успехи, накопленный опыт, кооперация российских и международных специалистов позволяют надеяться на новые открытия, на улучшение результатов лечения детей со злокачественными и доброкачественными заболеваниями системы крови, солидными опухолями и наследственной патологией, при которых показана аллогенная ТГСК.
Читайте также
- Синдром Гурлер
- Глиомы у детей до года: новейшие методы терапии
- Опухолевый тромбоз нижней полой вены с распространением в правое предсердие
- Современные возможности лучевой визуализации
- Неважно, сколько дней в твоей жизни. Важно, сколько жизни в твоих днях!
- Роль педиатра в успешном лечении гемобластозов у детей
- Адоптивная клеточная иммунотерапия солидных опухолей у детей
- Клинический пример терапии ингибитором рецептора интерлейкина‑1 — препаратом анакинра — у пациента с криопирин-ассоциированным периодическим синдромом

















