Статьи
Аллогенная трансплантация костного мозга: не только при лейкозах
КОМУ ОНА ПОКАЗАНА
С одной стороны, показания к ТГСК сужаются в тех случаях, когда находится новый, более эффективный и безопасный метод. С другой стороны, иногда приходит время вспомнить о старых показаниях, если новые методы работают как синергисты и усиливают эффект ТГСК. Одним из таких направлений стала аллогенная трансплантация у детей с солидными опухолями.
Традиционно ТГСК рассматривали как метод выбора при заболеваниях, вовлекающих систему кроветворения или иммунную систему. Первые аллогенные трансплантации применялись у детей с врожденной и приобретенной аплазией кроветворения, врожденными иммунодефицитами (ИД) и, естественно, лейкозами. До сих пор лейкозы остаются основным показанием к ТГСК. Спектр показаний при ИД расширяется. Выполняются трансплантации при аутоиммунных заболеваниях в попытке перезагрузить иммунную систему. Развиваются направления применения ТСГК при тяжелых гемоглобинопатиях (например, талассемиях и серповидноклеточных анемиях), болезнях обмена — в тех случаях, когда донорские гемопоэтические клетки способны обновить необходимую ткань или заместить продукцию дефектного белка (синдром Гурлера, остеопетроз).
Показания к ТГСК у детей с солидными опухолями традиционно были более узкими. До сих пор в качестве метода выбора и стандарта лечения рассматривается аутологичная ТГСК. При этом виде лечения пациенту возвращаются ранее заготовленные и криоконсервированные собственные гемопоэтические клетки после введения высоких доз химиопрепаратов (миелоаблативного режима кондиционирования). Попыток трансплантации донорских клеток было сравнительно мало, и далеко не всегда они были успешными. С чем это было связано и что изменилось за последнее время?
КТО БУДЕТ ДОНОРОМ
 Первые успешные трансплантации выполнялись от одного близнеца к другому. В дальнейшем, когда были исследованы механизмы гистосовместимости и появились первые методы HLA-типирования, оптимальными донорами продолжали считаться полностью совместимые брат или сестра. К сожалению, совместимый родственный донор находился не у всех пациентов. Начали появляться регистры неродственных доноров, объединенные в глобальную базу данных, в которой можно найти потенциального донора для больного. В частности, колоссально важную роль играет стремительно развивающийся в последние годы Российский регистр неродственных доноров. Но даже в этом случае подходящий вариант находится не для каждого пациента.
Первые успешные трансплантации выполнялись от одного близнеца к другому. В дальнейшем, когда были исследованы механизмы гистосовместимости и появились первые методы HLA-типирования, оптимальными донорами продолжали считаться полностью совместимые брат или сестра. К сожалению, совместимый родственный донор находился не у всех пациентов. Начали появляться регистры неродственных доноров, объединенные в глобальную базу данных, в которой можно найти потенциального донора для больного. В частности, колоссально важную роль играет стремительно развивающийся в последние годы Российский регистр неродственных доноров. Но даже в этом случае подходящий вариант находится не для каждого пациента.
Спасти ситуацию может гаплоидентичный (наполовину совместимый) донор. Несмотря на очевидные недостатки (значительно более высокий риск иммунных осложнений), в последние годы гаплоТГСК становится все ближе к тому, чтобы превратиться в стандарт лечения. Гаплоидентичные доноры для ребенка — это в первую очередь его родители, а также братья и сестры, которые бывают наполовину совместимы в два раза чаще, чем полностью совместимые. Гаплоидентичный донор есть почти у каждого пациента, он постоянно находится рядом с ним и мотивирован на участие в пересадке стволовых клеток. Это обстоятельство играет важнейшую роль в тех случаях, когда не удается найти совместимого донора или времени на поиски просто нет, а риск рецидива или развития серьезных осложнений, связанных с компрометированным иммунным статусом пациента, в период поиска донора крайне высок.
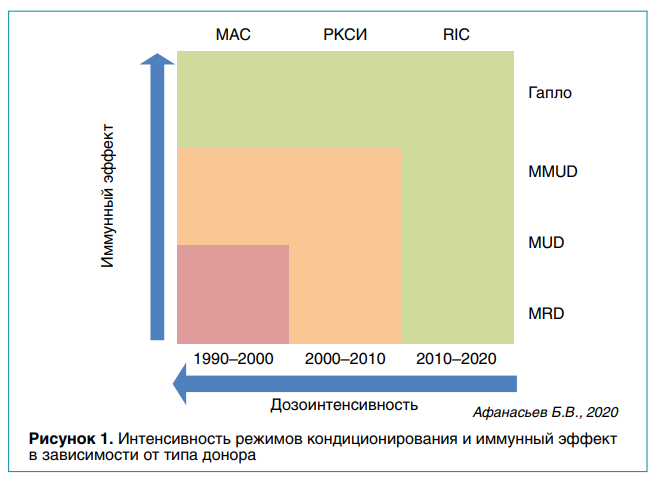
По мере накопления данных становится понятно, что у гапло-ТГСК есть и определенные преимущества. За счет неполной совместимости иммунные клетки донора способны обеспечить более мощный ответ против антигенов реципиента. Более того, потеря опухолью экспрессии HLA I класса может происходить за счет других субпопуляций клеток, в частности NK-клеток и Т-лимфоцитов. Потенциально это имеет особое значение для лечения детей с солидными опухолями, клетки которых часто подавляют экспрессию HLA, чтобы уйти из-под иммунного контроля, что особенно часто происходит после алло-ТГСК. По мере того как при трансплантации делается все больший акцент на иммунный эффект, в значительной части случаев начинают использоваться менее интенсивные (немиелоаблативные) режимы кондиционирования. Это позволяет снизить токсичность процедуры и избежать ряда отсроченных нежелательных эффектов. Подобные режимы начинают применяться все чаще (рис. 1).
Ранее более мощный иммунный ответ против опухоли после гапло-ТГСК в значительной степени нивелировался большим риском осложнений, в первую очередь реакциями «трансплантат против хозяина» и отторжения трансплантата, которые не позволяли добиваться долгосрочных результатов, сравнимых с ТГСК от совместимого донора. Тем не менее за последнее десятилетие гапло-ТГСК стала значительно безопаснее. Помимо совершенствования сопроводительной терапии, широкое применение нашли методы модификации трансплантата, позволяющие удалить из него наиболее агрессивные популяции лимфоцитов донора.
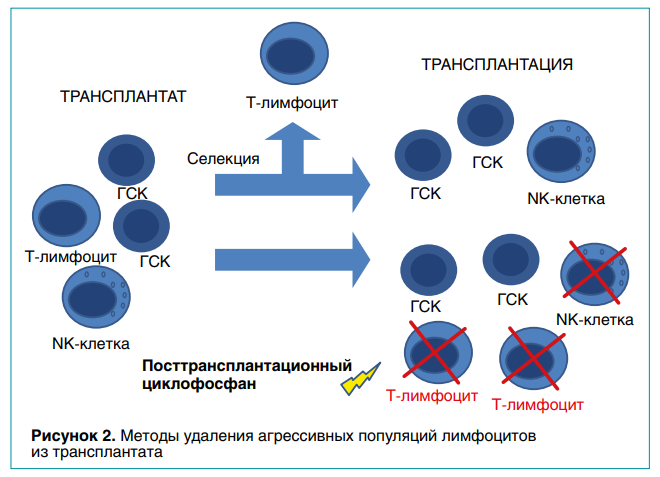
Это может осуществляться двумя путями:
-
вне организма реципиента при использовании методов иммуномагнитной селекции (донорские клетки смешиваются с бусинами ферромагнетика, покрытыми антителами, которые способны прикрепляться к отдельным субпопуляциям, что позволяет изъять их из трансплантата с помощью магнита);
-
in vivo — за счет введения через не - сколько дней после трансплантации циклофосфана, подавляющего наиболее активно пролиферирующие клетки (рис. 2).
Хотя первый метод позволяет сохранить в трансплантате нужные в посттрансплантационом периоде клетки (например, NK-клетки и γδТ-лимфоциты), второй привлекателен относительной простотой и отсутствием необходимости в дополнительном оборудованиии реагентах. Оба подхода продемонстрировали эффективность у детей с лейкозами и незлокачественными заболеваниями. Таким образом, гапло-ТГСК постепенно занимает свою нишу в рамках стандарта лечения, становясь более эффективным методом по сравнению с трансплантацией от частично совместимого неродственного донора, в том числе у детей с солидными опухолями.
ВОПРОС ПО СУЩЕСТВУ
Но почему же вновь поднимается вопрос об алло-ТГСК у пациентов с солидными опухолями? Хотя аутологичные трансплантации у таких детей до сих пор выполняются чаще и позволили добиться значительных успехов при отдельных показаниях, существуют подгруппы пациентов, у которых повышение дозоинтенсивности не оказалось эффективным. Для этих больных методы иммунотерапии, позволяющие обойти сформировавшиеся механизмы резистентности к химиопрепаратам, становятся особенно привлекательными.
Очень ярко преимущество иммунотерапии демонстрирует практика лечения пациентов с нейробластомой. Несмотря на успешное применение ауто-ТГСК в рамках комплексной терапии, до недавнего времени более половины пациентов из группы высокого риска умирали из-за развития рецидива заболевания. Тем не менее, учитывая присутствие на большинстве клеток нейробластомы относительно специфичной молекулярной мишени—GD2, можно использовать антитела, направленные на эту мишень. На больших группах больных уже продемонстрирована эффективность лечения антителами к GD2 в рамках поддерживающей терапии, направленной на уничтожение оставшихся после ауто-ТГСК отдельных химиорезистентных опухолевых клеток. Ведутся исследования применения иммунотерапии на других этапах лечения, в том числе при рецидиве заболевания.
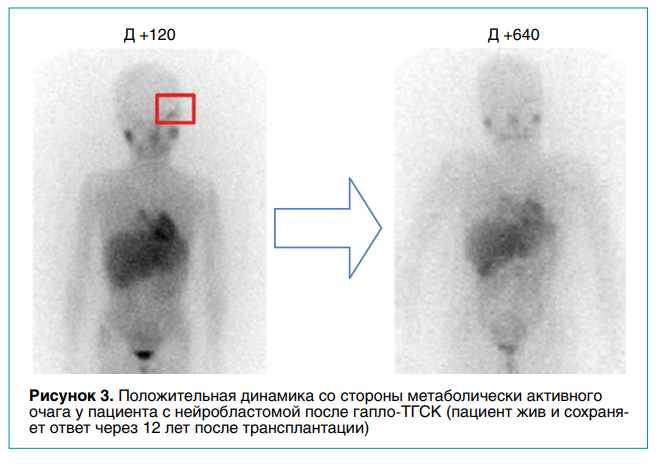
До недавнего времени рецидив нейробластомы у пациента из группы высокого риска считался практически неизлечимым. Методы лечения, используемые в большинстве случаев, фактически были направлены лишь на продление жизни ребенка. А первые успехи в этом направлении были связаны, в том числе в России, с применением гапло-ТГСК как способа закрепить эффект противорецидивной терапии. Более того, была продемонстрирована возможность длительного сохранения терапевтического эффекта с постепенным обратным развитием опухолевых очагов после трансплантации (рис. 3). Тем не менее у значительной части пациентов (около 80 %) рецидив после трансплантации все же развивался. В этой ситуации использование дополнительных методов иммунотерапии, способных выделить клетки-мишени и усилить длительный иммунный эффект ТГСК, несмотря на низкую экспрессию этими клетками молекул, активирующих иммунный ответ, оказывается особенно привлекательным.
 При использовании иммунотерапии после аллогенной трансплантации очень важно соблюдать правильный тайминг лечения. С недавних пор своевременное применение иммунотерапии стало возможным благодаря благотворительному фонду «Круг добра», помогающему детям с орфанными заболеваниями, к которым в силу своей относительной редкости принадлежит и нейробластома. Кроме того, помимо усилий экспертного сообщества, огромную роль в привлечении общественного внимания к проблеме и в формировании текущих показаний сыграло объединение родителей детей с диагнозом «нейробластома» — «Энби». Многим детям с ее рецидивом уже открыт доступ к иммунотерапии, в том числе после гапло-ТГСК, а первый опыт можно назвать положительным.
При использовании иммунотерапии после аллогенной трансплантации очень важно соблюдать правильный тайминг лечения. С недавних пор своевременное применение иммунотерапии стало возможным благодаря благотворительному фонду «Круг добра», помогающему детям с орфанными заболеваниями, к которым в силу своей относительной редкости принадлежит и нейробластома. Кроме того, помимо усилий экспертного сообщества, огромную роль в привлечении общественного внимания к проблеме и в формировании текущих показаний сыграло объединение родителей детей с диагнозом «нейробластома» — «Энби». Многим детям с ее рецидивом уже открыт доступ к иммунотерапии, в том числе после гапло-ТГСК, а первый опыт можно назвать положительным.
Вероятно, наибольший опыт гапло-ТГСК в России накоплен отделением трансплантации костного мозга для детей № 2 НИИ детской онкологии, гематологии и трансплантологии имени Р.М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета имени академика И.П. Павлова (крупнейшей трансплантационной клиники, выполнившей уже более 5 тысяч ТГСК у детей и взрослых). Отделение ориентировано в первую очередь на выполнение трансплантаций, в том числе аллогенных, у детей с солидными опухолями.
В то же время значительный опыт в данной области накоплен и в других федеральных центрах, в первую очередь в НМИЦ онкологии имени Н.Н. Блохина (одном из пионеров данного направления), НМИЦ детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева и НМИЦ онкологии имени Н.Н. Петрова. Учитывая трудности набора в исследования пациентов с редкими диагнозами, только совместная работа нескольких центров позволяет выработать оптимальные подходы к терапии.
Тот же принцип еще более применим к детям с другими диагнозами, у которых опыт использования ТГСК пока еще более неблагоприятный и для которых пока нет эффективных препаратов для иммунотерапии. В первую очередь это больные с саркомой Юинга. Несмотря на описание отдельных случаев эффективности иммунотерапии, пока непонятно, в каких именно подгруппах это преимущество будет максимальным. Учитывая еще большую редкость таких пациентов, межцентровое взаимодействие в рамках протоколов ТГСК становится критически важным.
В области применения гапло-ТГСК у детей с солидными опухолями мы до сих пор находимся в начале пути. Но, несмотря ни на что, уже с уверенностью можно утверждать, что данный метод будет развиваться и дальше.
Читайте также
- Продолжение эры детской онкоиммунологии. «Рогатая» мишень или обманка?
- Возможности радиационной иммуномодуляции в лечении онкологических заболеваний
- Мультидисциплинарный подход к лечению сепсиса у детей с онкогематологическими заболеваниями
- Рак щитовидной железы у детей: ключевые рекомендации
- Иммуноглобулины для подкожного введения — новая эра иммуномодулирующей терапии
- Междисциплинарное взаимодействие в детской онкохирургии


















