Статьи
Инфантильные гемангиомы: что нового в подходах к лечению?
Инфантильные, или младенческие, гемангиомы (ИГ) встречаются у 3–10 % доношенных и 30 % недоношенных детей, причем у девочек в 3 раза чаще, чем у мальчиков. Эта распространенная в раннем возрасте проблема может приводить к функциональным или эстетическим нарушениям. Вот почему важно как можно раньше выявлять данную патологию и приступать к лечению, первой линией которого сегодня считается системная фармакотерапия пероральным раствором пропранолола.
ФАКТОРЫ РИСКА
Инфантильная гемангиома — наиболее распространенное доброкачественное сосудистое опухолевидное новообразование — диагностируется у 5–10 % младенцев в течение первого года жизни. Отличается реактивным опухолеподобным ростом ткани, в основе которого лежит пролиферация клеток эндотелия капилляров с инволюцией в конечном итоге, а также медленным спонтанным разрешением (как правило, без существенных последствий) и типичной (до 60 % случаев) локализацией в челюстно-лицевой области.
К факторам риска развития ИГ относятся:
- принадлежность к женскому полу;
- недоношенность;
- низкий вес — риск ИГ увеличивается на 25 % на каждые 500 г дефицита массы тела при рождении;
- наследственность—случаи ИГ в семье.
С повышенной частотой ИГ связаны два синдрома:
1. PHACE — акроним от Posterior fossa abnormality, Hemangioma, Arterial anomaly, Cardiac defects, Eye abnormality (дефекты задней черепной ямки, сегментарные гемангиомы в области лица и/или волосистой части головы, аномалии сосудов головного мозга, сердечнососудистые аномалии и аномалии глаз).
2. LUMBAR — Lower body IH, Urogenital anomalies, Ulceration, Myelopathy, Body deformities, Anorectal malformations, Arterial anomalies, Renal anomalies (гемангиомы нижней части тела, урогенитальные аномалии, изъязвление, миелопатия, деформации тела, пороки развития, артериальные и почечные аномалии).
Синдром PHACE может также включать гемангиомы печени, а LUMBAR ассоциирован с гемангиомами нижней части тела, часто затрагивающими поясничнокрестцовую область.
В 30 % случаев ИГ регрессируют без последствий, но большая их часть формирует резидуальные явления в виде атрофических рубцов, синдрома дряблой кожи, телеангиоэктазий, фиброзножировых изменений. Существует и риск осложнений (язвы, кровотечения и др.). Для стратификации рисков и принятия решений о тактике лечения разработаны соответствующие инструменты классификации и оценки степени тяжести ИГ.
СТАДИИ ПОРАЖЕНИЯ
Клиническая картина ИГ определяется стадией поражения.
- Начальные проявления характеризуются наличием с самого рождения участка покраснения (или побледнения) кожи либо слизистой оболочки. Родители чаще всего воспринимают это как потертость, синячок или царапину.
- Пролиферация (активный рост) сопровождается трансформацией внешних признаков ИГ. В возрасте 2–3 недель подозрительное пятнышко начинает увеличиваться, приобретая насыщенную ярко-красную или багрово-синюю окраску. ИГ становится плотной и горячей на ощупь из-за локального повышения температуры.
- Стабилизация и начало инволюции (4–6 месяцев) выражаются в остановке роста и побледнении очага сосудистого поражения. Эти изменения происходят постепенно и, как правило, от центра к периферии.
- Выраженная инволюция: очаг сосудистой гиперплазии уменьшается, становясь менее плотным и приобретая все более светлый оттенок.
- Резидуальные (остаточные) проявления — конечный этап развития ИГ. Длительность и степень регресса образования варьируют от частичного (телеангиоэктазии, объемные фиброзножировые комплексы в толще тканей) до полного разрешения в течение года или максимум десяти лет.
Продолжительность стадий зависит от исходной площади поражения, объема и глубины вовлеченных в процесс тканей, а также от проводимой терапии. Следует отметить, что самопроизвольной инволюции подвергаются до 70–90 % сосудистых поражений и лишь 10 % пациентов требуется терапия. К факторам, определяющим необходимость лечения ИГ, относятся локализация, распространенность, глубина, множественность сосудистых образований, наличие ассоциированных аномалий (синдромы РНАСЕ и LUMBAR), а также осложнения, вызывающие функциональные и косметические дефекты.


ТРУДНОСТИ ДИАГНОСТИКИ
В связи с разнообразием сосудистой патологии у детей важна своевременная и правильная диагностика ИГ. Впервые ребенок может попасть в поле зрения не только педиатра, но и хирурга, кардиолога, онколога. Диагностика предполагает клинический осмотр младенца, сбор подробного анамнеза (течения беременности и семейного), оценку стадии развития образования. Для уточнения объема и глубины поражения, определения его гемодинамических особенностей, топографии, а также для дифференциальной диагностики используют ультразвуковые методы обследования.
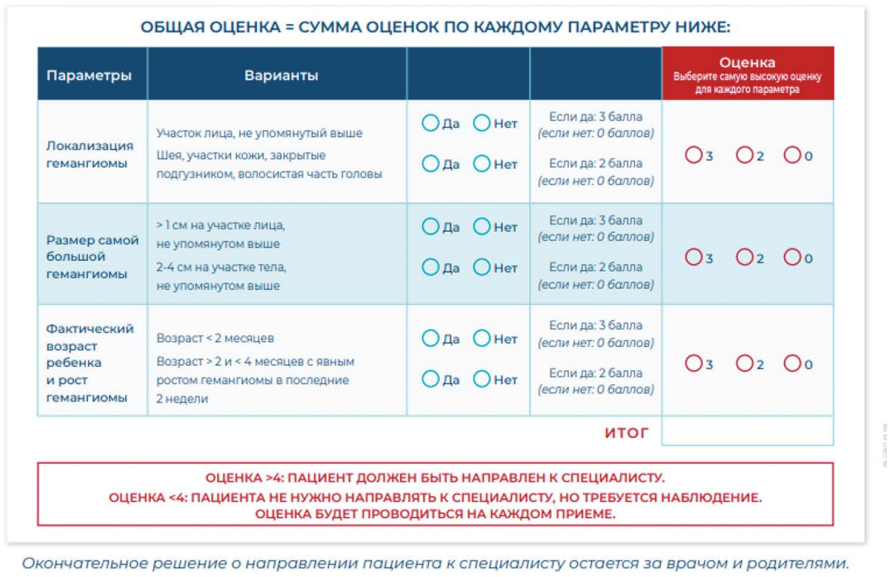
Для скрининга пациентов с ИГ на амбулаторном приеме и выявления тех, кому требуется системная терапия, применяется диагностическая шкала оценки IHReS, позволяющая провести первичную диагностику ИГ, быстро определить, нуждается ли ребенок в системной терапии, и направить его в специализированный стационар для начала системного лечения (рис. 1).
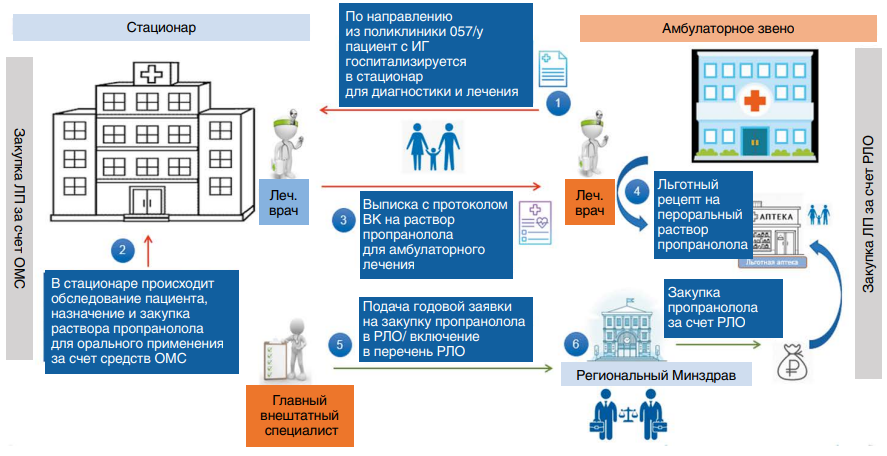
Все пациенты с впервые выявленной ИГ, которым требуется системная терапия (СТ), должны быть направлены в стационар для дообследования и начала СТ. На госпитализацию в стационар (специализированный центр) по лечению ИГ пациенты маршрутизируются из поликлиники по направлению № 057/у (рис. 2).

Детальная оценка топографии при необходимости хирургического вмешательства производится при помощи магнитнорезонансной или компьютерной томографии с контрастированием. Морфологические исследования (гистологическое, иммуногистохимическое) осуществляются для оценки пролиферативной активности клеток эндотелия и определения специфических белков-маркеров. При появлении стридорозного дыхания показано проведение прямой ларингоскопии для исключения подскладочной гемангиомы гортани, а при множественных кожных ИГ— УЗИ печени для исключения мультифокальных гемангиом.
К уникальным особенностям ИГ относятся:
- появление в течение первых недель жизни;
- быстрый рост с последующей постепенной медленной инволюцией;
- положительное иммуногистохимическое окрашивание биопсийных образцов на белок-транспортер глюкозы эритроцитарного типа (GLUT-1). GLUT-1 экспрессируется на протяжении жизненного цикла ИГ и может использоваться для дифференциальной диагностики ИГ и сосудистых мальформаций.
ГИПОТЕЗЫ ПАТОГЕНЕЗА
Этиология ИГ неизвестна. Предложен ряд гипотез патогенеза — например, теория происхождения из плаценты с участием внутренних и внешних триггерных факторов. К эндогенным триггерным факторам относятся нарушения регуляции ангио- и васкулогенеза. Из внешних провоцирующих факторов наиболее значима пренатальная гипоксия (ПГ), а именно анемия беременных, гестоз, обвитие плода пуповиной, фетоплацентарная недостаточность, многоплодная беременность и др. ПГ способствует формированию ИГ за счет активации ангиогенных факторов, приводящих к гиперплазии эндотелия капилляров. Сочетание внутриутробной гипоксии с повышенной частотой этих образований у маловесных новорожденных и недоношенных подтверждает данную гипотезу.
Актуальность проблемы ИГ определяется высокой распространенностью, ранним началом заболевания (с периода новорожденности), частым развитием осложнений в виде изъязвлений, нагноений, кровотечений. У данной категории педиатрических больных в дальнейшем наблюдаются функциональные и эстетические нарушения, которые могут стать причиной дыхательной недостаточности при подскладочных гемангиомах гортани, сердечной недостаточности и легочной гипертензии при гемангиомах печени, амблиопии при гемангиомах периорбитальной области. Остаточные явления в виде рубцов, атрофии и фиброзножировых изменений нередко бывают причиной психологического стресса у детей и родителей. Формы и типы ИГ представлены в таблице.

АЛГОРИТМ ЛЕЧЕНИЯ
Традиционно при выявлении ИГ применялись консервативные и инвазивные методы лечения с локальным или системным воздействием. Стратегия выбора того или иного метода зависит от возраста пациента, размера, формы и типа, стадии и локализации сосудистого образования. В качестве лекарственных средств использовались глюкокортикостероиды (ГКС), винкристин, интерферон, а в качестве инвазивных методов воздействия на ИГ—криодеструкция, лазерная хирургия, склерозирование и эмболизация питающих сосудов, хирургическое удаление. Сейчас ряд ранее применявшихся методов нельзя считать адекватным. Один из наиболее распространенных подходов к лечению пролиферирующей ИГ — системная фармакотерапия. Ранее в этом качестве широко использовались ГКС, однако их применение у детей ограничено побочными эффектами.
Современная терапия первой линии при ИГ предполагает применение блокаторов β-адренорецепторов. После случайного открытия в 2008 году в Европе влияния пропранолола на ИГ медикаментозная терапия данным препаратом во всем мире стала самым распространенным консервативным методом лечения этой патологии с доказанной эффективностью.
Пропранолол относится к неселективным бета-адреноблокаторам. Препарат конкурентно блокирует как β-1-адренорецепторы, находящиеся в сердце, так и β-2-адренорецепторы, которые преимущественно локализуются в бронхах и периферических сосудах.
Случайно обнаруженный положительный эффект пропранолола при лечении ИГ основан на способности препарата вызывать периферическую вазоконстрикцию, в том числе и в сосудах ИГ, благодаря уменьшению образования и высвобождения мощного вазодилататора — оксида азота (NO). Кроме того, пропранолол ингибирует процессы ангиогенеза, снижая экспрессию VEGF (васкулоэндотелиального фактора роста) и FGF (фактора роста фибробластов). В процессе ангиогенеза также принимают участие матриксные металлопротеиназы (ММР-2 и ММР-9), уровень которых повышается в фазе пролиферации инфантильных гемангиом. Их деятельность регулируется β-адренорецепторами. Пропранолол ингибирует активность ММР-2 и ММР-9, снижая тем самым интенсивность ангиогенеза. Также установлено, что пропранолол запускает процессы апоптоза эндотелиальных клеток.
Вследствие периферической вазоконстрикции на фоне приема пропранолола уменьшается скорость кровотока в ИГ. В результате системного воздействия сосудистая опухоль бледнеет, делается менее плотной, снижается местная температура. И все это появляется уже на вторые сутки от начала приема препарата.
До недавнего времени лечение пропранололом относилось к терапии оff-label, поскольку проводилось с отступлениями от инструкции по применению препарата. В связи с этим оно оказывалось возможным только после получения разрешения соответствующих этических комитетов медицинских учреждений и информированного согласия родителей.
Сегодня в мире, включая Россию, пропранолол в виде раствора для приема внутрь официально зарегистрирован для лечения пролиферирующих ИГ у детей, требующих системной терапии, в виде препарата Гемангиол (Hemangiol, Pierre Fabre DERMATOLOGIE, Франция) как новый стандарт лечения. Это специальная пероральная форма пропранолола для детей в виде сиропа. Многоцентровые плацебо-контролируемые исследования применения препарата Гемангиол показали положительную динамику после 5 недель лечения у 88 % пациентов. А к 24-й неделе лечения терапевтическая эффективность была доказана у 60 % больных. После подтверждения эффективности и благоприятного профиля безопасности препарат был включен в европейские и американские международные рекомендации по лечению ИГ. Сегодня это первый и единственный педиатрический препарат, одобренный для лечения данной патологии.
Применение других бета-блокаторов, в частности атенолола и надолола, которые иногда назначают как в России, так и за рубежом, относится к оff-lable терапии. Кроме того, следует отметить, что атенолол обладает большей кардиоселективностью, чем пропранолол, следовательно, имеет большее влияние на сердечно-сосудистую систему.
Хирургическое лечение в наши дни применяется у детей с угрожающими жизни обструктивными ИГ различных локализаций, а также при неэффективности лекарственной терапии. Кроме того, хирургический метод нашел применение при ИГ в стадии инволюции с остаточными деформациями кожи, атрофическими и гипертрофическими рубцами, участками растянувшейся, потерявшей эластичность кожи, а также остаточной фиброзно-жировой тканью, создающей избыточные объемы, что приводит к значительным эстетическим и функциональным нарушениям. Преимущество хирургического лечения именно на стадии инволюции обусловлено уменьшением риска кровотечения и потенциально меньшим размером поражения в связи с естественным течением процесса.
Определенное место в программе лечения ИГ занимает селективная лазеротерапия, в том числе применение импульсных лазеров на красителе (ИЛК), которые превосходят по эффективности другие типы лазеров. Использование ИЛК—эффективный и безопасный метод удаления остаточной эритемы и поверхностных телеангиоэктазий в регрессирующих гемангиомах. Наиболее оправданно оно при поверхностных (простых) ИГ небольших размеров.
Местное лечение аппликациями пропранолола (препарат Тимолол) эффективно только при простых ИГ небольших размеров.
С 2010 г. на базе Перинатального кардиологического центра при ГКБ № 67 и кардиологического отделения ДГКБ им. З.А. Башляевой ДЗМ совместно с кафедрой госпитальной педиатрии им. академика В.А. Таболина ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» проводится медикаментозное лечение неселективным β-адреноблокатором пропранололом детей с ИГ различной локализации, включая печень, гортань, а также наиболее тяжелых больных с PHACE(S)-синдромом. Только за период 2019–2021 гг. 80 детей были пролечены препаратом Гемангиол. Все они обследовались и лечились согласно разработанному коллективом авторов протоколу с динамической оценкой эффективности и безопасности проводимой терапии, включая оценку состояния сердечно-сосудистой системы.
Накопленный опыт успешного применения пропранолола в форме раствора для приема внутрь (более 600 пациентов) позволил создать на базе кардиологического отделения ДГКБ им. З.А. Башляевой Центр компетенции по лечению ИГ у детей, где в рамках системы ОМС проводятся комплексное лабораторно-инструментальное обследование (рис. 1–2), системная фармакотерапия и динамическое наблюдение за пациентами с ИГ, осуществляется индивидуальный подход к назначению пропранолола, коррекции доз препарата, а также к продолжительности лечения для достижения максимальной его эффективности и минимизации риска развития рецидивов (ребаунд-синдром).
Составленный и внедренный в клиническую практику алгоритм ведения пациентов с ИГ, слаженная работа команды специалистов — детских кардиологов, офтальмологов и оториноларингологов, врачей функциональной и ультразвуковой диагностики, хирургов и специалистов по лазерному лечению — позволяют избегать применения агрессивных методов терапии данной патологии и повышать качество жизни маленьких пациентов

















