Статьи
Хроническая сердечная недостаточность при сахарном диабете: от патофизиологии к стратегиям профилактики и лечения
Авторы:
- Бондаренко Ирина Зиятовна, врач кардиолог, доктор медицинских наук, главный научный сотрудник отделения кардиологии, эндоваскулярной и сосудистой хирургии ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва.
- Шацкая Ольга Александровна, врач кардиолог-эндокринолог, кандидат медицинских наук, ведущий научный сотрудник отделения кардиологии, эндоваскулярной и сосудистой хирургии ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва, член Московской городской ассоциации эндокринологов, Национальной ассоциации диетологов и нутрициологов, Межнационального центра исследования качества жизни.
- Иванцова Екатерина Владимировна, научный советник проекта PMI Science.
2. Эпидемиология ХСН
3. Этиология ХСН
4. Патогенез ХСН
5. Классификация ХСН
6. Клинические признаки и симптомы ХСН
7. Диагностика ХСН при СД
8. Лечение ХСН
8.1 Модификация образа жизни
8.1.1. Рекомендации по питанию
8.1.2. Рекомендации по физической активности [1, 2, 9, 12].
8.1.3. Отказ от курения
8.2. Общие принципы фармакотерапии при ХСН [1].
8.3. Лечение СД при наличии ХСН [1, 2].
9. Заключение
1. Определение
Хроническая сердечная недостаточность (ХСН) — это синдром, развивающийся в результате нарушения способности сердца к наполнению и (или) опорожнению, протекающий в условиях дисбаланса вазоконстриктивных и вазодилатирующих нейрогормональных систем, сопровождающийся недостаточной перфузией органов и систем и проявляющийся жалобами — одышкой, слабостью, сердцебиением и повышенной утомляемостью и, при прогрессировании, задержкой жидкости в организме (отечным синдромом) [1].
2. Эпидемиология ХСН
Эпидемия ХСН стремительно растет, оставаясь серьезной клинической проблемой и проблемой общественного здравоохранения. Общее число пациентов, имеющих ХСН, ежегодно увеличивается. По данным российских эпидемиологических исследований, распространенность ХСН в общей популяции составила 7 %, в том числе клинически выраженная — 4,5 %, увеличиваясь от 0,3 % в возрастной группе от 20 до 29 лет до 70 % у лиц старше 90 лет [1].
3. Этиология ХСН
Растет число факторов сердечно-сосудистого риска и сопутствующих заболеваний, влияющих на прогноз сердечной недостаточности, включая старение населения в целом.
Несколько популяционных исследований изучили общие факторы, предрасполагающие к развитию ХСН. В первую очередь это ИБС, сахарный диабет (СД), артериальная гипертония (АГ), ожирение и курение.
Ниже представлена классификация причин ХСН [1]:
1. ИБС;
2. Артериальная
гипертензия;
3. Кардиомиопатии:
1) семейные: гипертрофическая,
дилатационная, рестриктивная кардиомиопатии, аритмогенная дисплазия ПЖ,
некомпактный миокард ЛЖ;
2) приобретенные: миокардиты,
воспалительная кардиомиопатия:
а) инфекционные: вирусные,
бактериальные, грибковые, риккетсиозные, паразитические,
б) иммунные: столбнячный токсин,
вакцины, лекарственные препараты, сывороточная болезнь, гигантоклеточный
миокардит, аутоиммунные заболевания, саркоидоз, эозинофильный миокардит,
в) токсические: химиотерапия,
кокаин, алкоголь, тяжелые металлы (медь, железо, свинец);
4. Эндокринные / нарушение
питания: феохромоцитома, дефицит витаминов (например, тиамина), дефицит селена,
карнитина, гипофосфатемия, гипокалиемия, сахарный диабет, гипотиреоз
гипертиреоз;
5. Перипартальная;
6. Инфильтративная:
амилоидоз, гемохроматоз, гликогенозы, злокачественные заболевания;
Сахарный диабет
является сильным фактором риска развития ХСН, при повышении гликированного
гемоглобина на 1 % риск развития ХСН повышается на 8–36 % [2]. При СД
структура сердечной мышцы, как основа для развития ХСН неишемического генеза,
меняется задолго до появления коронарного атеросклероза.
Согласно российским клиническим рекомендациям по лечению сахарного диабета у взрослых, опубликованных в 2022 году, рекомендуется исследование уровня натрийуретических пептидов (натрийуретический пептид В-типа и N-терминальный фрагмент натрийуретического пропептида В мозгового (NT-proBNP) в крови) у пациентов с СД 2 с целью верификации ХСН. Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5). Исследование уровня NT-proBNP позволит определить генез одышки, особенно у пациентов с диабетической нефропатией. Кроме того, в обязательное обследование пациентов с СД и подозрением на ХСН входит выполнение Эхо-КГ.
В случае присоединения заболеваний, ассоциированных с атеросклерозом, дальнейшее течение сердечной недостаточности в популяции СД приобретает драматический характер. В причинах ее развития, помимо уже перечисленных, все большее значение приобретает ожирение. Сочетание ожирения и СД существенно утяжеляет прогноз ХСН.
Существует прямая связь между массой тела и параметрами диастолической дисфункции ЛЖ. В то же время индекс массы тела связан с повышенным риском развития сердечно-сосудистых заболеваний (ССЗ) главным образом благодаря его связи с другими факторами риска, в частности курением [2].
В качестве маркера степени гипоксии у пациентов с СД, ожирением и ХСН может быть использовано измерение пикового потребления кислорода во время проведения спироэргометрического теста. Оценка динамики показателей кардиореспираторной системы во время теста также информативна в качестве показателя эффективности лечения ХСН. В некоторых странах спироэргометрия включена в стандарты медицинской помощи [3].
Известно, что ожирение — это не только избыточная жировая, но и мышечная масса тела, включая массу миокарда[VE1] . Именно мышечная масса «парадоксальным» образом связана с улучшением работы кардиореспираторной системы, основной детерминанты формирования устойчивости к гипоксии [4]. Увеличение ударного объема левого желудочка (ЛЖ) и, соответственно, сердечного выброса ЛЖ создает условия для формирования компенсаторной гипертрофии миокарда и диастолической дисфункции ЛЖ. Эти механизмы способны длительно компенсировать кислородный долг тканям организма. В дальнейшем развивается систолическая дисфункция миокарда с постепенным снижением фракции выброса ЛЖ. В последних исследованиях «парадокс ожирения» был подтвержден не только для ХСН с сохраненной фракцией выброса ЛЖ (СН-сФВ), но и для более тяжелой ее формы — ХСН со сниженной насосной функцией ЛЖ (СН-нФВ) [4, 5].
СД регистрируется примерно у 40 % пациентов с СН-нФВ и у 45 % пациентов с СН-сФВ. Диабет и ожирение влияют на сократительную функцию ЛЖ даже в отсутствие ИБС и АГ. Важно отметить, что между СД и ХСН взаимосвязь является двунаправленной: сердечная недостаточность чаще развивается у пациентов с СД, а у пациентов с тяжелыми стадиями ХСН чаще развивается СД [6]. В свою очередь, при СД2 типа, особенно в сочетании с ожирением, нередко наблюдаются малоподвижный образ жизни и вредные привычки, что могут привести к снижению толерантности к физической нагрузке и замаскировать симптомы сердечной недостаточности.
Более высокий риск развития СД у пациентов с ХСН, наиболее вероятно, связан с нарушением у них чувствительности к инсулину: чем более выражена инсулинорезистентность, тем тяжелее протекает сердечная недостаточность. В крупнейшем исследовании CHARM за трехлетний период наблюдения у 8 % больных с ХСН развился СД. В свою очередь, пациенты с СД более тяжело болеют ХСН, чем лица без диабета, имеющие схожие показатели сократительной функции миокарда. У пациентов с диабетом более высока вероятность погибнуть вследствие сердечно-сосудистых заболеваний как ишемической, так и неишемической этиологии [6].
Недиагностированные случаи СД и предиабета одинаково часто встречаются в популяции с ХСН [6]:
В исследование PARADIGM-HF, в 13 % случаев у пациентов с ХСН не был диагностирован СД, в 25 % случаев — предиабет. В исследовании CHARM СД был не распознан с одинаковой частотой как у пациентов с сохраненной, так и сниженной фракцией выброса ЛЖ [6].
Рябцева Ольга Дмитриевна o.ryabtseva.2020@bk.ru 380642711709 Кандидат медицинских наук, нет Онкология - Онкогинеколог Луганский Республиканский Клинический Онкологический Диспансер, Главный врач
4. Патогенез ХСН
ИБС является наиболее частой причиной ХСН, когда коронарный кровоток и доставка кислорода к миокарду становятся недостаточными. На начальной стадии ХСН только в покое увеличение конечного диастолического давления (КДД) позволяет сохранять адекватный сердечный выброс (СВ). При нагрузке СВ никогда не достигает требуемой величины, при этом увеличения сократимости недостаточно, так как симпатический тонус уже и так повышен. При тяжелой декомпенсированной ХСН нормальный СВ не может быть достигнут даже в покое, несмотря на существенное повышение КДД.
При левожелудочковой недостаточности снижение сердечного выброса ведет к повышению КДД и давления в легочных венах. Это приводит к дилатации сердца, а повышение давления в легочных капиллярах — к задержке жидкости в интерстициальном пространстве легких. Увеличение крови и жидкости в легких делают их жесткими, что и является причиной одышки. Значительный подъем капиллярного давления способствует проникновению жидкости в альвеолы легких, что становится жизнеугрожающим из-за снижения газообмена и гипоксемии.
При недостаточности ЛЖ повышается давление в сосудах легких, что может приводить к перегрузке давлением и к недостаточности правого желудочка.
5. Классификация ХСН
В зависимости от фракции выброса (ФВ) левого желудочка сердца (ЛЖ) выделяют следующие формы ХСН [1]:
1.
ХСН со сниженной ФВ ЛЖ (ХСНнФВ) — ФВ
менее 40 %;
2.
ХСН с промежуточной ФВ ЛЖ (ХСНпФВ) —
ФВ 40–49 %;
3.
ХСН с сохраненной ФВ ЛЖ (ХСНсФВ) — ФВ
50 % и более.
6. Клинические признаки и симптомы ХСН
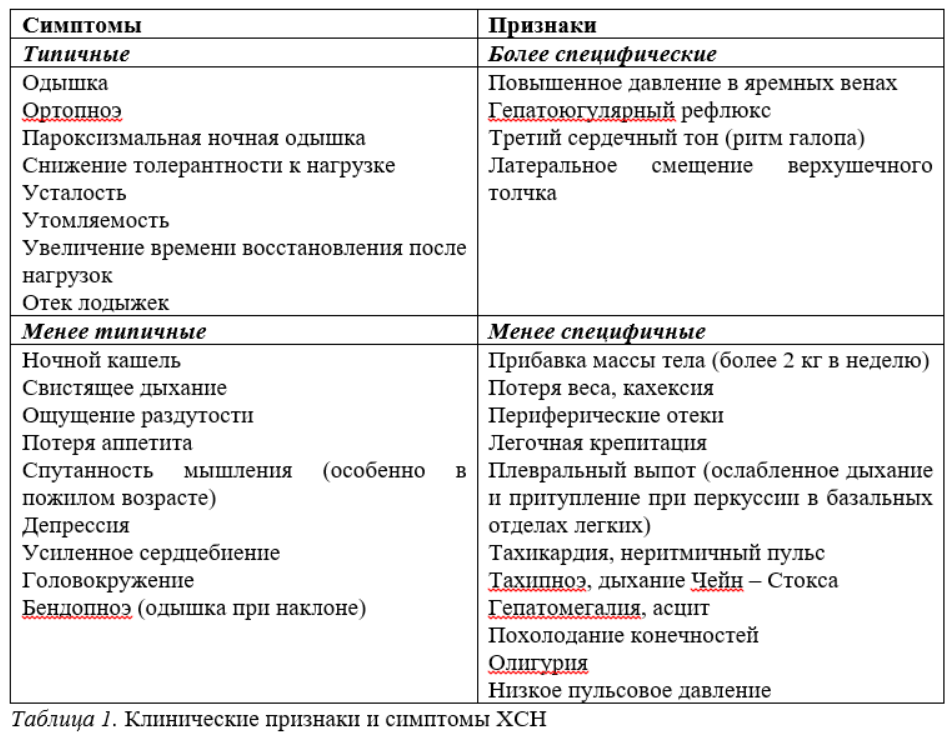
7. Диагностика ХСН при СД
По данным IDF Diabetes Atlas (2015), СД диагностирован у 415 млн человек, большинство из которых имеют ожирение. Еще у 316 млн лиц регистрируется нарушение толерантности к глюкозе.
Более 90 % пациентов с диагнозом СД — это пациенты с СД2 типа. Как правило, они заболевают во взрослом состоянии. Более 85 % больных СД 2-го типа имеют избыточную массу тела или ожирение. В подавляющем большинстве случаев пациенты с СД2 коморбидны, имеют инсулинорезистентность на фоне абсолютного или относительного дефицита собственного инсулина, а также микро и (или) макрососудистые заболевания, являющиеся самостоятельными или следствием хронической гипергликемии. Большинство пациентов уже имеют осложнения заболеваний, ассоциированных с атеросклерозом. Высокая смертность в этой популяции чаще всего вследствие ССЗ или заболеваний почек.
Около 10 % пациентов в структуре заболевших СД составляют пациенты с СД1 типа, болеющие с детства или с подросткового возраста. СД1 — это хроническое гетерогенное заболевание, вызванное аутоиммунным разрушением бета-клеток поджелудочной железы, что приводит к абсолютному дефициту инсулина. Нарушение секреции инсулина приводит к интенсивному перекисному окислению липидов и оксидативному стрессу, что нарушает углеводный, жировой и белковый обмены. СД 1 типа среди детей и подростков составляет до 90 % всех случаев заболевания. Дислипидемия у молодых пациентов с СД 1 типа встречалась в среднем у трех пациентов из четырех, что инициирует атерогенез и повышает сердечно-сосудистые риски в этой когорте более чем в 10 раз. CCЗ, как и у пациентов с СД 2, являются главной причиной смерти среди пациентов с СД1, составляя от четверти до половины всех причин смерти при длительности заболевания от 10 до 19 лет и более половины при длительности диабета 20 лет и более [7].
В условиях нарушения углеводного обмена и развития инсулинорезистентности патологические изменения в коронарных артериях и сердечной мышце рано стартуют, быстро прогрессируют, что затрудняет их своевременную диагностику. С каждым годом эти цифры растут.
Ключевые шаги в диагностике хронической сердечной недостаточности при СД
Диагноз ХСН требует наличие типичных клинических симптомов и объективных признаков дисфункции миокарда. Жалобы включают в себя одышку с постепенным снижением толерантности к физической нагрузке, быстрое утомление и симметричные отеки лодыжек. Однако эти симптомы недостаточно специфичны и могут служить лишь основой для дальнейшего обследования пациента и уточнения диагноза ХСН. В популяции СД эти жалобы могут отсутствовать или быть проявлением других коморбидных состояний: бессимптомное течение ИБС, хроническая болезнь почек в рамках диабетической нефропатии или декомпенсация углеводного обмена.
Обязательные обследования у пациентов с подозрением на ХСН включают в себя [1–3]:
- регистрацию электрокардиограммы (ЭКГ), которая представляет собой скрининговое исследование. ЭКГ без патологии делает диагноз ХСН маловероятным. ЭКГ может выявить такие нарушения ритма сердца, как фибрилляция предсердий, являющаяся причиной или следствием ХСН, рубцовые изменения в миокарде, наличие гипертрофии миокарда ЛЖ, расширенный комплекс QRS. Эти изменения увеличивают вероятность постановки диагноза ХСН и определяют дальнейшую стратегию обследования и лечения;
- рекомендуется измерять уровень натрийуретического пептида. Концентрация в плазме натрийуретического пептида B-типа (BNP) < 35 пг/мл, N-концевого натрийуретического пептида про-B-типа (NT-proBNP) < 125 пг/мл предполагает, что диагноз ХСН маловероятен. Степень повышения этого показателя свидетельствует о тяжести ХСН, а эффективность лечения определяется степенью его снижения. Тем не менее следует отметить, что существуют и другие причины повышения NT-proBNP: фибрилляция предсердий, возраст, острое или хроническое заболевание почек. И наоборот, его концентрация может быть непропорционально низкой при ожирении;
- биохимические показатели крови, такие как мочевина, электролиты, креатинин, ферменты печени и показатели функции щитовидной железы, общий анализ крови рекомендуются для исключения других патологических состояний, имеющие клиническое сходство с ХСН;
- эхокардиография (Эхо-КГ) рекомендуется в качестве ключевого исследования для диагностики ХСН. Помимо измерения ФВЛЖ, Эхо-КГ предоставляет информацию о размерах камер сердца, определяет наличие и тип гипертрофии миокарда ЛЖ (эксцентрический или концентрический), оценивает зоны нарушения локальной сократимости ЛЖ, степень легочной гипертензии, диастолическую функцию ЛЖ, выявляет клапанные пороки;
- рентген грудной клетки рекомендуется для определения других потенциальных причин одышки (например, заболевания легких), а также уточняющие параметры застойных изменений в легких на фоне ХСН.
8.1.1. Рекомендации по питанию
При ХСН диета, особенно в сочетании с правильно подобранной физической активностью, способствует обратному ремоделированию миокарда, улучшает функцию сердца и прогноз больных. Суточная калорийность и соотношение макронутриентов рациона зависят от ИМТ, композиционного состава тела и энерготрат покоя.
Потеря избыточного веса от 5 до 10 % связана с уменьшением риска развития сахарного диабета 2 типа и ишемической болезни сердца. В качестве начальной цели рекомендуется снижение массы тела не менее чем на 5 %, а достижение 5 % потери массы тела считается успехом при оценке ответа на терапию. Питание должно оказывать благотворное влияние не только на состав макронутриентов, направленный на создание отрицательного энергетического баланса, но также должны на чувство сытости, аппетит и чувствительность к инсулину.
ИМТ позволяет оценить степень соответствия массы человека и его роста и тем самым косвенно судить о том, является ли масса недостаточной, нормальной или избыточной. ИМТ рассчитывается по формуле ИМТ = масса тела (кг) : рост (м)².

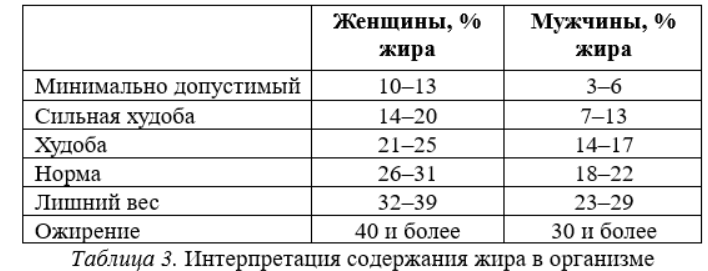
Дополнительно можно использовать данные биоимпедансометрии для оценки композиционного состава тела, так как у спортсменов за счет мышечной массы ИМТ может быть выше 30, при этом содержание жира в теле будет в норме, а у пожилых людей ИМТ может быть менее 25 за счет уменьшения мышечной массы и развития саркопении, при этом содержание жира в организме может быть избыточным.
Ожирение развивается вследствие нарушения энергетического баланса организма, когда поступление энергии с пищей превышает энергетические расходы организма.
Энергетические затраты организма складываются из следующих компонентов:
- энерготрат основного обмена;
- затрат энергии на физическую активность;
- специфического динамического действия пищи (пищевой термогенез, вызываемый приемом пищи);
- затрат энергии на рост и образование тканей (у детей, беременных и кормящих грудью женщин).
Для оценки суточного расхода энергии (СРЭ) можно воспользоваться следующей формулой: СРЭ = ВОО × КФА, где ВОО — величина основного обмена, КФА — коэффициент физической активности.
Также используется формула ВОЗ (1998), в которой учитывается не только коэффициент физической активности, но и пол, возраст и вес человека.
Для женщин:
18–30 лет (0,062 × вес в кг + 2,036) ×
240 × КФА
31–60 лет (0,034 × вес в кг + 3,538) ×
240 × КФА
старше 60 лет (0,038 × вес в кг + 2,755)
× 240 × КФА
Для мужчин:
18–30 лет (0,063 × вес в кг + 2,896) ×
240 × КФА
31–60 лет (0,484 × вес в кг + 3,653) ×
240 × КФА
старше 60 лет (0,491 × вес в кг + 2,459)
× 240 × КФА
Для расчета величины основного обмена
Формула Харриса – Бенедикта
Для женщин:
ВОО = 655 + (9,6 × вес, кг) + (1,8 × рост,
см) — (4,7 × возраст, г)
Для мужчин:
ВОО = 66 + (13,7 × вес, кг) + (5,0 × рост,
см) — (6,8 × возраст, г)
Формула Кэтча-Макардла
ВОО = 370 + (21.6 × безжировая масса, кг)
В зависимости от нагрузки выделяют следующие коэффициенты физической активности, см. таблицу 4.

Для снижения веса основным условием является создание дефицита калорий. Это достигается за счет уменьшения поступления энергии с пищей (от 1200 до 1500 ккал/сут для женщин и от 1500 до 1800 ккал/сут для мужчин с учетом массы тела и физической активности или снижение суточной калорийности на 15–20 % от исходного) и (или) увеличения расхода энергии. Возможен подход libitum — формальный показатель дефицита энергии не предписан, однако снижение суточной калорийности достигается путем ограничения или исключения определенных групп продуктов или использование заменителей пищи. С точки зрения дефицита калорий, выбор конкретной диеты менее важен. Оптимальная скорость потери веса составляет 0,5–1,0 кг в неделю.
Избыточное ограничение энергетической ценности может привести к снижению мышечной массы и развитию саркопении, повышению риска травматизма, снижению иммунитета, нарушению пищевого поведения, возникновению вторичного гиперальдостеронизма и прогрессированию ХСН.
Рекомендуемое распределение основных компонентов пищи в суточной калорийности: 55–70 % углеводов (из них до 10 % простыми), 10–15 % белков и 20–30 % жиров.
Рассмотрим основные принципы диетотерапии при ХСН [8–10].
1) Ограничение количества соли в рационе до 2,0–2,5 г в сутки. Не рекомендуется использование соли при приготовлении пищи. При нормализации уровня АД допустимо увеличение соли в рационе до 3,0–3,5 г для подсаливания готовой пищи. Повышенное количество натрия содержится в готовых продуктах:
a)
продукты, содержащие глутамат натрия;
i)
копченое мясо, окорок, бекон, солонина,
мясная нарезка, сосиски, колбасы;
ii) соленое
масло, маргарин, все виды твердых и мягких сыров;
iii) мясные
и рыбные блюда быстрого приготовления (полуфабрикаты);
iv) копченая
и консервированная рыба и морепродукты;
v) жареные
и соленые орешки, арахисовое масло, чипсы;
vi) соусы,
подливки, кетчупы, заправки для салата, маринады;
vii) все
виды супов быстрого приготовления, бульонные кубики.
2) Достаточное употребление белка (0,8–1,3 г/кг идеальной массы тела) в соответствии с физиологической потребностью, характером физической нагрузки, учитывая также наличие сопутствующей патологии. Белок необходимо употреблять в каждый прием пищи, то есть равномерно распределять в течение суток. В рационе должен присутствовать как животный, так и растительный белок. Источники животного белка: мясо, яйца, творог, молочные продукты, птица, рыба, морепродукты, субпродукты. Источники растительного белка: злаки и бобовые, однако нужно иметь в виду, что растительные белки хуже усваиваются и обладают меньшей биологической ценностью.
3) Оптимальное содержание омега-3 полиненасыщенных жирных кислот (ПНЖК) в рационе (оптимальное соотношение омега-3 и омега-6 в рационе — 1 : 5–10). Омега-3 ПНЖК содержатся в авокадо, орехах, семечках, маслах холодного отжима, водорослях, рыбе, выращенной в естественных экологически чистых условиях. Необходимо исключить продукты, в состав которых входят трансжиры, которые не усваиваются в организме (на этикетках они могут быть указаны как растительный жир, маргарин, заменитель масла какао, кондитерский жир, заменитель молочного жира, растительные сливки, гидрогенизированное масло и др.). Примеры продуктов с трансжирами: готовые ресторанные продукты, магазинные десерты, замороженное тесто, маргарин, фастфуд, мороженое, чипсы, полуфабрикаты, пицца, продукты в панировке, промышленные соусы.
4) Использование продуктов, богатых калием и магнием. Продукты, богатые калием: отруби, грибы, орехи макадамия и миндаль, темно-зеленые овощи, авокадо, абрикосы, фрукты и тыквенные семечки. Продукты, богатые магнием: тыквенные семечки, льняное и кунжутное семя, орехи. Суточное количество поступающего калия с питанием необходимо увеличить до 4–5 г в день и магния до 0,8–1,0 г в сутки. Соотношение калия и натрия в рационе — более 2,5–3,0.
5) Ограничение рафинированных углеводов в диете до 35–40 г в сутки (например, белый и темный рафинированный сахар, мед, кленовый сироп, кукурузный сироп, кукурузный сироп с фруктозой, карамель, десерты с перечисленными подсластителями, сладости и др.), а при гипокалорийном питании — полное исключение.
6) Дробный режим питания, включающий три основные приема пищи и 1–2 перекуса в течение дня позволит распределить калорийности пищи (оптимальное распределение макронутриентов и регулярность приема пищи). Последний прием пищи должен быть не позднее чем за 2–3 часа до сна. Важно учитывать циркадные ритмы, то есть оптимальное временное окно приема пищи.
7) Необходимо следить за объемом употребляемой жидкости. В сутки следует
i)
выпивать от 1,5 до 2,0 л жидкости. При
необходимости (по рекомендации
ii) врача)
ограничивается количество жидкости (до 800 мл — 1 л в сутки).
В Копенгагенском общем популяционном исследовании представлены таблицы десятилетнего риска сердечно-сосудистых заболеваний, основанных на соблюдении диетических рекомендаций или уровнях холестерина, не связанных с ЛПВП. Десятилетний абсолютный риск определяется путем определения пола, статуса курения, возрастной группы, систолического артериального давления и диетической группы (левая диаграмма) или уровня холестерина без ЛПВП (правая диаграмма).
Рисунок 1. Таблицы десятилетнего риска сердечно-сосудистых заболеваний
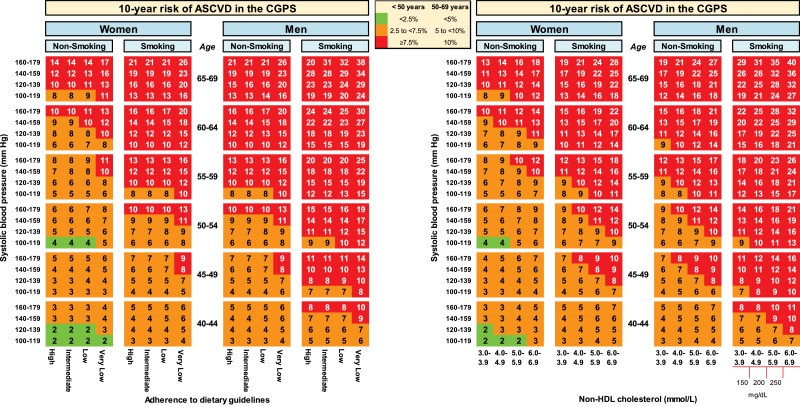
Самый высокий десятилетний абсолютный риск для мужчин в 38 % наблюдается у мужчин в возрасте 65–69 лет с очень низким соблюдением диетических рекомендаций, систолическим артериальным давлением между 160 и 179 мм рт. ст., и которые были курильщиками. Соответствующий десятилетний абсолютный риск для женщин составляет 32 %.
Десятилетние диаграммы абсолютного риска для ASCVD, включающие диетическую оценку или холестерин без ЛПВП как для мужчин, так и для женщин, могут быть аргументом в пользу убеждения пациентов придерживаться рекомендаций по питанию. Диаграммы, включающие диетический риск, могут использоваться при оценке риска развития сердечно-сосудистых заболеваний у пациента или при обсуждении изменения привычек образа жизни. Таким образом, целевая стратегия профилактики соответствует профилю пациента и предпочтениям, как рекомендовано в руководящих принципах ESC по ССЗ 2021 годам [11].
8.1.2. Рекомендации по физической активности [1, 2, 9, 12].
По данным проведенных клинических исследований, физическая активность (ФА) улучшает структурно-функциональные параметры миокарда, снижает количество госпитализаций в связи с декомпенсацией сердечной недостаточности, снижает уровень сердечно-сосудистой смертности и улучшает качество жизни больных ХСН.
ФА подбирается индивидуально с учетом возраста больного, осложнений СД, сопутствующих заболеваний в зависимости от функционального класса ХСН, но противопоказана при декомпенсации ХСН и других острых состояниях (например, при миокардитах, нарушениях ритма сердца высоких градаций, нестабильной стенокардии, при тяжелом стенозе клапанных отверстий и др).
Временные противопоказания к физической активности (ФА) у больных СД:
· уровень глюкозы плазмы (ГП) > 13 ммоль/л в сочетании с кетонурией или > 16 ммоль/л даже без кетонурии (в условиях дефицита инсулина ФА будет усиливать гипергликемию);
· гемофтальм, отслойка сетчатки, первые полгода после лазеркоагуляции сетчатки;
· неконтролируемая артериальная гипертензия.
Для профилактики гипогликемии при длительной ФА (более 2 часов) рекомендуется снижение дозы инсулина, поэтому длительные нагрузки должны быть запланированными:
· уменьшить дозу препаратов инсулина короткого и ультракороткого действия и продленного действия, которые будут действовать во время и после ФА, на 20–50 %, или установить временную базальную скорость инфузии инсулина при использовании помповой инсулинотерапии;
· при очень длительных и (или) интенсивных ФА: уменьшить дозу инсулина, который будет действовать ночью после ФА, иногда — на следующее утро, или установить временную базальную скорость использования помповой инсулинотерапии;
· во время и после длительной ФА: дополнительный самоконтроль гликемии каждые 2–3 часа, при необходимости — прием 1–2 ХЕ медленно усваиваемых углеводов (при уровне глюкозы плазмы [ГП] менее 7 ммоль/л) или быстро усваиваемых углеводов (при уровне ГП менее 5 ммоль/л).
Для профилактики гипогликемии при кратковременной ФА (не более 2 часов) рекомендуется дополнительный прием углеводов:
· измерить гликемию перед и после ФА и решить, нужно ли дополнительно принять 1–2 ХЕ (медленно усваиваемых углеводов) до и после ФА;
· при исходном уровне ГП выше 13 ммоль/л или если ФА имеет место в пределах 2 часов после еды, дополнительный прием ХЕ перед ФА не требуется;
· в отсутствие самоконтроля необходимо принять 1–2 ХЕ до и 1–2 ХЕ после ФА.
Во время ФА нужно иметь при себе углеводы в большем количестве, чем обычно: не менее 4 ХЕ при кратковременной и до 10 ХЕ при длительной ФА.
В зависимости от переносимости физических нагрузок больным ХСН рекомендуются разные виды аэробных нагрузок, упражнений на сопротивление, дыхательная гимнастика.
При I–II ФК ХСН длительность нагрузки может составлять 45 минут в день, допустимы ходьба, плавание, езда на велосипеде, бег на месте, выполнение упражнений на все группы мышц.
При III ФК ХСН длительность нагрузки может достигать 30 минут в день, рекомендуются дыхательная гимнастика, ходьба, плавание, выполнение упражнений на все группы мышц.
При IV ФК ХСН длительность нагрузки может быть 10–15 минут в день, достигать 30 минут в день, рекоменду.тся дыхательная гимнастика, ходьба, плавание, выполнение упражнений для мелких групп мышц.
Также рекомендуется постепенное начало и завершение физической нагрузки, избегать нагрузок сразу после еды, следует прекратить выполнение любых упражнений при появлении боли в груди, головокружения, общей слабости, одышки и т.д.
8.1.3. Отказ от курения
Одним из неблагоприятных предикторов развития ХСН, независимо от традиционных факторов риска, является никотиновая зависимость, развивающаяся при употреблении любых форм табака. В МКБ-10 с учетом выраженности симптомов отмены табачная зависимость отнесена к категории «Психические расстройства и расстройства поведения, обусловленные употреблением психоактивных веществ»: «Острая никотиновая интоксикация» (F17.0), «Синдром зависимости от табака» (F17.2) и «Синдром отмены табака» (F17.3).
Метаанализ Yang и соавт. показал, что курение сигарет повышает риск развития ХСН на 60 %, при этом риск развития сахарного диабета увеличивается в 1?5 раза (на 30–40 % для активных курильщиков) [13]. Курение является независимым фактором риска сахарного диабета 2 типа: влияние табачного дыма демонстрирует синергетическое взаимодействие со статусом низкой секреции инсулина (прогрессирующая потеря функции и массы β-клеток) и высокой инсулинорезистентностью для развития диабета [14, 15, 16]. Эти эффекты связаны с усилением действия свободных радикалов (нарушают гомеостаз сосудов и правильное функционирование эндотелия), хроническим воспалительным состоянием, окислительным стрессом, стрессом эндоплазматического ретикулома, митохондриальной дисфункцией, а также с накоплением церамидов [15, 17, 18, 19].
Отказ от курения — модифицируемый фактор риска, являющийся одним из самых действенных профилактических мер для улучшения прогноза заболевания.
При отказе от курения в организме происходят положительные изменения, в том числе снижение факторов риска ХСН:
· через 1 неделю восстанавливается обоняние и вкусовые ощущения, начинаются симптомы отмены;
· через 1 месяц улучшается работа ССС — становится легче ходить, одышка и кашель уменьшаются, снижается систолическое и диастолическое артериальное давление и частота пульса, при этом отмечается пик симптомов отмены [20];
· через 3 месяца улучшается работа ССС — становится легче ходить и заниматься спортом, снижаются респираторные симптомы, увеличивается аппетит и вес, наблюдается снижение гликилированного гемоглобина [21] и общего холестерина (у более молодых пациентов) [22], уровня альфа-1-антитрипсина [23];
· через 6 месяцев улучшается бронхиальная проходимость и уменьшаются симптомы у астматиков, улучшается аппетит, растет вес, также снижается уровень окислительного стресса [24];
· через 1 год улучшается функция легких, снижаются проявления ХОБЛ, снижается риск инфаркта миокарда и ИБС на 30–50 %, снижается прогрессирование хронического заболевания почек за счет улучшения микроальбуминурии без метаболических побочных эффектов у пациентов, у которых уже диагностирован сахарный диабет [20];
· через 2 года и далее между 5-м и 15-м годами риск инсульта такой же, как у некуривших;
· через 10 лет риск рака легких падает, через 15 лет риск инфаркта миокарда такой же, как у некуривших.
Важно учитывать, что риск развития сахарного диабета 2 типа выше среди бросивших курить недавно (не более 2–6 лет), по сравнению с курильщиками, в 1,22 раза. Он достигает пика через 5–7 лет, а затем постепенно снижается. Временное повышение риска диабета прямо пропорционально увеличению веса, при этом он не увеличивается среди бросивших курить без увеличения веса [25]. Набор веса при отказе от курения происходит из-за стремления избавиться от возникшего беспокойства на фоне синдрома отмены за счет увеличения потребления нездоровой пищи (никотин оказывает воздействие на центр голода и насыщения, поэтому у курильщиков нередко чувство голода снижено). Табачный дым нарушает метаболизм липидов, увеличивая риск развития атеросклероза или висцерального ожирения.
У бросивших курить не происходит временного увеличения смертности, независимо от изменения веса после прекращения курения [25]. Отказ от курения, независимо от увеличения веса, важен для снижения краткосрочного и долгосрочного риска развития сердечно-сосудистых заболеваний и общей смертности (улучшается гликемический контроль и кардиометаболические факторы риска, снижается риск микро- и макрососудистых осложнений) [26]. Следует внимательно следить за набором веса у пациентов после отказа от курения: необходимо придерживаться правильного питания. Европейские рекомендации по сердечно-сосудистой профилактике 2021 года предполагают информирование о том, что курение не помогает контролировать вес. Кроме того, курильщики на 47 % чаще испытывают нарушения сна, что также увеличивает риск ожирения и осложнения течения других заболеваний (на фоне усиления тревожных и депрессивных состояний) [27, 28, 29, 30]. Бессонница несет в себе риск неспособности бросить курить [31]. Эта зависимость прямо связана с количеством выкуренных сигарет в день и пачка-годами. Ожирение может привести к учащению курения, опосредованному несколькими факторами: скоплением нездорового поведения, например потреблением высококалорийных продуктов. Эти факторы могут создать цикл, способствующий курению среди населения с ожирением.
В настоящее время для пациентов разработаны две программы по отказу от курения: короткая и длительная. Также с пациентами проводятся мотивирующие беседы и никотинзаместительная терапия.
Короткая лечебная программа включает пять шагов.
1) спросить: опрос пациента о статусе курения в прошлом и настоящем;
2) сверить диагноз: оценивается степень никотиновой зависимости и желание пациента бросить курить;
3) советовать: с учетом индивидуальных особенностей советовать пациентам отказаться от курения;
4) содействовать: рекомендации по отказу от курения и назначение лечения;
5) следить: контроль выполнения рекомендаций, поддержка пациента.
Использование данный программы повышает отказ от курения в 1,7 раза.
Длительная лечебная программа включает стратегическое (лечение табачной зависимости) и мотивационное (повышение мотивации отказа от курения и последующее лечение) консультирование.
Фармакотерапия табачной зависимости включает никотинзаместительную терапию (назначение никотинсодержащих препаратов в виде жевательной резинки, ингалятора, пластыря, таблеток) и лечение никотиновой зависимости (варениклин, при невозможности использования варениклина возможно использование цитизина и нортриптилина).
При определении степени никотиновой зависимости коэффициент Фагерстрема более 5 баллов говорит об обязательности применения никотинсодержащих препаратов.
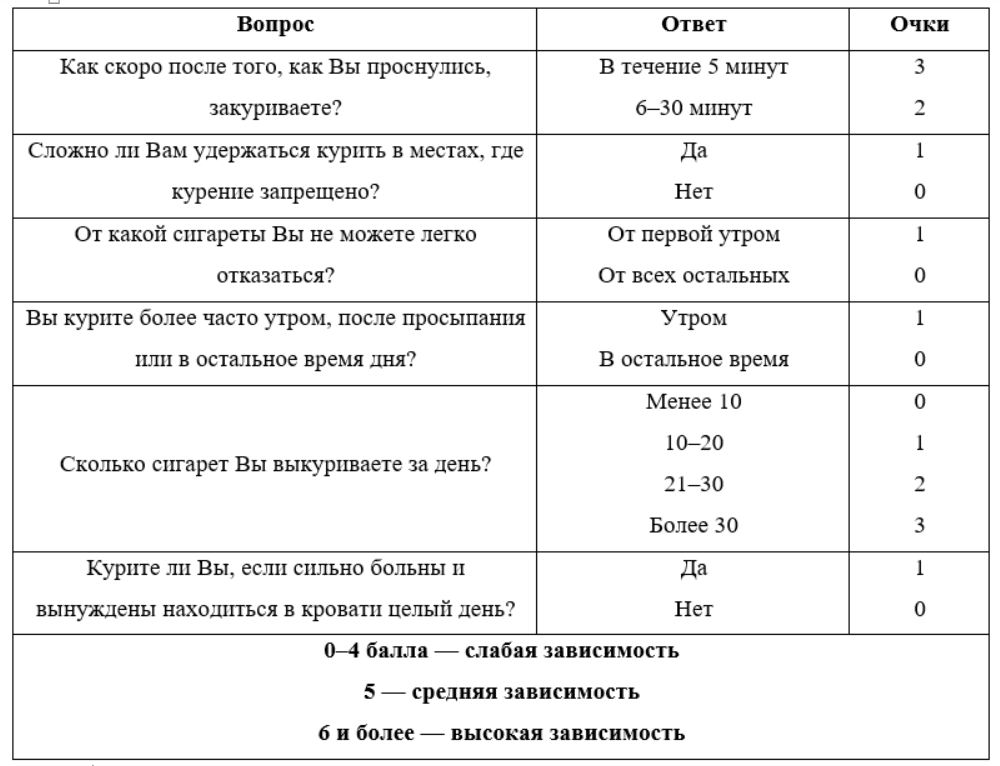
Таблица 5. Тест Фагерстрема
Еще одним показателем для начала медикаментозной терапии является количество выкуриваемых сигарет. Можно использовать индекс курильщика, равный количеству выкуриваемых в день сигарет, умноженному на 12. Индекс, превышающий значение 200, является признаком злостного курильщика с высокой степенью никотиновой зависимости.
Второй вариант расчета индекса «пачка-лет»: ИК «пачка-лет» = (количество сигарет в сутки × общий стаж курения (лет) / 20. Критическим уровнем индекса курильщика «пачка-лет» считается значение более 10.
Доказано, что применение лекарственных средств удваивает эффективность лечения никотиновой зависимости. Главной задачей терапии является предотвращение возобновления курения.
Наиболее важными немедикаментозными приемами отказа от курения являются следующие:
1) назначение даты отказа от курения, поддержка членов семьи, совместный с близкими отказ от курения, чтение печатных материалов, посвященных проблеме отказа от курения;
2) смена или модификация стереотипов, связанных с курением, увеличение контактов с некурящими, расширение круга удовольствий, не связанных с курением;
3) употребление большого количества жидкости, особенно воды и несладких, лучше кислых, соков, постоянное освежение полости рта;
4) отказаться от мысли, что одна или две сигареты не принесут вреда, но и не рассматривать отхождение от программы по отказу от курения, как неудачу и причину прекращения лечения;
5) использовать 3–5 раз в день простые дыхательные упражнения в сочетании с ходьбой: глубокий вдох на четыре шага с полным последующим выдохом (всего 10–20 шагов).
После того как врач рассказал пациенту о рисках продолжения курения и способах отказа от него и убедился, что в настоящее время пациент не мотивирован на отказ от курения (не готов или не хочет отказаться от табакокурения), врач может проинформировать пациента о концепции снижения вреда.
Концепция снижения вреда — стратегия, используемая в медицине и социальной сфере с целью максимального сокращения вреда, которому подвергается человек и (или) общество в результате опасных действий или поведения и который невозможно полностью исключить или предотвратить. Она может находить применение в минимизации рисков у группы пациентов, которые не готовы резко изменить свой образ жизни и полностью исключить риски: курение, физическая активность, диета. Наилучшую эффективность данная методика показывает у пациентов с очень выраженным аддиктивным влечением к никотину или отсутствием мотивации на отказ от курения.
Пациенту можно предложить перейти на альтернативные источники доставки никотина (они имитируют и заменяют потребление традиционных табачных изделий). Одним из примеров может служить электрическая система нагревания табака (ЭСНТ). В данном продукте, в отличие от классических сигарет, не происходит горение табака, а лишь нагревание до температуры 250–350 °С, соответственно резко снижается выброс вредных и потенциально вредных веществ, которые объединены термином «смолы» (смесь твердых частиц без воды и никотина), что, по результатам исследований, снижает риск развития ССЗ более чем на 92 % [32]. В процессе работы ЭСНТ не происходит химических реакций с выделением тепловой энергии. Аэрозоль, образующийся при нагревании табака, не содержит твердых частиц и, как следствие, не попадает под определения «дым». Количество выделяемых веществ из-за отсутствия окисления снижено более чем в 10 раз (около 7000 в дыме сигареты и 529 в аэрозоле СНТ).
При этом никотин как таковой не отвечает за активацию тромбоцитов или повышение уровня фибриногена в плазме, наблюдаемое у курильщиков. В настоящее время организации здравоохранения принимают и поддерживают точку зрения, что основными факторами развития болезней, связанных с курением, являются продукты горения, а не никотин [33].
Бездымные продукты вошли в алгоритмы Американской ассоциации кардиологов в 2018 году (рис. 2).
Рисунок 2. Тактика консультирования пациента, который не мотивирован в настоящее время на отказ от курения
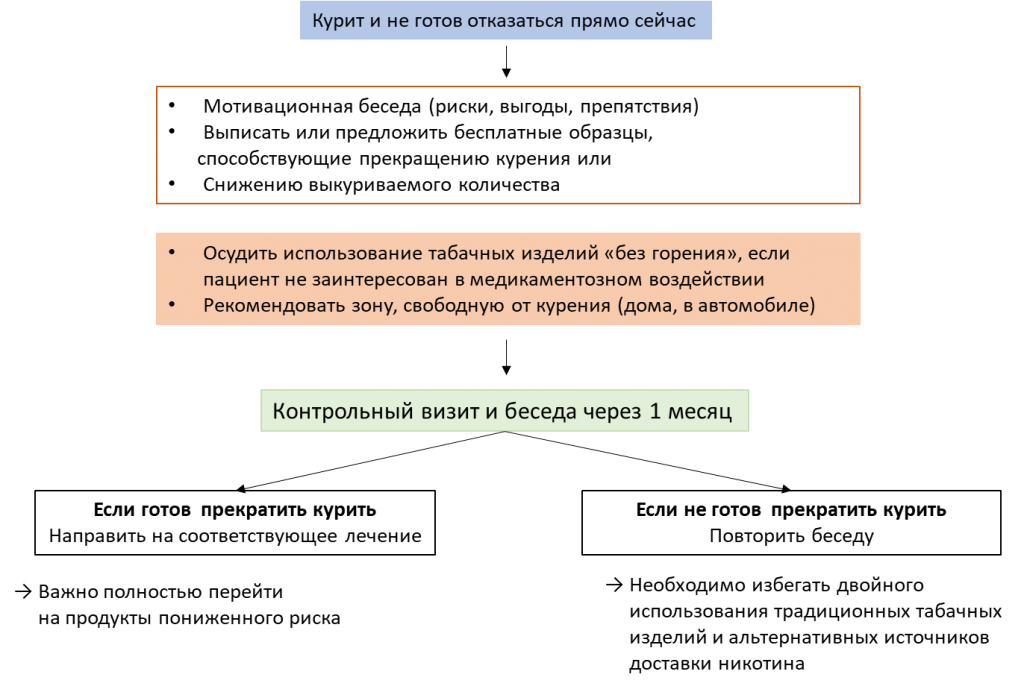
Важным моментом является избегание совместного применения табачных изделий и альтернативных систем доставки никотина, поскольку существует значительно более высокий риск ССЗ и их осложнений среди лиц, одновременно употребляющих электронные сигареты и традиционные табачные продукты, по сравнению только с курением табака [34].
7 июля 2020 года Управление по санитарному надзору за качеством пищевых продуктов и лекарственных средств США (FDA) опубликовало решение по заявкам на получение для электрических систем нагревания табака статуса «продукта с модифицированным риском».
Продукция с пониженным риском (ППР) — это термин для обозначения продукции, которая, вероятно, обладает или потенциально может обладать пониженным риском причинения вреда здоровью курильщиков, переключившихся на данные виды продукции, по сравнению с риском причинения вреда здоровью при продолжении курения сигарет.
На основании результатов независимых клинических исследований [35, 36, 37, 38, 39], можно считать, что полный переход на ЭСНТ с традиционных продуктов курения может быть связан с положительным влиянием на эндотелиальную дисфункцию и окислительный стресс и соответственно на риск развития заболеваний, связанных с курением, в том числе ХСН и сахарный диабет.
Важной особенностью личности, способствующей развитию табачной зависимости и препятствующей успешному отказу от курения, может являться наличие психических заболеваний. Повышенное желание курить может быть связано с важными регуляторами начала и прогрессирования заболевания [40].
Наличие курения в анамнезе и безуспешных попыток отказа должно являться поводом направления пациента к психологу для помощи в отказе и скрининге возможных психических заболеваний, способствующих табачной зависимости. Это особенно важно, поскольку различные когнитивные процессы, особенно зрительно-пространственные навыки и навыки внимания, полезны для отказа от курения, а эмоциональные состояния, такие как депрессия и тревога, оказывают негативное влияние [41].
Курение в молодом и пожилом возрасте имеет некоторые отличия (степень никотиновой зависимости у пожилых людей достоверно выше), что требует разных подходов в немедикаментозных мероприятиях в рамках программ отказа от курения в разных возрастных группах. Даже те, кто бросают курить гораздо позже, получают некоторые преимущества: в возрасте 65 лет ожидаемое увеличение продолжительности жизни — от 1,4 до 2,0 года для мужчин и от 2,7 до 3,7 года — для женщин; в возрасте 70–80 лет и старше также происходит снижение риска смертности от всех причин по сравнению с нынешними курильщиками [42].
Отказ от курения должен стать важнейшим компонентом лечения любого пациента на любой стадии развития заболеваний независимо от возраста. Комплексный подход с учетом сложности заболевания может быть наиболее эффективным методом терапии.
8.2. Общие принципы фармакотерапии при ХСН [1]
В многочисленных рандомизированных исследованиях было доказано, что блокирование ренин-ангиотензин-альдостероной системы (РААС) и симпатической нервной системы ингибиторами ангиотензинпревращающего фермента (иАПФ) / блокаторами АТ1-рецепторов (БРА) или ингибитором рецептора ангиотензина-неприлизина (ARNI), бета-адреноблокаторами, а также назначение антагонистов минералокортикоидных рецепторов улучшает качество жизни, увеличивает выживаемость, снижает риск госпитализации, особенно, у пациентов с СНнФВ. Комбинация иАПФ (или БРА), ARNI, бета-адреноблокаторов и антагонистов минералокортикоидов рекомендуется в качестве базового лечения этих пациентов, если нет противопоказаний. У пациентов с СД необходим тщательный контроль функции почек, особенно если ранее применялось эндоваскулярное лечение заболеваний, ассоциированных с атеросклерозом. Дозы должны быть оттитрованы до эффективных, используемых в клинических испытаниях (или до максимально переносимых, если это невозможно).
Если сохраняются симптомы ХСН, рекомендуется использовать АРНИ в качестве замены ингибиторов АПФ. Рекомендуемые дозы этих препаратов указаны в таблице 1. При непереносимости иАПФ назначаются БРА в эффективных дозах или ARNI.
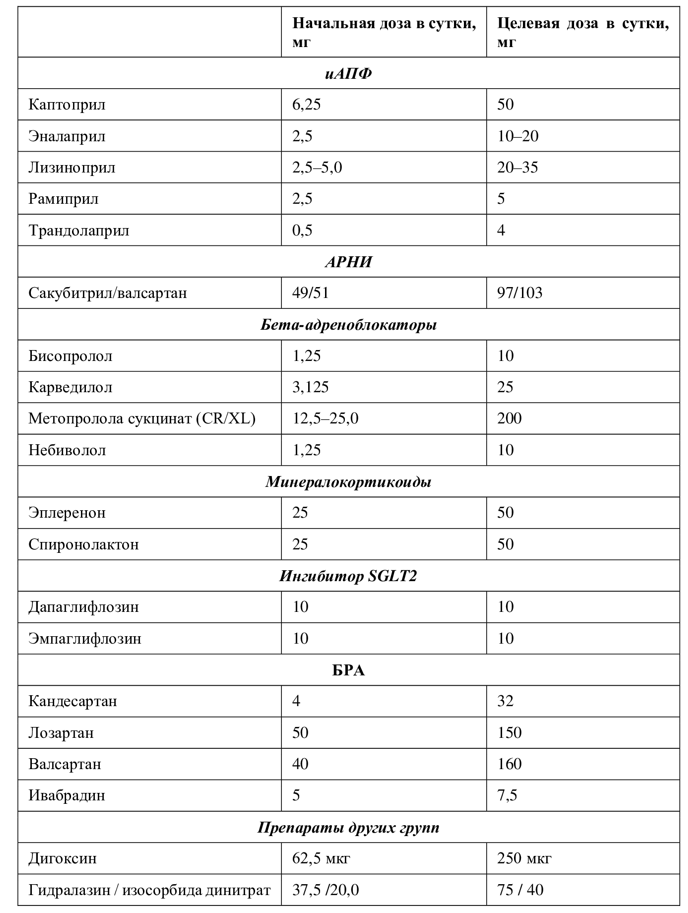
Таблица 6. Дозы препаратов, используемые в ключевых рандомизированных исследованиях у пациентов с ХСН со сниженной фракцией выброса ЛЖ
8.3. Лечение СД при наличии ХСН [1, 2]
Компенсация углеводного обмена при СД и ХСН имеет свои особенности. В последние годы в официальные российские, европейские и американские рекомендации для лечения ХСН, независимо от наличия или отсутствия СД (кроме СД 1 типа), входят ингибиторы SGLT2 дапаглифлозин и эмпаглифлозин в качестве дополнения к базовой терапии. Наиболее эффективны эти препараты у пациентов с СНнФВ.
Ингибиторы SGLT2 канаглифлозин, дапаглифлозин, эмпаглифлозин, эртуглифлозин и сотаглифлозин изучались у пациентов с верифицированными ССЗ или факторами их развития в исследованиях EMPA-REG OUTCOME и VERTIS-CV, а также в CANVAS и DECLARE-TIMI 58. В исследование SCORED включались пациенты с СД2 и риском и наличием ХБП и ССЗ. Во всех исследованиях принимали участие и пациенты с ХСН. Эмпаглифлозин и канаглифлозин достоверно уменьшали композитную конечную точку, включающих смерть от сердечно-сосудистых заболеваний, нефатальный ИМ и нефатальный инсульт, а также госпитализации по поводу ХСН. Наиболее значимые изменения были продемонстрированы в исследовании EMPA-REG OUTCOME. Эмпаглифлозин также уменьшал смертность от всех причин и смерть от сердечно-сосудистых заболеваний (рис. 2, 3, 4).
Рисунок 3. Снижение сердечно-сосудистой смертности, инфаркта миокарда и инсульта без смертельного исхода в исследовании EMPA-REG OUTCOME
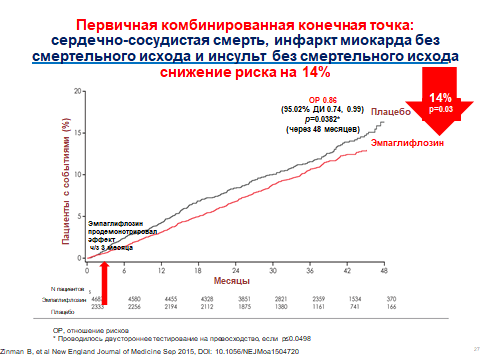
Рисунок 4. Снижение общей смертности в исследовании EMPA-REG OUTCOME
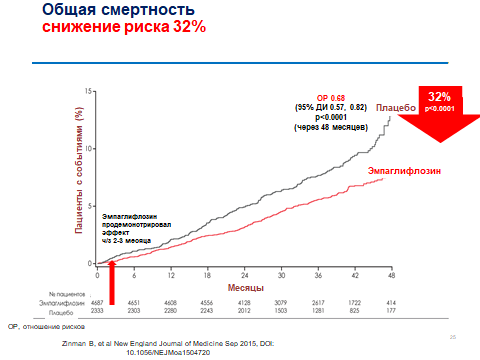
Рисунок 5. Снижение сердечно-сосудистой смертности в исследовании EMPA-REG OUTCOME
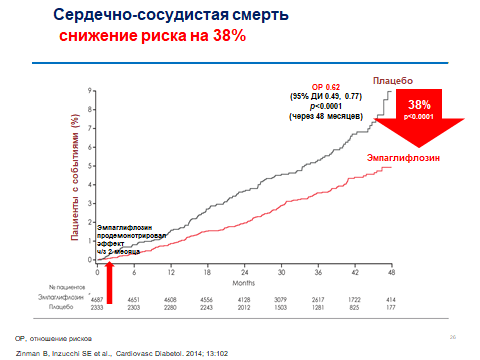
В DECLARE-TIMI 58 дапаглифлазин не увеличивал частоту развития серьезных сердечно-сосудистых событий, входящих в состав комбинированной первичной конечной точки. Но наблюдалось статистически значимое снижение частоты развития событий комбинированной первичной конечной точки, включающей госпитализацию по поводу ХСН и (или) сердечно-сосудистую смерть. В VERTIS-CV наблюдалось статистически значимое снижение госпитализации, связанное с декомпенсацией ХСН. В исследовании SCORED сотаглифлозин снижал смертность от сердечно-сосудистых заболеваний и частоту госпитализаций, связанной с ХСН. В метаанализе этих исследований у пациентов с ХБП (CREDENCE) ингибиторы SGLT2 снижали госпитализацию по поводу декомпенсации сердечной недостаточности на 22 %. Таким образом, имеется класс-эффект молекулы ингибиторов SGLT2 в отношении снижения госпитализации у пациентов с СД2 и ХСН.
На основании результатов этих крупных рандомизированных исследований в настоящее время ингибиторы SGLT канаглифлозин, дапаглифлозин, эмпаглифлозин, эртуглифлозин и сотаглифлозин рекомендуются для предотвращения смерти от ХСН и сердечно-сосудистых заболеваний, а также ухудшения функции почек у пациентов с диабетом 2 типа и ССЗ. Дапаглифлозин и эмпаглифлозин официально рекомендованы для лечения пациентов с СД2 и СНнФВ, а сотаглифлозин, ввиду его способности снижать смертность от сердечно-сосудистых заболеваний и повторную госпитализацию по поводу ХСН, — у пациентов, недавно перенесших госпитализацию по поводу декомпенсации ХСН.
Метформин рассматривается как безопасный препарат у пациентов с ХСН по сравнению с инсулином и препаратами сульфонилмочевины. Однако он не рекомендуется пациентам с СКФ ниже 30 мл/мин/1,73 м2, лицам с печеночной недостаточностью из-за риска развития лактоацидоза. По этой же причине он не применяется у пациентов с острыми формами сердечной недостаточности или прогрессирующей ИБС
У ингибиторов дипептидилпептидазы-4 (DPP-4), согласно рандомизированным клиническим исследованиям, влияние на сердечно-сосудистую смертность или прогрессирование ХСН было нейтральным, но и не приносящим какие-либо преимущества по сердечно-сосудистым исходам. В то же время в исследовании, где пациенты получали саксаглиптин, — на 27 % была увеличена вероятность ухудшения прогноза по ХСН. Поэтому саксаглиптин не рекомендован в качестве сахароснижающего препарата у пациентов с сердечной недостаточностью. На фоне приема видаглиптина наблюдалось увеличение объема ЛЖ и увеличения сердечно-сосудистой заболеваемости и смертности в пилотном исследовании у пациентов с СД2 и ХСН. Поэтому эти препараты не рекомендуются для уменьшения сердечно-сосудистых событий у пациентов с диабетом и сердечной недостаточностью.
Агонисты рецепторов глюкагоноподобного пептида-1 (GLP-1) снижают риск ИМ, инсульта и смерти от сердечно-сосудистых заболеваний у пациентов с СД2 но не влияют на течение ХСН. Поэтому эта группа препаратов, в отличие от ингибиторов SGLT2, не рекомендуются для пациентов, имеющих ХСН.
Инсулин необходим пациентам с СД1 и для контроля гипергликемии у пациентов с СД2, особенно когда функция бета-клеток поджелудочной железы перестает вырабатывать собственный инсулин. Это гормон, удерживающий натрий, поэтому может усиливать задержку жидкости у пациентов с ХСН, таким образом, усугубляя ее течение. Если инсулин необходим пациенту с сердечной недостаточностью, он должен находиться наблюдаться кардиологом, так как имеет высокий риск декомпенсации ХСН. Препараты сульфонилмочевины также не рекомендованы пациентам с ХСН Тиазолидиндионы (глитазоны) вызывают задержку натрия и воды и повышенный риск декомпенсации ХСН. Они противопоказаны пациентам с сердечной недостаточностью.
9. Заключение
Таким образом, комплексный подход к ранней диагностике, лечению и модификации факторов риска ХСН ведет к улучшению прогноза и качества жизни больных СД.
Четкое и последовательное выполнение пациентами рекомендаций врача позволяет значительно замедлить патологический процесс и улучшить качество жизни пациента.
Список литературы
- Хроническая сердечная недостаточность. Клинические рекомендации 2020. Российский кардиологический журнал. 2020; 25 (11): 4083. DOI: 10.15829/1560-4071-2020-4083.
- Алгоритмы специализированной медицинской помощи больным сахарным диабетом. Под редакцией И.И. Дедова, М.В. Шестаковой, А.Ю. Майорова. 10-й выпуск (дополненный). М.; 2021. DOI: 10.14341/DM12802.
- Дедов И.И., Шестакова М.В., Мельниченко Г.А., Мазурина Н.В., Андреева Е.Н., Бондаренко И.З., Гусова З.Р., Дзгоева Ф.Х., Елисеев М.С., Ершова Е.В., Журавлева М.В., Захарчук Т.А., Исаков В.А., Клепикова М.В., Комшилова К.А., Крысанова В.С., Недогода С.В., Новикова А.М., Остроумова О.Д., Переверзев А.П., Роживанов Р.В., Романцова Т.И., Руяткина Л.А., Саласюк А.С., Сасунова А.Н., Сметанина С.А., Стародубова А.В., Суплотова Л.А., Ткачева О.Н., Трошина Е.А., Хамошина М.Б., Чечельницкая С.М., Шестакова Е.А., Шереметьева Е.В. Междисциплинарные клинические рекомендации «Лечение ожирения и коморбидных заболеваний». Ожирение и метаболизм. 2021; 18 (1): 5–99. DOI: 10.14341/omet12714.
- Salvatore Carbone, Justin M Canada tt all Obesity paradox in cardiovascular disease: Where do we stand? May 2019 Vascular Health and Risk Management Volume 15: 89–100. DOI: 10.2147/vhrm.S168946.
- Carbone S, Lavie CJ, Arena R. Obesity and heart failure: Focus on the obesity paradox. Mayo Clin Proc. 2017; 92 (2): 266–279. DOI: 10.1016/j.mayocp.2016.11.00110.
- Pfeffer MA, Swedberg K, McMurray JJ; CHARM Investigators and Сommittees. Prevalence of prediabetes and undiagnosed diabetes in patients with HFpEF and HFrEF and associated clinical outcomes. Cardiovasc Drugs Ther 2017; 31: 545–549.
- Libby P., Okamoto Y., Rocha V.Z., & Folco E. (2010). Inflammation in atherosclerosis: Transition from theory to practice. Circulation journal, 74 (2), 213–220. doi.org/10.1253/circj.cj-09-0706
- V.E. Bianchi. Nutrition in chronic heart failure patients: A systematic review. Heart Fail Rev. 2020 Nov; 25 (6): 1017–1026. DOI: 10.1007/s10741-019-09891-1.
- Кардиоваскулярная профилактика 2022. Российские национальные рекомендации. Российское кардиологическое общество, Национальное общество профилактической кардиологии. https://scardio.ru/content/Guidelines/Kardiovascular_profilaktika_2022.pdf
- C. Chrysohoou, E. Mantzouranis, Y. Dimitroglou, A. Mavroudis, K. Tsioufis. Fluid and Salt Balance and the Role of Nutrition in Heart Failure. Nutrients. 2022 Mar 26; 14 (7): 1386. DOI: 10.3390/nu14071386.
- Kjeldsen EW, Thomassen JQ, Rasmussen KL, Nordestgaard BG, Tybjærg-Hansen A, Frikke-Schmidt R. Impact of diet on ten-year absolute cardiovascular risk in a prospective cohort of 94 321 individuals: A tool for implementation of healthy diets. Lancet Reg Health Eur. 2022; 19: 100419. DOI: 10.1016/j.lanepe.2022.100419.
- L. Long, I.R. Mordi, C. Bridges, V.A. Sagar, E.J. Davies, A.Js. Coats, H. Dalal, K. Rees, S.J. Singh, R.S. Taylor. Exercise-based cardiac rehabilitation for adults with heart failure. Cochrane Database Syst Rev. 2019; 1 (1): CD003331. DOI: 10.1002/14651858.CD003331.pub5.
- Maddatu J, Anderson-Baucum E, Evans-Molina C. Smoking and the risk of type 2 diabetes. Transl Res. 2017 Jun; 184: 101–107. DOI: 10.1016/j.trsl.2017.02.004. Epub 2017 Mar 6.
- Trends Endocrinol Metab. 2012 July; 23 (7): 334–342. DOI: 10.1016/j.tem.2012.03.006. The endocrine effects of nicotine and cigarette smoke.
- Tong X, Chaudhry Z, Lee CC, Bone RN, Kanojia S, Maddatu J, Sohn P, Weaver SA, Robertson MA, Petrache I, Evans-Molina C, Kono T. Cigarette smoke exposure impairs β-cell function through activation of oxidative stress and ceramide accumulation. Mol Metab. 2020 Jul; 37: 100975. DOI: 10.1016/j.molmet.2020.100975. Epub 2020 Mar 13.
- Cigarette smoking is an independent risk factor for type 2 diabetes: A four-year community-based prospective study. Nam H. Cho,Juliana C. N. Chan, Hak Chul Jang, Soo Lim, Hyung L. Kim, Sung Hee Choi. 05 October 2009, Clinical Endocrinology.
- Wittel UA, Hopt UT, Batra SK. Cigarette smoke-induced pancreatic damage: experimental data. Langenbecks Arch Surg. 2008 Jul; 393 (4): 581–8. DOI: 10.1007/s00423-007-0273-3. Epub 2008 Jan 12.
- Śliwińska-Mossoń M, Milnerowicz S, Milnerowicz H. Diabetes mellitus secondary to pancreatic diseases (type 3c): The effect of smoking on the exocrine-endocrine interactions of the pancreas. Diab Vasc Dis Res. 2018 May; 15 (3): 243–259. DOI: 10.1177/1479164118764062. Epub 2018 Mar 21. PMID: 29558826.
- Topsakal S, Ozmen O, Aslankoc R, Aydemir DH. Pancreatic damage induced by cigarette smoke: the specific pathological effects of cigarette smoke in the rat model. Toxicol Res (Camb). 2016 Mar 17; 5 (3): 938–945. DOI: 10.1039/c5tx00496a. PMID: 30090402; PMCID: PMC6062390.
- Hieshima K, Suzuki T, Sugiyama S, Kurinami N, Yoshida A, Miyamoto F, Kajiwara K, Jinnouchi T, Jinnouchi H. Smoking Cessation Ameliorates Microalbuminuria with Reduction of Blood Pressure and Pulse Rate in Patients with Already Diagnosed Diabetes Mellitus. J Clin Med Res. 2018 Jun; 10 (6): 478–485. DOI: 10.14740/jocmr3400w. Epub 2018 Apr 13.
- Tobacco and diabetes: Clinical relevance and approach to smoking cessation in diabetic smokers, Marco López Zubizarreta, Endocrinología, Diabetes y Nutrición, Vol. 64. Issue 4.pages 221–231 (April 2017).
- Chen HJ, Huang WH, Chan HL, Hwang LC. Improvement in Cardiometabolic Risk Factors During Smoking Cessation Treatment in Patients with Type 2 Diabetes: A Retrospective Cohort Study. Diabetes Metab Syndr Obes. 2021 Apr 16; 14: 1695–1702. DOI: 10.2147/dmso.S303446. PMID: 33889004; PMCID: PMC8057786.
- Hasegawa K, Komiyama M, Takahashi Y. Obesity and Cardiovascular Risk After Quitting Smoking: The Latest Evidence. Eur Cardiol. 2019 Apr; 14 (1): 60–61. DOI: 10.15420/ecr.2019.4.2. PMID: 31131038; PMCID: PMC6523057.
- Flores L, Vidal M, Abian J, Cases A, Campistol JM, Clària J, Lario S, Esmatjes E. The effects of smoking and its cessation on 8-epi-PGF2alpha and transforming growth factor-beta 1 in Type 1 diabetes mellitus. Diabet Med. 2004 Mar; 21 (3): 285–9. DOI: 10.1111/j.1464-5491.2004.01133.x. PMID: 15008841.
- Hu Y, Zong G, Liu G, Wang M, Rosner B, Pan A, Willett WC, Manson JE, Hu FB, Sun Q. Smoking Cessation, Weight Change, Type 2 Diabetes, and Mortality. N Engl J Med. 2018 Aug 16; 379 (7): 623–632.
- Campagna, D., Alamo, A., Di Pino, A. et al. Smoking and diabetes: Dangerous liaisons and confusing relationships. Diabetol Metab Syndr 11, 85 (2019).
- Boakye D, Wyse CA, Morales-Celis CA, Biello SM, Bailey MES, Dare S, Ward J, Gill JMR, Pell JP, Mackay DF. Воздействие табака и нарушение сна у 498 208 участников биобанка Великобритании. J Общественное здравоохранение (Oxf). 2018 Сен 1; 40 (3): 517–526. DOI: 10.1093/pubmed/fdx102. PMID: 29040744; PMCID: PMC6166587.
- Амири С., Бехнежад С. Курение и риск возникновения проблем, связанных со сном: систематический обзор и метаанализ проспективных исследований. Общественное здравоохранение. 2020 Окт; 111 (5): 775–786. DOI: 10.17269/s41997-020-00308-3. Epub 2020 Мар 17. PMID: 32185746; PMCID: PMC7501367.
- Hahad O, Beutel M, Gilan DA, Michal M, Schulz A, Pfeiffer N, König J, Lackner K, Wild P, Daiber A, Münzel T. Связь курения и отказа от курения с распространенными и инцидентными симптомами депрессии, тревоги и нарушения сна среди населения в целом. J Аффект Дизорд. 2022 Сен 15; 313: 100–109. DOI: 10.1016/j.jad.2022.06.083. Epub 2022 28 июня. PMID: 35777492.
- Ioannidou D, Kalamaras G, Kotoulas SC, Pataka A. Курение и обструктивное апноэ сна: существует ли связь между этими кардиометаболическими факторами риска? Гендерный анализ. Медицина (Каунас). 2021 Окт 20; 57 (11): 1137. DOI: 10.3390/medicina57111137. PMID: 34833356; PMCID: PMC8621446.
- Alicia Nuñez PhD, Joshua Unbin Rhee, Patricia Haynes, Subhajit Chakravorty, Freda Patterson, William D.S. Killgore, Rebecca A. Gallagher, Lauren Hale, Charles Branas, Nancy Carrazco, Pamela Alfonso-Miller, Jo-Ann Gehrels, Michael A. Grandner, Smoke at night and sleep worse? The associations between cigarette smoking with insomnia severity and sleep duration, Sleep Health, Volume 7, Issue 2, 2021, Pages 177–182.
- McGrath, T.E., Wooten, J.B., Chan W.G. and Hajaligol, M.R., 2007, Formation of polycyclic Aromatic Hydrocarbons from Tobacco: the ‘Link’ between Low Temperature Residual Solid and PAH Formation, Food and Chemical Toxicology, 45, 6, 1039–1050.
- Benowitz NL, Fitzgerald GA, Wilson M, Zhang Q. Nicotine effects on eicosanoid formation and hemostatic function: comparison of transdermal nicotine and cigarette smoking. J Am Coll Cardiol. 1993 Oct; 22 (4): 1159–67. DOI: 10.1016/0735-1097 (93)90431-y. PMID: 7691912.
- Barua RS et al. ACC Expert Consensus Decision Pathway on Tobacco Cessation Treatment A Report of the American College of Cardiology Task Force on Clinical Expert Consensus Documents. Journal of the American College of Cardiology. 2018; 72 (25).
- Jean-Pierre Schaller, Daniela Keller, Laurent Poget Pacitto, et al. Evaluation of the Tobacco Heating System 2.2. Part 2: Chemical composition, genotoxicity, cytotoxicity, and physical properties of the aerosol Regulatory Toxicology and Pharmacology 81 (2016). S27eS47. DOI: 10.1016/j.yrtph.2016.10.001.
- Kiyohara K.; Tabuchi T. Electronic cigarette use in restaurants and workplaces where combustible tobacco smoking is not allowed: An Internet survey in Japan. Tob Control. 2018 May; 27 (3): 254–257. DOI: 10.1136/tobaccocontrol-2016-053581.
- Lüdicke F., Picavet P., Baker G., Haziza C., Poux V., Lama N., Weitkunat R. Effects of switching to the menthol tobacco heating system 2.2, smoking abstinence, or continued cigarette smoking on clinically relevant risk markers: A randomized, controlled, open-label, multicenter study in sequential confinement and ambulatory settings (Part 2). Nicotine Tob. Res. 2018, 20, 173–182. DOI: 10.1093/ntr/ntx028.
- Haziza C., de La Bourdonnaye G., Donelli A. et al. Favorable Changes in Biomarkers of Potential Harm to Reduce the Adverse Health Effects of Smoking in Smokers Switching to the Menthol Tobacco Heating System 2.2 for 3 Months (Part 2). Nicotine Tob. Res. 2020, 22, 549–559. DOI: 10.1093/ntr/ntz084.
- Choi S, Lee K, Park SM. Combined Associations of Changes in Noncombustible Nicotine or Tobacco Product and Combustible Cigarette Use Habits with Subsequent Short-Term Cardiovascular Disease Risk Among South Korean Men: A Nationwide Cohort Study. Circulation. 2021 Nov 9; 144 (19): 1528–1538. DOI: 10.1161/circulationaha.121.054967.
- Aguilar MC, Gurpegui M, Diaz FJ, de Leon J. Nicotine dependence and symptoms in schizophrenia: naturalistic study of complex interactions. Br J Psychiatry. 2005 Mar; 186: 215–21.
- Güngen AC, Tekeşin A, Koç AS, Güngen BD, Tunç A, Yıldırım A, Ceyran Ö, Memiş I. The effects of cognitive and emotional status on smoking cessation. Eur Rev Med Pharmacol Sci. 2022 Jul; 26 (14): 5092–5097. DOI: 10.26355/eurrev_202207_29295. PMID: 35916805.
- Taylor DH Jr, Hasselblad V, Henley SJ, Thun MJ, Sloan FA. Преимущества отказа от курения для долголетия. Am J Общественное здравоохранение. 2002 Июн; 92 (6): 990–6. DOI: 10.2105/ajph.92.6.990. Erratum in: Am J Public Health 2002 Sep; 92 (9): 1389. PMID: 12036794; PMCID: PMC1447499.


















