Статьи
Новые возможности лечения больных неметастатическим кастрационно- резистентным раком предстательной железы
С 21 по 27 июня 2021 года в Санкт-Петербурге уже в седьмой раз прошел международный онкологический форум «Белые ночи» — одно из крупнейших ежегодных мероприятий в области онкологии, объединяющее широкий круг специалистов из России, ближнего и дальнего зарубежья. На протяжении недели онкологи и смежные специалисты делились знаниями и обсуждали актуальные вопросы, в том числе касающиеся появления новых высокоэффективных препаратов. Одному из них был посвящен симпозиум компании Bayer, которая в этом году выводит на рынок препарат даролутамид, предназначенный для лечения больных неметастатическим кастрационно-резистентным раком предстательной железы.
ПЕРЕЛОМНЫЙ МОМЕНТ
На мероприятиях онкофорума «Белые ночи — 2021» не раз говорилось о том, что буквально на наших глазах происходит переломный момент в лечении онкологических заболеваний. Это связано с созданием новых высокоэффективных препаратов, позволяющих не только повышать показатели выживаемости, но и сохранять высокое качество жизни онкобольных. Данная тема подробно обсуждалась на симпозиуме, посвященном современным возможностям лечения пациентов с неметастатическим кастрационно-резистентным раком предстательной железы (нмКРРПЖ). С докладами на этом мероприя5П5л4ацеботии выступили:
- Борис Яковлевич Алексеев - д. м. н., профессор, онколог-уролог, ученый секретарь РООУ, заместитель генерального директора по научной работе ФГБУ «НМИЦ радиологии» Минздрава РФ;
- Всеволод Борисович Матвеев - д. м. н., профессор, член-корреспондент РАН, президент Российского общества онкоурологов;
- Мария Игоревна Волкова - д. м. н., ведущий научный сотрудник отделения урологии ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава РФ, ученый секретарь московского регионального отделения Российского общества онкоурологов.
В БОРЬБЕ ЗА КАЧЕСТВО ЖИЗНИ
В. Б. Матвеев напомнил, насколько важно для больных нмКРРПЖ сохранение качества жизни и привычных видов деятельности на фоне проводимого медикаментозного лечения. Большинство таких пациентов имеют минимальный набор симптомов со стороны РПЖ, активны в семье и социуме, продолжают работать, но при этом нередко отягощены профилем коморбидности в виде сахарного диабета и артериальной гипертензии, а значит, вынуждены принимать препараты еще и по поводу данных заболеваний. Что касается непосредственно нмКРРПЖ, то для больных имеют значение не только показатели общей выживаемости, но и время до развития биохимического прогрессирования — в первую очередь уровень простатического специфического антигена (ПСА) и время его удвоения.
О риске прогрессирования рака предстательной железы с вероятностью появления отдаленных метастазов принято судить по времени удвоения ПСА (ВУПСА) — наихудший прогноз имеют пациенты с показателем ВУПСА 8–10 месяцев. После перехода нмКРРПЖ в мКРРПЖ риск смерти от любых причин увеличивается с 16 % до 56 %, а при появлении костных метастазов 5-летняя выживаемость сокращается до 3 %. Раннее применение антиандрогенов нового поколения у пациентов с нмКРРПЖ при регистрации ВУПСА на сроке менее 10 месяцев позволяет значимо увеличить время до прогрессирования РПЖ, поэтому назначение данных препаратов в комбинации с андрогенной депривацией у больных данной категории прописано в клинических рекомендациях Ассоциации онкологов по лечению пациентов с РПЖ от 2020 года.
Препараты этой группы позволяют сохранить привычное качество жизни и не вступают в конфликт с текущей терапией сопутствующих заболеваний. Даролутамид также включен в ведущие международные клинические рекомендации как один из препаратов для лечения пациентов с нмКРРПЖ при ВУПСА <10 мес. После получения результатов международного рандомизированного двойного слепого плацебо-контролируемого исследования III фазы ARAMIS в феврале 2021 года даролутамид был зарегистрирован на территории РФ и сейчас уже доступен российским пациентам.
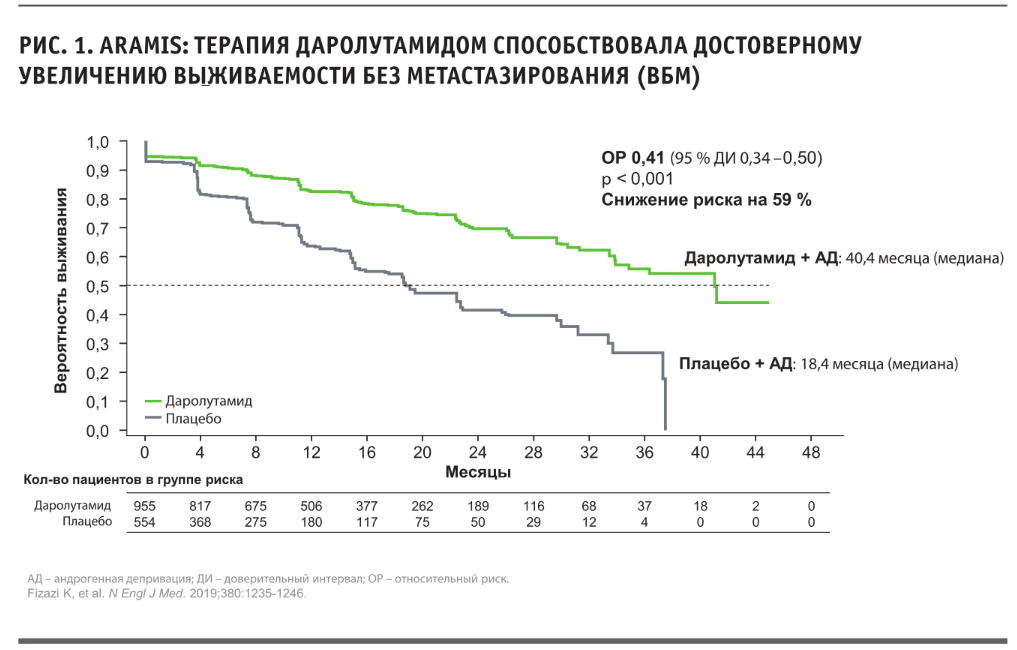
БЕЗ РИСКА ПРОГРЕССИРОВАНИЯ
Результаты регистрационного исследования ARAMIS, которое проходило в том числе и в РФ (в нем приняли участие 105 пациентов в 19 клинических центрах), более подробно представил Б. Я. Алексеев.
Он отметил, что согласно критериям включения к участию допускались с нмКРРПЖ и ВУПСА <10 мес (у большинства — менее 6 мес), то есть с крайне высоким риском появления метастазов, не получавшие ранее химио- или иммунотерапию. В группе лечения дозировка даролутамида составляла 600 мг 2 раза в день. Все участники постоянно получали андроген-депривационную терапию. Применение даролутамида приводило к статистически достоверному и клинически значимому снижению риска прогрессирования: медиана выживаемости без появления отдаленных метастазов (медиана выживаемости без метастазирования, ВБМ) в группе даролутамида составила 40,4 мес, в то время как в группе андроген-депривационной монотерапии — всего 18,4 мес.
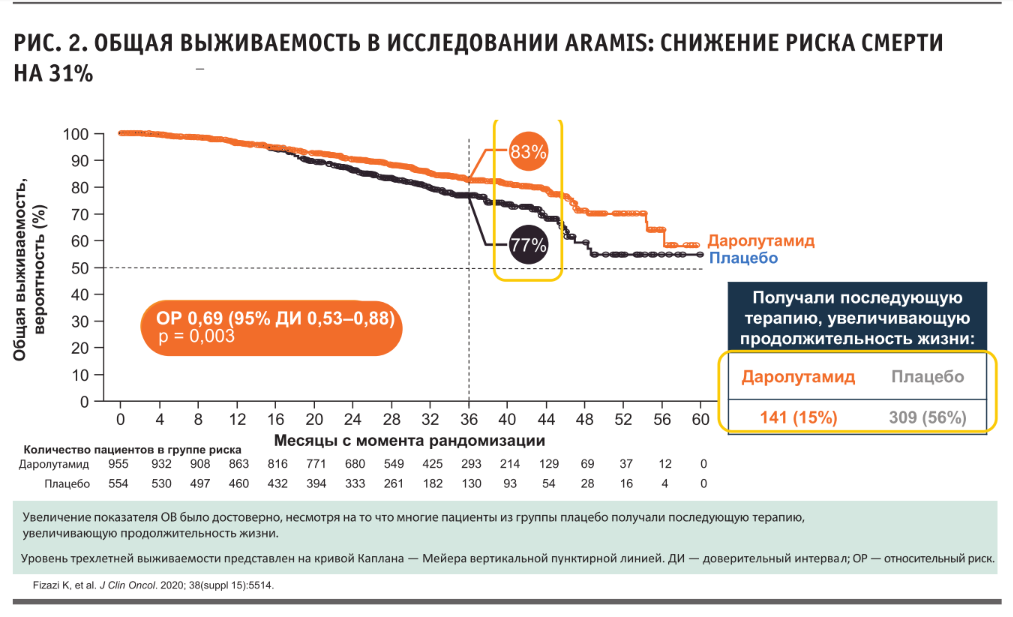
Назначение даролутамида позволило не только снизить вероятность отдаленного метастазирования или смерти на 59 %, но и увеличить продолжительность жизни, уменьшив риск смерти на 31 %, согласно анализу показателя общей выживаемости. Препарат продемонстрировал высокую эффективность вне зависимости от возраста пациентов, исходного уровня ПСА, степени дифференцировки опухоли и прочих факторов. Разница в продолжительности жизни в группах была достоверной, даже несмотря на кроссовер — назначение даролутамида и других препаратов, увеличивающих продолжительность жизни, 55 % участников из группы плацебо при появлении признаков прогрессирования.
Даролутамид также зарекомендовал себя как препарат, сохраняющий качество жизни пациентов. Его раннее назначение на стадии нмКРРПЖ позволило в 2 раза увеличить время до прогрессирования болевого синдрома и, соответственно, возникновения потребности в опиоидных анальгетиках, отсрочить начало агрессивной и часто плохо переносимой цитотоксической химиотерапии, продлить период до появления костных метастазов, которые могут приводить к инвалидизации, уменьшить на 67 % вероятность последующего назначения противоопухолевой терапии.
НЕЖЕЛАТЕЛЬНЫЕ ЯВЛЕНИЯ
Доклад М. И. Волковой был посвящен анализу переносимости даролутамида в исследовании ARAMIS. В начале выступления спикер отметила, что даролутамид является чистым ингибитором андрогенных рецепторов без влияния на системные стероиды и функцию костного мозга, что нашло отражение в благоприятном профиле безопасности препарата. Как известно, ингибиторам андрогенов 2-го поколения свойственна неврологическая токсичность, которая связана с их способностью проникать через гематоэнцефалический барьер (ГЭБ) в силу малых размеров. Например, большая часть нежелательных явлений при применении энзалутамида и апалутамида выражалась следующими признаками неврологической токсичности: усталостью, головокружением, падениями и т. д.
По химической структуре даролутамид тоже представляет собой малую молекулу. Однако по сравнению с молекулами энзалутамида и апалутамида, обладающими ригидным ядром, молекула даролутамида отличается повышенной гибкостью, более высокой полярностью и большим потенциалом образования водородных связей, что обусловливает Увеличение показателя ОВ было достоверно, несмотря на то что многие пациенты из группы плацебо получали последующую терапию, более низкую способность препарата проникать через ГЭБ.
В доклинических исследованиях концентрация даролутамида в головном мозге через 8 часов после экспозиции была в 50 раз ниже, чем у энзалутамида, и в 30 раз ниже, чем у апалутамида. Мария Игоревна подчеркнула, что благодаря эффективности препарата длительность лечения даролутамидом оказывается гораздо выше, чем плацебо, поэтому частота нежелательных явлений (НЯ) в протоколе ARAMIS рассчитывалась с поправкой на экспозицию.
Нежелательные реакции 3 и 4-й степеней тяжести и случаи отмены препарата из-за НЯ были представлены в группах даролутамида и плацебо с равной частотой. При анализе структуры неврологической токсичности оказалось, что такие реакции, как усталость и астения, обмороки, ухудшение памяти и другие когнитивные нарушения регистрировались в группе даролутамида и плацебо с одинаковой частотой. То же самое относилось и к регистрации гипертензии, артралгии, диареи, судорог и т. д.
ПРОФИЛЬ БЕЗОПАСНОСТИ
М. И. Волкова обратила внимание на сравнение профилей безопасности трех антиандрогенов 2-го поколения: даролутамида, энзалутамида и апалутамида. Сетевой метаанализ исследований ARAMIS, PROSPER и SPARTAN показал отсутствие разницы относительного риска НЯ и нежелательных реакций 3 и 4-й степеней тяжести антиандрогенов 2-го поколения и плацебо. Однако при анализе отдельных НЯ обнаружилось, что энзалутамид и апалутамид чаще, чем даролутамид, вызывали развитие усталости, а апалутамид чаще двух других препаратов данной группы вызывал развитие артериальной гипертензии и сыпи. Кстати, в отношении артериальной гипертензии, в том числе выраженной, даролутамид проявил себя как наиболее безопасный препарат из трех ингибиторов андрогенов 2-го поколения.
Отдельно М. И. Волкова упомянула, что в протоколе ARAMIS даролутамид значимо повышал качество жизни пациентов, уменьшая уровень боли и выраженность мочевых симптомов. В качестве особого преимущества даролутамида спикер назвала его хорошую совместимость с основными препаратами, которые назначаются для лечения сопутствующих заболеваний.
В силу возрастных особенностей больные нмКРРПЖ имеют отягощенный коморбидный фон и принимают не менее одного препарата по поводу сопутствующих патологий: гипотензивные средства, антикоагулянты и антиагреганты, статины, антиаритмики, противовоспалительные, обезболивающие препараты и т. д. Лекарственные взаимодействия реализуются посредством конкурентных взаимовлияний с транспортными белками и системой цитохромов. Исходя из этого, ингибиторы андрогенов 2-го поколения энзалутамид и апалутамид не рекомендуется назначать с достаточно широким спектром препаратов, среди которых антиаритмики, гипотензивные средства, антибиотики, ингибиторы протонной помпы, антитромботические средства, антипсихотики и многие другие.
В отличие от «одноклассников» даролутамид обладает более благоприятным профилем лекарственных взаимодействий: его нежелательно назначать лишь с кларитромицином, рифампицином, розувастатином и карбамазепином. В рамках исследования ARAMIS частоты необходимости модификации терапии сопутствующих заболеваний в группах даролутамида и плацебо были сопоставимы. При дополнительном анализе пациентов, получавших статины, различий по частоте межлекарственных взаимодействий в группах даролутамида и плацебо обнаружено не было.
Сегодня даролутамид изучается для терапии пациентов с метастатическими, но при этом гормонально чувствительными формами заболевания. Первичный анализ данных исследования III фазы ARASENS (эффективность и безопасность препарата у пациентов с метастатическим гормонально чувствительным раком предстательной железы) ожидается в конце 2021 года.
Ольга Безрукова, к.м.н.
Читайте также
- Мы снова всех опередили, но вот в чем?
- Комбинированная иммунотерапия метастатического рака почки
- Хавьер Кортес: о новых трендах и лечении рака молочной железы в Испании
- Московский онкологический форум — знаковое событие столичного здравоохранения
- «Мы здесь не из-за денег». Медицина в XXI веке: бизнес или предназначение?
- Генетическая панель РАМ-100 — новая идеология в молекулярной диагностике рака молочной железы
- Первичная профилактика фебрильной нейтропении при химиотерапевтическом лечении
- Эффективность моноклонального антитела пролголимаб при терапии метастатической меланомы: клиническое исследование MIRACULUM

















