Статьи
Острый бронхиолит: между бронхитом и пневмонией
Острый бронхиолит (ОБ) — это самолимитирующееся воспалительное заболевание бронхиол у детей первых двух лет жизни (чаще всего первых 6 месяцев) с развитием бронхиальной обструкции. Клинически диагностируется по свистящему дыханию, а при аускультации легких — по рассеянным свистящим хрипам или диффузной крепитации.
ОБЩИЕ ДАННЫЕ
Диагноз «острый бронхиолит» применяется в отношении первого эпизода острого вирус-индуцированного бронхообструктивного синдрома (БОС). Это наиболее частое инфекционное заболевание нижних дыхательных путей (НДП) у детей грудного возраста. По отечественным данным, заболеваемость ОБ составляет 114–137 случаев на тысячу детей. Часто вместо ОБ ребенку устанавливают некорректный диагноз «двусторонняя пневмония с БОС». Максимум заболеваемости отмечается в возрасте от 2 до 8 месяцев жизни.
ОБ обычно вызывают респираторные вирусы, чаще всего респираторно-синцитиальный вирус (РСВ), выявляемый у 75 % больных, а также рино- и аденовирусы, вирусы парагриппа и гриппа, метапневмовирусы человека, коронаи бокавирусы, Bordetella pertussis. Заражение происходит преимущественно воздушно-капельным и контактным путями, возможны нозокомиальные вспышки. Постинфекционный иммунитет в отношении РСВ нестоек, что приводит к частому реинфицированию. Не менее четверти случаев ОБ обусловлено микст-инфекцией, что утяжеляет течение заболевания.
У детей грудного возраста ОБ — самая частая форма бронхита, что связано с меньшим диаметром и богатой васкуляризацией слизистой оболочки бронхов. Дихотомически ветвясь, конечные бронхиолы появляются начиная с 6–16-й генерации бронхиального дерева. Даже у взрослых их диаметр составляет менее 1 мм, а в стенке отсутствуют хрящ и слизистые железы.
Морфологические изменения при ОБ характеризуются некрозом эпителия бронхов, гиперсекрецией и сгущением слизи, нейтрофильной инфильтрацией, образованием слизистых пробок. Даже незначительное утолщение стенки бронхиол снижает воздушный поток, поскольку сопротивление дыхательных путей обратно пропорционально четвертой степени ее радиуса. Нарушение вентиляционно-перфузионных отношений способствует быстрому развитию гипоксемии, при тяжелом течении — гиперкапнии.
ФАКТОРЫ РИСКА
Факторы риска развития ОБ и его тяжелого течения с необходимостью госпитализации, в том числе в отделение реанимации и интенсивной терапии (ОРИТ):
- мужской пол;
- недоношенность и малая масса тела при рождении (менее 2500 г);
- возраст менее 3–6 месяцев и масса тела менее 5 кг (ОБ протекает тем тяжелее, чем меньше гестационный, постконцептуальный и календарный возраст недоношенного ребенка);
- врожденная пневмония, синдром аспирации мекония и искусственная вентиляция легких (ИВЛ) в неонатальном периоде;
- низкий социально-экономический уровень жизни и недостаточная образованность ухаживающих за ребенком, стесненные условия проживания, пассивное курение;
- наличие в семье старших братьев и сестер;
- бронхолегочная дисплазия (БЛД), муковисцидоз, врожденные пороки сердца (ВПС) и дыхательных путей, синдром Дауна, нервно-мышечные заболевания, иммунодефициты.
КЛИНИЧЕСКАЯ КАРТИНА
Заболевание, как правило, развивается на 3–5-й день от начала острой инфекции верхних дыхательных путей. Клиническая картина ОБ складывается из нереспираторных и респираторных симптомов.
Нереспираторная симптоматика включает в себя недлительное повышение температуры до субфебрильных цифр, хотя бронхиолиты адено- и энтеровирусной этиологии сопровождаются фебрилитетом. У ребенка отмечаются раздражительность, сонливость, отказ от еды. Возможно развитие катарального отита, появление тахикардии, так называемой ложной гепатомегалии из-за смещения печени эмфизематозно вздутыми легкими.
Респираторные симптомы предполагают внезапно появляющееся свистящее дыхание, экспираторную или смешанную одышку, насморк, спастический кашель, тахипноэ — в тяжелых случаях частота дыхательных движений (ЧДД) достигает 90 в минуту, цианоз и апноэ. Над легкими определяется коробочный оттенок звука, при аускультации выслушиваются крепитация как результат слипания и разлипания стенок бронхиол, рассеянные влажные мелкопузырчатые и сухие свистящие хрипы, в тяжелых случаях—диффузное ослабление дыхания. Максимальной выраженности БОС достигает на 3–4-е сутки заболевания, может сопровождаться развитием преходящей кислородозависимости. Наиболее подвержены апноэ недоношенные, у которых этот симптом встречается с частотой 25–40 %.
Диагноз «ОБ» — клинический, его критерии: возраст до двух лет, субфебрильная или нормальная температура, апноэ, ринит (назофарингит), сухой кашель, свистящее дыхание, снижение толерантности к энтеральному питанию, тахипноэ, одышка, вздутие грудной клетки, коробочный перкуторный звук, диффузная крепитация, свистящие, влажные мелкопузырчатые диффузные хрипы. Всем детям с ОБ показано проведение пульсоксиметрии. Маркерами дыхательной недостаточности (ДН) II и III степени, при которой требуется назначение кислородотерапии и ИВЛ, служат показатели SpO2 ниже 90 % и 75 % соответственно.
В типичных случаях для подтверждения диагноза ОБ не требуется лабораторных или инструментальных исследований, их использование может приводить к полипрагмазии, удлинению госпитализации. Необходимость в дополнительных исследованиях возникает, если симптомы ОБ сопровождаются лихорадкой; отсутствуют катаральные явления в носоглотке; у ребенка тяжелое общее состояние. Данные гемограммы при ОБ характеризуются лейко- и нейтропенией, лимфоцитозом. Посевы крови, мочи, определение С-реактивного белка и/или прокальцитонина, рентгенография грудной клетки, люмбальная пункция проводятся при сочетании высокой лихорадки с падением SpO2 ниже 92 % и апноэ. В других случаях вероятность бактериемии, бактериальной инфекции у детей с ОБ крайне низка. Исключение составляют эпизоды внутрибольничной РСВ-инфекции, развитие ОБ у детей с цианотическими ВПС или другими заболеваниями, требующими терапии в ОРИТ. Определение газового состава крови целесообразно при тяжелом течении заболевания (ДН II–III степени, цианоз, апноэ).
Этиологическая расшифровка заболевания проводится для предотвращения дальнейшего распространения вируса путем изоляции больных. Она также позволяет избежать необоснованного применения антибиотиков, может иметь предсказательное значение в отношении риска развития в последующем бронхиальной астмы (БА), которая возникает после ОБ риновирусной или РСВ-этиологии. Выявление респираторных вирусов, особенно риновируса, при повторных эпизодах БОС либо при БОС у детей старше 1–2 лет жизни—веское основание заподозрить БА.
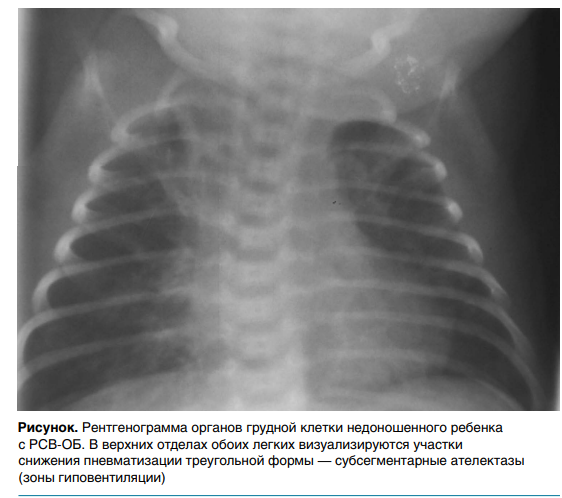
К возможным показаниям для рентгенологического исследования органов грудной клетки (РГ ОГК) при ОБ относятся симптомы, подозрительные на пневмонию (лихорадка выше 38 о С более 3 дней, инфекционный токсикоз, локальные физикальные данные), и ухудшение состояния на фоне лечения. На рентгенограммах у 20–30 % больных ОБ могут определяться участки гиповентиляции и (или) ателектазы, которые симулируют пневмонию и характеризуются самопроизвольным расправлением (рис.). Ателектазы могут сохраняться в течение 9–15 дней, пока не восстановится бронхиолярный эпителий. Показанием к проведению компьютерной томографии (КТ) может быть подозрение на развитие облитерирующего бронхиолита, подумать о нем необходимо при сохранении одышки через 4–6 недель от начала ОБ.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ
- Апноэ или цианоз;
- ДН (SpO2 < 92 % при дыхании воздухом, ЧДД выше 60 в минуту, втяжение грудной клетки, кряхтящее дыхание, раздувание крыльев носа);
- Дегидратация, затруднение кормления (снижение потребления жидкости до 50–75 % от обычного объема или отсутствие мочеиспусканий в течение 12 часов);
- Общее тяжелое состояние (симптомы выраженной интоксикации, ребенок не реагирует на обычные стимулы, просыпается только после длительной стимуляции);
- Кислородозависимые пациенты на дому, например с БЛД;
- Неэффективность терапии в домашних условиях или невозможность ее проведения (по социальным показаниям);
- Тяжелые сопутствующие заболевания.
ПОДХОДЫ К ТЕРАПИИ
У многих детей с ОБ имеется легкое или умеренное обезвоживание в результате тахипноэ и анорексии, поэтому им рекомендуется осторожно вводить жидкость, количество которой больше физиологической потребности. Если сосание затруднено из-за одышки, а также в связи с риском аспирации, оправданно введение жидкости через зонд или парентерально. Парентеральная регидратация проводится глюкозо-солевыми растворами в объеме не более 20 мл/кг/сут, учитывая риск развития отека легких и синдрома неадекватной секреции антидиуретического гормона. Больной ребенок чувствует себя наиболее комфортно в положении полулежа (при этом головной конец кровати приподнимают на 10–30о ) со слегка запрокинутой назад головой.
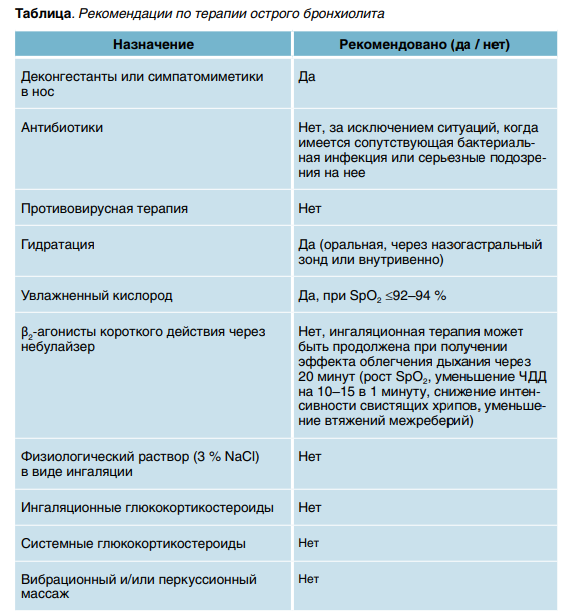
Базисная терапия ОБ заключается в обеспечении достаточной оксигенации пациента. Оксигенотерапия проводится при показателях SpO2 ниже 92–94 %. В зависимости от степени тяжести течения ОБ назначают непрерывную кислородотерапию через назальные канюли, высокопоточную оксигенацию, CPAP-терапию или ИВЛ. Основные подходы к лечению ОБ с позиций доказательной медицины, представленные в клинических рекомендациях Минздрава России (2021), приведены в таблице.
Ингаляционные бронхолитики используют через небулайзер 3–4 раза в день, предпочтение отдают комплексному препарату фенотерол + ипратропия бромид (назначается в дозе одна капля/кг на ингаляцию). При ОБ противопоказаны пероральные β2-агонисты, антигистаминные и антилейкотриеновые препараты, муколитики и диуретики.
МЕТОДЫ ПРОФИЛАКТИКИ
Профилактика ОБ включает грудное вскармливание на протяжении не менее 6 месяцев. Снизить частоту ОБ может вскармливание смесью, обогащенной пятью олигосахаридами грудного молока. Лучшие способы профилактики внутрибольничной РСВ-инфекции — ношение масок и дезинфекция рук.
Препаратом для пассивной иммунопрофилактики у детей из групп риска является паливизумаб, представляющий собой моноклональные антитела к F-протеину РСВ. Паливизумаб показан недоношенным в возрасте до 6 месяцев, рожденным на 35-й неделе беременности или ранее; детям до двух лет, которым потребовалось лечение по поводу БЛД в течение последних 6 месяцев; малышам до 2 лет с гемодинамически значимыми ВПС. Возможно его назначение детям не старше 2 лет из других групп риска тяжелого течения РСВ-инфекции.
Паливизумаб вводится внутримышечно ежемесячно из расчета 15 мг/кг с интервалом 30 ± 5 дней в течение 5 месяцев независимо от сезона. Желательно, чтобы первая инъекция была проведена за 3–5 дней до выписки из стационара.



















