Статьи
Принципы ведения неврологических пациентов в период пандемии COVID‑19
30.06.2020
Цель данного обзора — осветить существующие данные о рисках инфицирования SARS-CoV-2 среди пациентов
с отдельными неврологическими заболеваниями и особенности ведения их в условиях пандемии.
РАССЕЯННЫЙ СКЛЕРОЗ И ДРУГИЕ АУТОИМУННЫЕ БОЛЕЗНИ ЦНС
Пациенты с рассеянным склерозом (РС) не имеют повышенного риска заражения новым коронавирусом вне зависимости от того, находятся ли они в фазе ремиссии или обострения. Увеличить риск могут проблемы с дыханием и / или глотанием вследствие значимой инвалидизации, а также проведение селективной иммунотерапии (ИТ).
При наличии острой или подострой неврологической симптоматики, особенно на фоне повышения температуры тела, необходимо исключить инфекционное поражение нервной системы (энцефалит, менингит, менингоэнцефалит, острый рассеянный энцефаломиелит, прогрессирующая мультифокальная лейкоэнцефалопатия (ЛЭП)). Для этого пациента переводят в инфекционный стационар. Необходимо четко дифференцировать признаки обострения существующего заболевания и неврологические проявления коронавирусной инфекции (КВИ) для правильного оказания медицинской помощи. Магнитно-резонансная томография (МРТ) головного и спинного мозга, в том числе с контрастным усилением, выполняется в плановом порядке.
Подход к назначению препаратов, изменяющих течение рассеянного склероза (ПИТРС), должен быть индивидуальным — чем выше клиническая эффективность медикамента, тем более персонализированно и осторожно следует рассматривать возможность его использования.
Применение ПИТРС в условиях COVID‑19
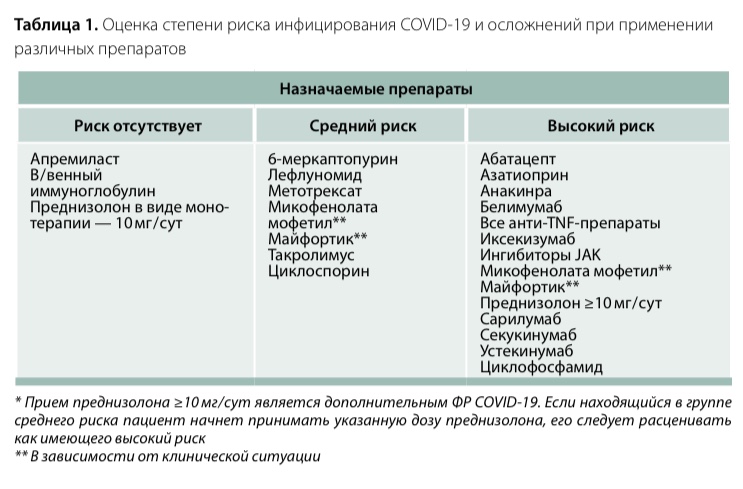
Безопасность применения того или иного лекарственного средства (ЛС) определяется для каждого случая отдельно (табл. 1). Продолжение или начало лечения препаратами интерферонов β‑1а и -1b, глатирамера ацетата считается безопасным. Терапия такими таблетированными ЛС, как терифлуномид, диметилфумарат, финголимод, может привести к лейко- и лимфопении, поэтому их назначение требует контроля общего анализа крови не реже 1 раза в 3 мес. для оценки иммунного ответа.
К препаратам 2-й линии, рекомендованным в условиях пандемии COVID‑19, относится натализумаб, однако необходимо учитывать возможность развития прогрессирующей мультифокальной ЛЭП на фоне его приема. Для профилактики нежелательных явлений и безопасности пациента интервал между инфузиями может быть увеличен. У получающих финголимод или натализумаб в период 2–4 мес. После отмены может произойти «ребаунд-эффект».
Применение таких средств, как окрелизумаб, алемтузумаб, кладрибин, а также выполнение трансплантации гемопоэтических стволовых клеток по возможности следует отложить.
Иммуносупрессия при заболеваниях спектра оптикомиелита на фоне COVID‑19
Несмотря на то что риск инфицирования SARS‑CoV‑2 при терапии азатиоприном, микофенолата мофетилом, метотрексатом возрастает, рекомендуется придерживаться привычного режима лечения: в подобных клинических ситуациях эффективность воздействия на основное неврологическое заболевание является приоритетной. Риск осложнений повышается у получающих иммуносупрессант в комбинации с преднизолоном в дозе ≥10 мг / сут. Инфузии ритуксимаба также могут увеличивать вероятность присоединения вирусных инфекций, но для большинства патологий спектра оптикомиелит-ассоциированных расстройств значимость терапевтического эффекта выше,чем потенциальная реализация рисков. Иногда целесообразно пересмотреть сроки повторных курсов и / или использовать альтернативные лечебные программы — например, при дополнительных факторах риска (ФР) либо отрицательных результатах определения антител к аквапорину‑4 (AQP4). Серьезные осложнения COVID‑19 диктуют необходимость прекращения ИТ заболеваний этой группы. У пациентов с внезапными и жизнеугрожающими рецидивами целесообразно перейти на прием только кортикостероидов до окончания эпидемического периода.
При развитии аутоиммунного энцефалита либо анти‑MOG-синдрома (присутствие антител к гликопротеину миелина олигодендроцитов — MOG) основной риск также будет связан с иммуносупрессией.
ИНСУЛЬТ
Само по себе ОНМК не делает пациента более восприимчивым к инфекции, однако инвалидность, особенно вследствие бульбарного пареза и / или дыхательной недостаточности, как и сопутствующие болезни (в том числе сердечная патология и сахарный диабет) увеличивают ее риск.
Имеются данные о возможной связи между COVID‑19 и 7‑кратным повышением вероятности инсульта в возрасте до 50 лет при минимальных проявлениях КВИ или их отсутствии, при этом риск возрастает в случае имеющихся нарушений гемостаза. Гиперкоагуляция при критических состояниях и кардиоэмболия в период инфицирования SARS‑CoV‑2 могут быть причинами различного рода сосудистых событий. Вследствие тропности вируса к рецепторам ангиотензинпревращающего фермента 2 типа (АПФ2) страдающие артериальной гипертензией могут иметь повышенную вероятность внутричерепного кровоизлияния из‑за колебаний артериального давления. Кроме того, у некоторых инфицированных наблюдается тяжелая тромбоцитопения — еще один фактор высокого риска внутримозговой геморрагической катастрофы. Способность вируса индуцировать прямое повреждение нейронов в кардиореспираторных центрах ствола мозга на экспериментальных моделях вызывает настороженность относительно возможного участия возбудителя в патогенезе дыхательной недостаточности у больных с COVID‑19, хотя прямых доказательств подобного механизма для человека пока нет.
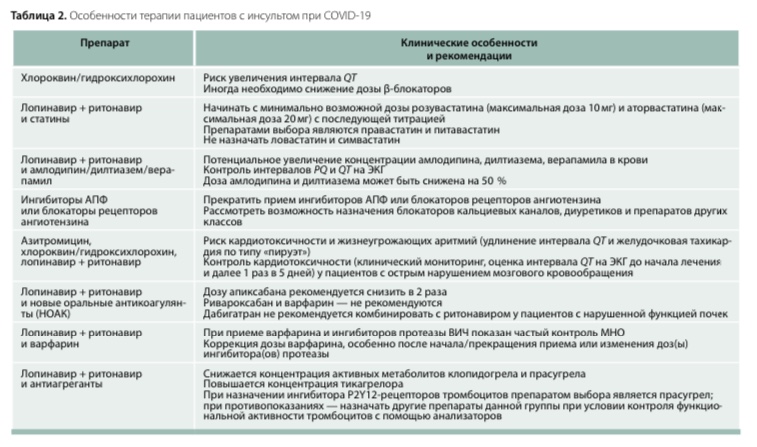
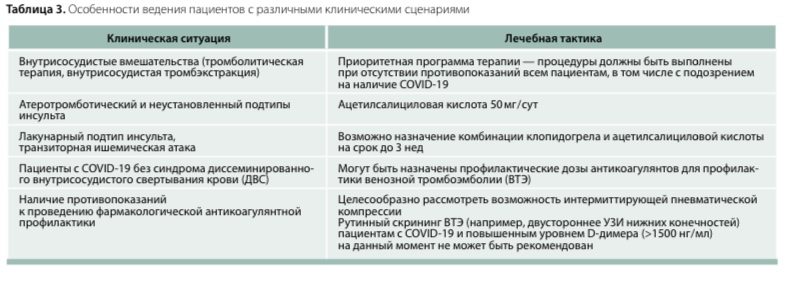
Особенности ведения пациентов с ОНМК (предсуществующим или развившимся во время пандемии) на фоне КВИ представлены в табл. 2 и 3.
ЭПИЛЕПСИЯ
Повышенному риску инфицирования SARS‑CoV‑2 подвержены пациенты с осложненной эпилепсией, в том числе фармакорезистентной, ввиду выраженных бульбарных поражений и / или слабости дыхательных мышц, а также расстройств дыхания, связанных с кифосколиозом или нарушениями подвижности. Значительная вероятность заражения отмечается и у больных с клиническими формами, чувствительными к гипертермии (в частности, синдромом Драве), туберозным склерозом и энцефалитом Расмуссена, получающих супрессивную ИТ.
Необходимо учитывать возможное взаимодействие противоэпилептических препаратов (ПЭП) с противовирусными и другими средствами, которые могут использоваться в лечении COVID‑19. Показано, что 7 ПЭП (габапентин, леветирацетам, прегабалин, ретигабин, топирамат, вигабатрин и зонисамид) не изменяют своего метаболизма и не влияют на течение КВИ. Вальпроаты и ламотриджин взаимодействуют лишь с лопинавиром / ритонавиром, остальные антиконвульсанты — с 2 или более ЛС. Некоторые медикаменты, применяемые для лечения инфекций верхних дыхательных путей (например, противоотечное средство псевдоэфедрин или антигистаминный препарат дифенгидрамин), могут усугубить судороги у пациентов с эпилепсией. Несмотря на сообщения о редких случаях развития судорожного синдрома при назначении хлороквина и гидроксихлорохина, противопоказаний к их назначению таким больным нет.
По общему мнению, если пациент хорошо контролирует свое заболевание, менять терапию в связи с пандемией КВИ не следует.
БОЛЕЗНЬ ПАРКИНСОНА
Пациенты с болезнью Паркинсона (БП) имеют высокий риск инфицирования COVID‑19 вследствие пожилого возраста, выраженной соматической коморбидности, а также при поздних (IV–V) стадиях по Хен–Яру, когда большую часть времени они проводят в постели.
В итальянском исследовании на репрезентативной выборке среди лиц от 55 лет и старше с БП было констатировано
12 сопутствующих заболеваний (включая поражение коронарных артерий, цереброваскулярные нарушения и сердечную недостаточность), увеличивающих вероятность тяжелого течения КВИ. Другое ретроспективное когортное исследование, проведенное в Японии, показало, что в сравнении с возрастными пациентами (учитывая зависимость от пола) больные паркинсонизмом, госпитализированные по поводу пневмонии, имели менее высокий уровень внутрибольничной смертности,
но более длительный срок госпитализации.
Повышенная восприимчивость к SARS‑CoV‑2 усугубляется наличием вегетативных расстройств на поздних стадиях БП. Существуют острые последствия COVID‑19 вегетативного характера для этой категории пациентов. Интенсивный кашель способен вызвать рефлекторный обморок; обезвоживание может усилить ортостатическую гипотензию, повышая вероятность обморока и падений, что опасно для этого контингента больных. В недавних работах сообщалось о нейротропизме вируса с вовлечением сосудодвигательного и дыхательного центров ствола головного мозга, что может увеличивать риск развития дыхательных и кардиоваскулярных расстройств центрального генеза.
Благодарим за предоставленный материал С.С. Никитина, С. В. Копишинскую, Н. О. Жаринову, И. А. Величко, Н. Г. Жукову,
В. В. Буцева, И. В. Коробейникова, А. А. Гасанову, А. С. Аракеляна, О. В. Петручик, А. Н. Паюдиса
с отдельными неврологическими заболеваниями и особенности ведения их в условиях пандемии.
РАССЕЯННЫЙ СКЛЕРОЗ И ДРУГИЕ АУТОИМУННЫЕ БОЛЕЗНИ ЦНС
Пациенты с рассеянным склерозом (РС) не имеют повышенного риска заражения новым коронавирусом вне зависимости от того, находятся ли они в фазе ремиссии или обострения. Увеличить риск могут проблемы с дыханием и / или глотанием вследствие значимой инвалидизации, а также проведение селективной иммунотерапии (ИТ).
При наличии острой или подострой неврологической симптоматики, особенно на фоне повышения температуры тела, необходимо исключить инфекционное поражение нервной системы (энцефалит, менингит, менингоэнцефалит, острый рассеянный энцефаломиелит, прогрессирующая мультифокальная лейкоэнцефалопатия (ЛЭП)). Для этого пациента переводят в инфекционный стационар. Необходимо четко дифференцировать признаки обострения существующего заболевания и неврологические проявления коронавирусной инфекции (КВИ) для правильного оказания медицинской помощи. Магнитно-резонансная томография (МРТ) головного и спинного мозга, в том числе с контрастным усилением, выполняется в плановом порядке.
Подход к назначению препаратов, изменяющих течение рассеянного склероза (ПИТРС), должен быть индивидуальным — чем выше клиническая эффективность медикамента, тем более персонализированно и осторожно следует рассматривать возможность его использования.
Применение ПИТРС в условиях COVID‑19
Безопасность применения того или иного лекарственного средства (ЛС) определяется для каждого случая отдельно (табл. 1). Продолжение или начало лечения препаратами интерферонов β‑1а и -1b, глатирамера ацетата считается безопасным. Терапия такими таблетированными ЛС, как терифлуномид, диметилфумарат, финголимод, может привести к лейко- и лимфопении, поэтому их назначение требует контроля общего анализа крови не реже 1 раза в 3 мес. для оценки иммунного ответа.
К препаратам 2-й линии, рекомендованным в условиях пандемии COVID‑19, относится натализумаб, однако необходимо учитывать возможность развития прогрессирующей мультифокальной ЛЭП на фоне его приема. Для профилактики нежелательных явлений и безопасности пациента интервал между инфузиями может быть увеличен. У получающих финголимод или натализумаб в период 2–4 мес. После отмены может произойти «ребаунд-эффект».
Применение таких средств, как окрелизумаб, алемтузумаб, кладрибин, а также выполнение трансплантации гемопоэтических стволовых клеток по возможности следует отложить.

Иммуносупрессия при заболеваниях спектра оптикомиелита на фоне COVID‑19
Несмотря на то что риск инфицирования SARS‑CoV‑2 при терапии азатиоприном, микофенолата мофетилом, метотрексатом возрастает, рекомендуется придерживаться привычного режима лечения: в подобных клинических ситуациях эффективность воздействия на основное неврологическое заболевание является приоритетной. Риск осложнений повышается у получающих иммуносупрессант в комбинации с преднизолоном в дозе ≥10 мг / сут. Инфузии ритуксимаба также могут увеличивать вероятность присоединения вирусных инфекций, но для большинства патологий спектра оптикомиелит-ассоциированных расстройств значимость терапевтического эффекта выше,чем потенциальная реализация рисков. Иногда целесообразно пересмотреть сроки повторных курсов и / или использовать альтернативные лечебные программы — например, при дополнительных факторах риска (ФР) либо отрицательных результатах определения антител к аквапорину‑4 (AQP4). Серьезные осложнения COVID‑19 диктуют необходимость прекращения ИТ заболеваний этой группы. У пациентов с внезапными и жизнеугрожающими рецидивами целесообразно перейти на прием только кортикостероидов до окончания эпидемического периода.
При развитии аутоиммунного энцефалита либо анти‑MOG-синдрома (присутствие антител к гликопротеину миелина олигодендроцитов — MOG) основной риск также будет связан с иммуносупрессией.
ИНСУЛЬТ
Само по себе ОНМК не делает пациента более восприимчивым к инфекции, однако инвалидность, особенно вследствие бульбарного пареза и / или дыхательной недостаточности, как и сопутствующие болезни (в том числе сердечная патология и сахарный диабет) увеличивают ее риск.
Имеются данные о возможной связи между COVID‑19 и 7‑кратным повышением вероятности инсульта в возрасте до 50 лет при минимальных проявлениях КВИ или их отсутствии, при этом риск возрастает в случае имеющихся нарушений гемостаза. Гиперкоагуляция при критических состояниях и кардиоэмболия в период инфицирования SARS‑CoV‑2 могут быть причинами различного рода сосудистых событий. Вследствие тропности вируса к рецепторам ангиотензинпревращающего фермента 2 типа (АПФ2) страдающие артериальной гипертензией могут иметь повышенную вероятность внутричерепного кровоизлияния из‑за колебаний артериального давления. Кроме того, у некоторых инфицированных наблюдается тяжелая тромбоцитопения — еще один фактор высокого риска внутримозговой геморрагической катастрофы. Способность вируса индуцировать прямое повреждение нейронов в кардиореспираторных центрах ствола мозга на экспериментальных моделях вызывает настороженность относительно возможного участия возбудителя в патогенезе дыхательной недостаточности у больных с COVID‑19, хотя прямых доказательств подобного механизма для человека пока нет.
Особенности ведения пациентов с ОНМК (предсуществующим или развившимся во время пандемии) на фоне КВИ представлены в табл. 2 и 3.


ЭПИЛЕПСИЯ
Повышенному риску инфицирования SARS‑CoV‑2 подвержены пациенты с осложненной эпилепсией, в том числе фармакорезистентной, ввиду выраженных бульбарных поражений и / или слабости дыхательных мышц, а также расстройств дыхания, связанных с кифосколиозом или нарушениями подвижности. Значительная вероятность заражения отмечается и у больных с клиническими формами, чувствительными к гипертермии (в частности, синдромом Драве), туберозным склерозом и энцефалитом Расмуссена, получающих супрессивную ИТ.
Необходимо учитывать возможное взаимодействие противоэпилептических препаратов (ПЭП) с противовирусными и другими средствами, которые могут использоваться в лечении COVID‑19. Показано, что 7 ПЭП (габапентин, леветирацетам, прегабалин, ретигабин, топирамат, вигабатрин и зонисамид) не изменяют своего метаболизма и не влияют на течение КВИ. Вальпроаты и ламотриджин взаимодействуют лишь с лопинавиром / ритонавиром, остальные антиконвульсанты — с 2 или более ЛС. Некоторые медикаменты, применяемые для лечения инфекций верхних дыхательных путей (например, противоотечное средство псевдоэфедрин или антигистаминный препарат дифенгидрамин), могут усугубить судороги у пациентов с эпилепсией. Несмотря на сообщения о редких случаях развития судорожного синдрома при назначении хлороквина и гидроксихлорохина, противопоказаний к их назначению таким больным нет.
По общему мнению, если пациент хорошо контролирует свое заболевание, менять терапию в связи с пандемией КВИ не следует.
БОЛЕЗНЬ ПАРКИНСОНА
Пациенты с болезнью Паркинсона (БП) имеют высокий риск инфицирования COVID‑19 вследствие пожилого возраста, выраженной соматической коморбидности, а также при поздних (IV–V) стадиях по Хен–Яру, когда большую часть времени они проводят в постели.
В итальянском исследовании на репрезентативной выборке среди лиц от 55 лет и старше с БП было констатировано
12 сопутствующих заболеваний (включая поражение коронарных артерий, цереброваскулярные нарушения и сердечную недостаточность), увеличивающих вероятность тяжелого течения КВИ. Другое ретроспективное когортное исследование, проведенное в Японии, показало, что в сравнении с возрастными пациентами (учитывая зависимость от пола) больные паркинсонизмом, госпитализированные по поводу пневмонии, имели менее высокий уровень внутрибольничной смертности,
но более длительный срок госпитализации.
Повышенная восприимчивость к SARS‑CoV‑2 усугубляется наличием вегетативных расстройств на поздних стадиях БП. Существуют острые последствия COVID‑19 вегетативного характера для этой категории пациентов. Интенсивный кашель способен вызвать рефлекторный обморок; обезвоживание может усилить ортостатическую гипотензию, повышая вероятность обморока и падений, что опасно для этого контингента больных. В недавних работах сообщалось о нейротропизме вируса с вовлечением сосудодвигательного и дыхательного центров ствола головного мозга, что может увеличивать риск развития дыхательных и кардиоваскулярных расстройств центрального генеза.
Благодарим за предоставленный материал С.С. Никитина, С. В. Копишинскую, Н. О. Жаринову, И. А. Величко, Н. Г. Жукову,
В. В. Буцева, И. В. Коробейникова, А. А. Гасанову, А. С. Аракеляна, О. В. Петручик, А. Н. Паюдиса


















