Статьи
Рак желудка после эрадикации H. pylori: призрак или реальная угроза?
02.11.2020
Рак желудка (РЖ) занимает лидирующие позиции в структуре онкологической заболеваемости и смертности во всем мире. Ежегодно от него умирают около 800 тысяч человек. Примерно у двух третей пациентов это заболевание диагностируется на поздней стадии, когда проведение радикальных методов лечения становится невозможным.

Инфекция Helicobacter pylori (H. pylori) рассматривается в качестве основного этиологического фактора рака желудка. Ретроспективный анализ данных о 371 813 пациентах (средний возраст — 62 года; 92,3 % мужчин) с диагностированной инфекцией H. pylori, находившихся под наблюдением с 1 января 1994 года по 31 декабря 2018 года, показал, что суммарная заболеваемость раком желудка через 5, 10 и 20 лет после обнаружения H. pylori составила 0,37 %, 0,5 % и 0,65 % соответственно. В то же время по результатам эпидемиологических исследований установлено, что внедрение национальных программ по проведению массовой эрадикационной терапии приводит к резкому снижению риска развития РЖ.
Эти данные нашли свое отражение в соответствующем положении международного консенсуса Маастрихт V по диагностике и лечению хеликобактерной инфекции, согласно которому эрадикация H. pylori снижает риск развития РЖ. Показатель NNT (англ. number needed to treat), или ЧБНТ для эрадикационной канцеропревенции (число больных, которых необходимо лечить, чтобы устранить H. pylori и тем самым предотвратить 1 случай РЖ), составляет 124 для популяции в целом. При этом в разных географических регионах наблюдаются существенные различия показателя NNT в популяциях с различным уровнем заболеваемости раком — от 15 среди китайских мужчин до 245 среди американских женщин.
Однако, как оказалось, проведение эрадикации и элиминация H. pylori не всегда устраняют риск развития РЖ, поскольку у некоторых пациентов к этому моменту уже формируются предраковые изменения слизистой оболочки желудка (атрофия, кишечная метаплазия и интраэпителиальная неоплазия / дисплазия).
Согласно собственным данным, в открытом когортном проспективном исследовании персистенция воспалительного инфильтрата в слизистой оболочке желудка через год после успешной эрадикационной терапии отмечается у 28,2 % пациентов (рис. 1). Сохранение хронического воспалительного инфильтрата ассоциировано с повышением активности ферментов перекисного окисления липидов и выработкой активных форм кислорода. В условиях «оксидативного стресса» происходят необратимые повреждения ДНК клеток, которые, накапливаясь со временем, создают «стартовую площадку» для развития РЖ в последующем.
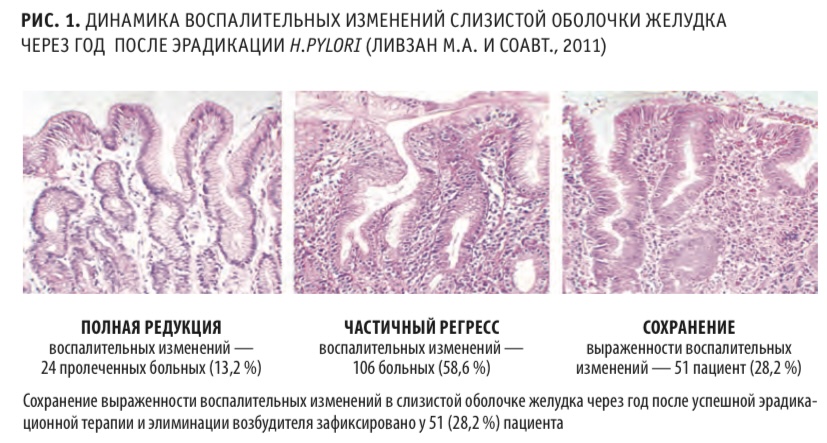
Следовательно, крайне важно выявлять пациентов из группы высокого риска по развитию РЖ среди больных с постхеликобактерным гастритом для проведения своевременной канцеропревенции. В программу лечения таких пациентов необходимо включать курсы цитопротективной терапии, позволяющей защитить клетки слизистой оболочки желудка от повреждающего действия продуктов воспаления и перекисного окисления липидов, с целью профилактики прогрессирования предраковых изменений.
ГДЕ ТОЧКА НЕВОЗВРАТА?
Стратификация риска развития РЖ помимо диагностики инфекции H. pylori включает оценку морфологических изменений слизистой оболочки желудка по системе Operative Link for Gastritis Assessment of Atrophic Gastritis (OLGA), предложенной международной группой экспертов в 2008 году. В нашей стране существует удобная модифицированная визуально-аналоговая шкала оценки атрофии слизистой оболочки желудка, разработанная на основе данной системы и утвержденная в 2009 году 3-м съездом Российского общества патолого-анатомов (А.В. Кононов, С.И. Мозговой). Системой определяются интегральные показатели степени и стадии хронического гастрита. Под степенью понимается выраженность инфильтрации собственной пластинки слизистой оболочки желудка воспалительными клетками (лимфоцитами, плазматическими клетками и нейтрофилами). Под стадией — наличие атрофических изменений.
Стадия атрофических изменений и степень воспаления не определяют наличие и выраженность клинических симптомов, при этом данные гистологического исследования необходимы для прогноза и выбора тактики ведения пациента.
Формирование кишечной метаплазии в хорошо известном клиницистам каскаде P. Correa по пути прогрессии хронического активного гастрита до рака желудка является своеобразной «точкой невозврата», которая ограничивает эффективность последующих мер канцеропревенции (рис. 2). Если воспаление и неопределенная атрофия при своевременной и рациональной терапии могут регрессировать, то кишечная метаплазия тенденции к обратному развитию не имеет.
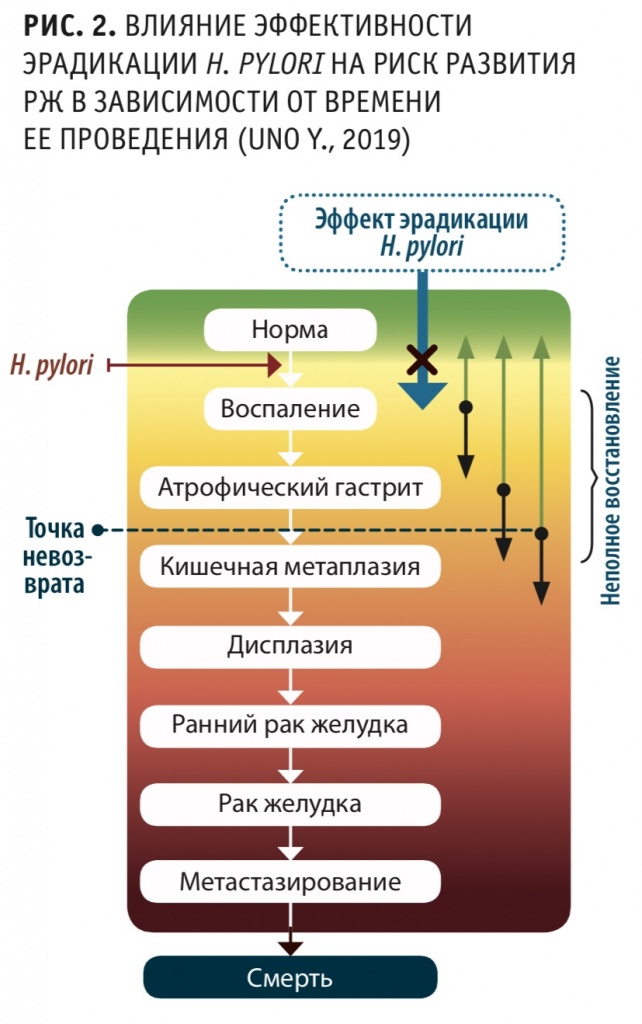
В 2017 году было установлено, что после успешной эрадикации H. pylori для восстановления слизистой оболочки желудка у части пациентов может потребоваться до 10 лет. В другом исследовании 2018 года с включением 1755 пациентов, находившихся под наблюдением в течение 5 лет после эрадикации, сообщается, что РЖ развился у 5 % лиц с III и IV стадией хронического гастрита. Среди пациентов со II стадией в 53 % случаев изменений не наблюдалось, в 19 % отмечался переход в стадию III, и только 28 % больных вернулись к стадии 0 или I. Эти результаты свидетельствуют о том, что у пациентов с хроническим гастритом даже на стадиях, поддающихся лечению (неопределенная атрофия), гистологическое восстановление слизистой оболочки желудка после успешной эрадикации до уровня, обнаруживаемого у неинфи¬цированных лиц, может занимать достаточно длительное время.
На фоне уже сформировавшейся атрофии слизистой оболочки желудка после элиминации H. pylori важную роль играет дисбиоз верхних отделов пищеварительного тракта.
Нарушение нормальной микрофлоры поддерживает воспаление и сохраняет риск развития РЖ. Колонизация желудка микроорганизмами, отличными от Н. pylori (Helicobacter spp, Proteus mirabilis, Citrobacter freundii, Klebsiella pneumoniae, Enterobacter cloacae, Staphylococcus aureus), провоцирует выработку нитрозаминов с их проканцерогенным потенциалом.
ОНКОЛОГИЧЕСКАЯ НАСТОРОЖЕННОСТЬ
H. pylori относится к наиболее важным факторам развития рака желудка. У лиц с уже сформировавшимися предраковыми изменениями слизистой оболочки желудка (атрофия, кишечная метаплазия, интраэпителиальная неоплазия/дисплазия) даже после успешной эрадикации сохраняется риск развития РЖ. Пациентам данной группы в зависимости от выраженности воспалительных изменений и тяжести атрофии требуются постоянное динамическое наблюдение и своевременное осуществление необходимых мер канцеропревенции.
Читайте также
- Маммография? Спасибо, не надо!
- SOLAR-1. Алпелисиб – теперь и в России
- Клиническая практика терапии неоперабельного уротелиального рака после прогрессирования
- Рак щитовидной железы: современные возможности и перспективы лечения
- 10 вопросов к главному онкологу о сегодняшнем и завтрашнем дне специальности
- Олапариб в лечении мКРРПЖ: результаты исследования PROfound
- Преимущества таргетной терапии при раке легкого
- Есть ли место иммунотерапии при ранних стадиях онкологических заболеваний?

















