Статьи
Ранняя диагностика рака легкого: достижения и проблемы
— Виктор Викторович, насколько распространен сегодня рак легкого (РЛ) в России и мире, есть ли заметная динамика в показателях заболеваемости и смертности от данного заболевания?
— Рак легкого — злокачественное новообразование (ЗНО), стабильно занимающее на протяжении уже нескольких десятилетий одно из первых мест по распространенности в мире; это же относится и к нашей стране. Максимальные показатели заболеваемости у мужчин регистрируются в Центральной и Западной Европе (53,5 случаев на 100 тыс.) и в Западной Азии, а минимальные — в странах Средней и Восточной Африки. Эту опухоль также отличает не только высочайшая агрессивность, но и другая, еще более грозная особенность: бессимптомное течение на I–II стадиях. Появление таких клинических симптомов, как слабость, похудение, кашель, кровохарканье, обструктивная пневмония, боли в грудной клетке, свидетельствует о наличии уже местно распространенного процесса с вовлечением органов средостения и грудной клетки.
Если говорить о I стадии РЛ, то даже здесь после радикальной, казалось бы, операции выздоравливают не более 70 % пациентов, а 5летняя выживаемость при II стадии не превышает 50 %.
Ежегодно в мире регистрируется более 1,3 млн случаев РЛ, что составляет 12 % в структуре общей онкологической заболеваемости. При этом погибают от данной патологии более 1,2 млн человек ежегодно. В нашей стране каждый год выявляется более 52 тыс. новых случаев РЛ, и в течение 1го года после установления диагноза от этого заболевания умирают более 54 % заболевших. РЛ очень редко диагностируется в возрасте до 40 лет. Средний возраст выявления этой опухоли — 60 лет, а наибольшая распространенность отмечается у лиц старше 75 лет. Около 87 % случаев развития РЛ ассоциировано с курением.
— Какой тип РЛ наиболее опасен?
— До последнего времени выделяли две основные клинико морфологические формы РЛ, отличающиеся степенью злокачественности, частотой и характером метастазирования. Это немелкоклеточный РЛ (НМРЛ) и мелкоклеточный РЛ (МРЛ), их соотношение соответственно 80 и 20 %. В свою очередь, к НМРЛ относили плоскоклеточный, крупноклеточный рак и аденокарциному. По данным морфологической классификации ВОЗ от 2015 г., каждый гистологический тип теперь рассматривается отдельно. А вот понятие НМРЛ официально больше не используется, хотя и остается легитимным. Аденокарцинома — самый распространенный морфологический тип РЛ, она чаще развивается как периферический РЛ.
В итоге на ранних стадиях РЛ выявляется только в 25 % случаев, а у 75 % пациентов — уже на III–IV стадии, когда возможно только консервативное лечение.
— Раз выявляемость этой опухоли на ранних стадиях так низка, в мире, наверное, уже проведено немало попыток скрининга РЛ?
— Действительно, первые попытки были еще в начале 1950х гг. И их стало намного больше после того, как в 1958 г. американские ученые Е. Хаммонд и Д. Холл сделали крупнейшее в онкологии открытие, установив, что курение — главный фактор риска развития РЛ. США, Япония, Англия, ФРГ, Канада и Швеция стали пионерами крупных скрининговых исследований. В центре внимания таких изысканий чаще всего оказывались люди старше 40–45 лет, в основном мужчиныкурильщики.
Расскажу сначала о нелучевом методе диагностики, который стал использоваться при скрининге РЛ, — цитологическом исследовании мокроты (ЦИМ). В 1951 г. Георгиос Папаниколау, автор известного «теста Папаниколау», или цитологического мазка для определения предраковых или раковых клеток во влагалище и шейке матки, впервые продемонстрировал возможность прижизненной диагностики рака in situ легких с использованием ЦИМ. Метод сразу показал высокую специфичность в обнаружении опухолей — особенно центральной локализации при плоскоклеточном РЛ.
Динамическое цитологическое исследование мокроты позволяло иногда выявлять центральный РЛ за 5–13 лет до появления рентгенологических и клинических симптомов. Было также доказано, что появлению преинвазивного плоскоклеточного рака в течение 3–8 лет может предшествовать цитологически диагностируемая атипическая плоскоклеточная метаплазия бронхиального эпителия, а рак in situ может существовать в виде крошечных «очажков» в легочной ткани до 10–15 лет, пока не проявится клинически. Этот период был назван «золотым периодом» развития ЦРЛ.
— Замечательные результаты! Но, видимо, возникли препятствия для внедрения этого метода в практику?
— Таким препятствием оказалась чувствительность данного метода, не превышавшая в первые годы его применения 15 %. К началу XXI в. чувствительность ЦИМ удалось поднять примерно до 55 %. Столь невысокое значение этого показателя не позволило использовать исследование мокроты в качестве надежного скринингового метода РЛ.
Уже в нашем веке продолжается усовершенствование ЦИМ. Например, разрабатываются технологии иммуноцитологического исследования мокроты с использованием моноклональных антител. Такие тесты выявляют повышенную экспрессию РНКсвязывающего белка hnRNP A2/B1. При изучении с помощью полимеразной цепной реакции в бронхиальном лаваже больных РЛ установлено, что чувствительность и специфичность этого метода достигают соответственно 73 и 86 %. А при использовании этого метода вместе с традиционным цитологическим исследованием чувствительность возрастает до 80 %.
Группа корейских ученых недавно представила работу по ранней диагностике РЛ путем выявления в мокроте подтипов MAGE A1–6 генов с помощью полимеразной цепной реакции в реальном времени. В мокроте здоровых людей положительный уровень экспрессии этих генов был менее 2 %, а у больных РЛ — более 54 %. К сожалению, других настолько надежных онкомаркеров РЛ пока нет.
Что касается анализов на драйверные или активирующие канцерогенез мутации таких генов, как EGFR, EML4ALK, KRAS, то они применяются не для ранней диагностики РЛ, а как молекулярные мишени для назначения таргетных противоопухолевых препаратов уже на распространенной стадии РЛ.
Заслуживает внимания и метод автоматизированной количественной цитометрии, разработанный в Канаде. Он основан на системной оценке характеристик ядра клетки, полученных из образцов мокроты пациентов, и на поиске так называемых опухоль ассоциированных изменений.
Технология была апробирована, в том числе в НМИЦ онкологии им. Н. Н. Петрова в СанктПетербурге, где в исследовании участвовали 268 человек. При специфичности 77 % общая чувствительность метода составила 58 % при ранних стадиях развития РЛ. Методика оказалась наиболее чувствительной (67 %) при выявлении плоскоклеточного РЛ.
— А использование для скрининга рентгено- и флюорографии ждало успешное будущее?
— Это не совсем так. Начнем с небольшого исторического экскурса.
Первые попытки рентгенологического скрининга РЛ предприняты еще в 1949 г.: американские ученые Р. Оверхолт и С. Сомедт для ранней диагностики данной опухоли предложили проводить периодическое рентгенологическое исследование населения. Авторам удалось выявить всего 10 бессимптомных опухолей на 100 тыс. тестов, и особенно низкой эффективность такой диагностики оказалась в группе пациентов с центральным бессимптомным РЛ.
Более удачным оказался проект, выполненный в США в 1951 г., в котором оценивались данные флюорографического обследования 6,1 тыс. мужчин старше 45 лет. Выявлено 84 больных РЛ с резектабельностью в 35 %.
В 1953 г. опубликованы данные огромного (1,87 млн участников) исследования, где для скрининга применялись рентген и ЦИМ. В результате обнаружили лишь 193 (0,01 %) случаев РЛ с резектабельностью в 56 % и 5летней выживаемостью в 44 %.
Во второй половине прошлого века последовала целая серия других подобных работ с участием нескольких миллионов человек. Благодаря усовершенствованию технологий рентгенологического исследования и ЦИМ получены более перспективные, но отнюдь не обнадеживающие результаты. В скрининговой группе уровень выявляемости, резектабельности, а также 5 и даже 10летней выживаемости оказывались выше, чем в контрольной группе. Но в итоге даже после сверхинтенсивного скрининга, представляющего собой четыре ежегодных рентгеновских исследования злостных курильщиков плюс ЦИМ в течение 6 лет, не удалось достоверно снизить смертность в группе больных РЛ.
И все же скрининг РЛ с помощью «рентгена+ИМ» не считается совсем бесперспективным. Поэтому в мире есть много онкологов, не согласных с последними рекомендациями Американского онкологического общества, где рентгенография грудной клетки не рекомендована для скрининга РЛ изза низкой эффективности.
— А что можно сказать о скрининге с использованием компьютерной томографии (КТ)?
— В 1993 г. в Европе стартовало исследование (The Early Lung Cancer Project, ELCAP), которое уже вскоре переросло в крупный международный проект (International ELCAP), где участвовали более 30 тыс. человек. Они обследовались сначала с использованием базовой рентгенографии и низкодозной КТ, а затем с помощью КТ высокого разрешения.
Правда, скрининг проводился только в группах высокого риска РЛ. Даже самые богатые страны не могут себе позволить использовать настолько дорогой метод для поголовного обследования: недавно подсчитано, что на выявление 1 пациента со скрытой формой РЛ необходимо более 1 тыс. долларов.
В 2006 г. по итогам исследования IELCAP выявлено 484 случая РЛ, из них 85 % — I стадии. Радикальные операции выполнили 411 пациентам. Затем на основании 40 мес наблюдения смоделировали 10летнюю выживаемость, которая составила 80 % среди всех пациентов и 88 % — при I стадии РЛ. Последовали и другие масштабные скрининговые работы с участием курильщиков старше 40 лет, например, в Японии, где вместе с КТ и рентгенографией применялось и ЦИМ. После 15 050 тестов обнаружились 993 случая с подозрением на РЛ, и для уточнения диагноза использовалась уже КТ высокого разрешения. В результате РЛ выявлен у 71 пациента, и из них 89 % в I стадии опухолевого процесса.
— Несмотря на то, что КТ по причине высокой стоимости непригодна для всеобщего или тотального скрининга, в группах высокого риска этот метод намного эффективнее рентгенографии?
— Вы правы. Вопервых, КТскрининг гораздо значительнее, чем рентгенография, повышает показатели выявляемости, резектабельности и выживаемости. Причем особенно на начальных стадиях РЛ. Вовторых, КТ гораздо более зорко «различает» центральную локализацию рака (60 % всех видов РЛ). А ведь именно к центральной локализации обычно относится рак не только у курильщиков, но и метастатические поражения бронхиального дерева у пациентов с любыми типами этого новообразования после радикального лечения опухоли I и II стадии.
— Насколько же эффективным КТ-скрининг оказался в отношении самой «твердой» конечной точки — снижения смертности по причине РЛ?
— К сожалению, оптимистичная оценка по этому показателю дана только по результатам исследований IELCAP и еще одного, проведенного в Mayo Clinic (США). Оно включало 1,5 тыс. курильщиков старше 50 лет. В течение 6 лет наблюдения в скрининговой группе смертность от РЛ достоверно снижалась на 28 %, а в перспективе 15 лет — на 15 %. Зато другие крупные исследования КТскрининга получили сдержанную или даже негативную оценку в отношении снижения смертности.
Что касается МРТ и позитронноэмиссионной томографии (ПЭТ), то они непригодны для скрининга и используются только при дообследовании пациента для дифференциальной диагностики первичной опухоли, определения распространенности опухолевого процесса и выявления рецидивов.
— Продолжаются ли в мире попытки применения лучевых методов для скрининга РЛ?
— Только для групп высокого и очень высокого риска. Цель таких работ состоит в поиске более надежной и «зоркой» методики для обнаружения, прежде всего, раннего бессимптомного центрального РЛ, остающегося ключевой проблемой в онкопульмонологии.
Несколько рандомизированных работ доказали высокую эффективность низкодозной мультиспиральной компьютерной томографии (НДСКТ) для скрининга РЛ среди заядлых курильщиков. Специфичность этого анализа при диагностике опухолей размером от 1 до 1,5 см достигает 90–97 %, а 63 % таких новообразований обнаруживаются на стадии IA или IB. Это значительно лучше результатов стандартного КТисследования, где большинство случаев РЛ выявляется на стадиях IB и II. Благодаря применению НДСКТ смертность от РЛ достоверно снизилась на 20 % по сравнению с итогами использования флюорографии.
В Научнопрактическом центре медицинской радиологии Департамента здравоохранения Москвы разработан пилотный проект, где НДСКТ применяется в группах высокого риска для скрининга РЛ и других заболеваний органов грудной клетки.
В рамках проекта проходит кластерное рандомизированное популяционное исследование такого метода.
— Но это же дорогое мероприятие?
— НДСКТобследования осуществляются в рамках уже доведенных до медицинских организаций средств, и это не требует дополнительных затрат. Старт проекта — начало 2018 г., в нем примут участие более 3,6 тыс. москвичей, удовлетворяющих критериям групп высокого риска по РЛ. Проект осуществляется на базе 10 московских поликлиник и Московского научно практического центра борьбы с туберкулезом Департамента здравоохранения Москвы.
— Существуют ли эндоскопические методы, пригодные для скрининга РЛ?
— Бронхоскопическое исследование никогда не использовалось для таких же широкомасштабных скринингов РЛ, которые проводились с помощью флюорографии, ЦИМ и КТ. Эта процедура весьма сложна и трудоемка, поскольку требуется тщательный осмотр не только основного ствола, но и множества извилистых и узких ветвей бронхиального древа. И анализ может быть проведен только эндоскопистомпульмонологом, прошедшим специальную подготовку. Во всем мире таких специалистов гораздо меньше, чем лучевых диагностов.
Кроме того, бронхоскопия, проводимая даже с помощью самых современных устройств с тонким и эластичным зондом, не может осуществляться без местной, а иногда и общей анестезии.
— Для чего же тогда применяется бронхоскопия?
— Это основной метод раннего обнаружения скрытых рентгенонегативных форм центрального РЛ, которые не способны «увидеть» даже самые совершенные методы КТ, МРТ или ПЭТ. Считается, что плоскоклеточный центральный РЛ возникает в дыхательных путях вследствие последовательных молекулярных и клеточных изменений.
Современная эндоскопия — совершенно незаменимый способ идентификации поверхностно распространенных очагов мета и диспластического предрака и раннего рака малого размера и без явных признаков опухолевой инфильтрации слизистой оболочки трахеи и бронхов.
К концу 1960х гг. в тех же странах, где широко апробировался скрининг по схеме «рентген+ЦИМ», накоплен опыт и по бронхоскопической диагностике центрального РЛ, разработана методика поиска скрытой опухоли бронха. Следующий этап связан с изобретением в 1966 г. гибкого бронхофиброскопа. Результативность бронхофиброскопической диагностики начального центрального рака, по сравнению с ригидной бронхоскопией, возросла на 40–50 %.
Успешно прошли и первые исследования, правда, в очень небольших (например, 168 злостных курильщиков) скрининговых группах. Так было доказано, что бронхоскопия отлично «распознает» не только сам РЛ, но и предраковые заболевания. Напомню, что ценность эндоскопической бронхоскопии заключается и в возможности получать биопсийные образцы ткани, а также проводить малоинвазивные хирургические процедуры.
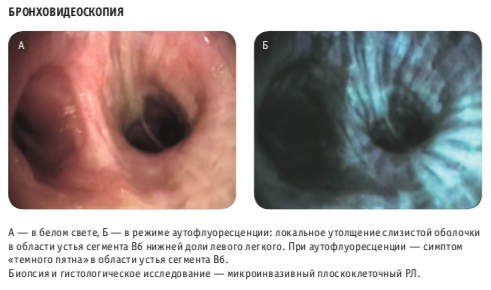
Следующим шагом в совершенствовании эндоскопии стало создание методик, которые помогали различать скрытые очаги рака слизистой оболочки бронхов, недоступные для традиционной эндоскопической визуализации в белом свете. Я говорю о методах так называемой экзогенной флуоресценции, эндогенной аутофлуоресценции и узкоспектральной эндоскопической спектрофотометрии.
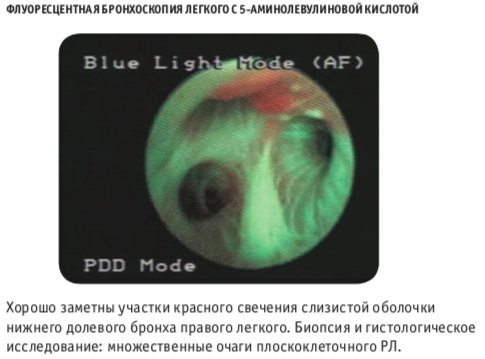
Флуоресцентная бронхоскопическая диагностика основана на избирательности накопления экзогенных и индуцированных эндогенных фотосенсибилизаторов в ткани опухоли и возможности ее обнаружения по характерной флуоресценции.
Принцип узкоспектральной эндоскопии состоит в элиминации из испускаемого источником света красной спектральной составляющей и эндоскопического осмотра слизистой оболочки в синезеленой части спектра, соответствующей пикам поглощения света гемоглобином. В зеленой части спектра визуализируются венулы подслизистого слоя. А в синем свете определяются капилляры слизистой оболочки. Применение подобной бронховидеоскопии позволяет оценивать архитектонику и аномалию капиллярной сети слизистой оболочки бронхиального дерева.
Наиболее современными технологиями эндоскопии бронхов считаются конфокальная лазерная эндомикроскопия и эндоцитоскопия — методики прижизненной микроскопической диагностики очагов предрака и раннего центрального РЛ. Такие методы дают возможность осматривать слизистую оболочку бронхов с увеличением до 1150 раз и непосредственно в процессе исследования получать изображения, сравнимые с гистологическими. В результате данной оптической биопсии или «гистологии in vivo» формируется микроскопическое изображение настолько высокого разрешения, что можно прижизненно оценить аномалии капиллярной сети слизистой оболочки и подслизистого слоя, особенности метаболизма, оксигенации и пролиферативной активности в зоне неоплазии, а главное — микроструктуру ткани вплоть до размера клеточного ядра.
— Расскажите, пожалуйста, подробнее о способах диагностики РЛ в руководимом вами отделении.
— Мы начали применять эндоскопические методы в диагностике РЛ еще с 1984 г. За последние 30 лет обследовано более 16 тыс. пациентов из групп высокого риска. Выявлено 172 случая раннего РЛ, изучены и классифицированы различные формы роста и локализации так называемых малых опухолей слизистой оболочки бронхов.
В отделении применяется не только стандартная бронховидеоскопия в белом свете, но также мультимодальное эндоскопическое исследование. Оно стало основой экспертной диагностики предраковых заболеваний и раннего РЛ. В предыдущем номере «Онкологии Сегодня» мой коллега С. С. Пирогов уже рассказал об этом комплексе инновационных исследований, но в отношении рака желудка. При обследовании бронхов мы применяем, в принципе, те же приемы.
Речь идет об использовании таких технологий, как аутофлуоресценция, узкоспектральная эндоскопия и эндосонографическое исследование, а также эндоскопии сверхвысокого увеличения: конфокальной лазерной эндомикроскопии и эндоцитоскопии. Такой комбинированный подход дает возможность детально изучить слизистую оболочку не только на макро, но и на микроструктурном уровне.
Это с высокой точностью позволяет выявить различные этапы предраковых заболеваний и РЛ. По итогам нашей работы показатели чувствительности и специфичности при использовании мультимодальной бронхоскопии с целью выявления скрытых очагов рака превысили 90 %.
Затем, благодаря применению эндобронхиальных методов органосохраняющего хирургического лечения, удалось добиться полной регрессии очагов этих ЗНО в 89 %, а при размере опухоли не более 1 см по плоскости полная регрессия составила 100 %.
— Как вы считаете, смогут ли уже в обозримом будущем в клинической практике применяться скрининговые методы, например, НДСКТ, или какие-то из описанных вами бронхоскопических методов? Возможно, пока в небольших группах самого высокого риска?
— По оценкам ВОЗ, злостных курильщиков в мире свыше 1,25 млрд человек. Мне кажется, что еще остается открытым вопрос о разработке скринингового метода РЛ, надежного и доступного для широкой клинической практики, а тем более — пригодного как для поголовных осмотров населения, так и в группах онкологического риска.
В то же время я надеюсь, что уже вскоре будет создан метод диагностики предрака и самого раннего РЛ с чувствительностью и специфичностью, близкими к 100 %. С позиций сегодняшнего дня, одним из ведущих методов выявления скрытых форм центрального РЛ может стать мультимодальное эндоскопическое исследование легких.

















