Статьи
РМП: иммунотерапия для всех?
Иммунотерапия в первой линии может быть предложена практически любому больному метастатическим или местнораспространенным раком мочевого пузыря. О пациентах, которым иммунотерапия необходима сразу, и тех, кто может подождать, а также о рефлекторном нахождении врача в зоне комфорта — в экспертном мнении А.С. Калпинского на основании собственного опыта и литературных данных.
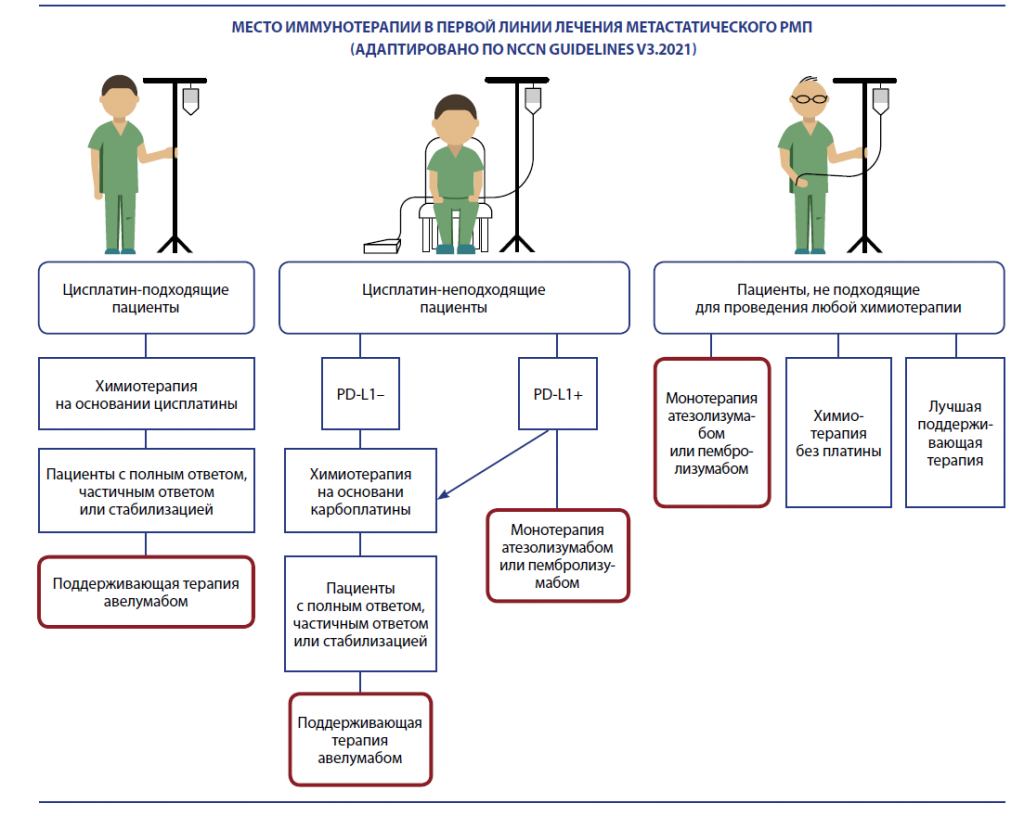
Согласно обновленным международным рекомендациям, практически любому пациенту с метастатическим или местнораспространенным раком мочевого пузыря (РМП) может быть проведена терапия ингибиторами иммунных контрольных точек уже в первой линии. Ранее такая опция была доступна для больных, которым невозможно проведение терапии на основе цисплатина (при условии положительного статуса PD-L1), или же не подходящих ни для какой химиотерапии на основе препаратов платины.
Теперь иммунотерапия может быть назначена в комбинации с химиотерапией (атезолизумаб) или же в поддерживающем режиме (авелумаб). Таким образом, в том или ином варианте ингибиторы иммунных контрольных точек могут быть рекомендованы практически любому пациенту уже в первой линии лечения. Означает ли это, что от химиотерапии можно отказаться или что ее значение становится все меньшим? И есть ли пациенты, для которых иммунотерапия — опция не первого выбора?
Остаться в зоне комфорта
Химиотерапия на основе цисплатина была и остается наиболее эффективным вариантом лечения в течение нескольких десятилетий.
— Всегда преимущества были и остаются за режимами на основе цисплатина, — отмечает А.С. Калпинский. — Еще на заре развития системной терапии РМП выживаемость при применении цисплатина составляла около 15 месяцев., при смене же на карбоплатин — около 9 месяцев. При этом и в России, и в мире признана проблема как недоиспользования режимов химиотерапии в целом, так и предпочтения специалистов применять менее токсичный и менее эффективный режим на основе карбоплатина.
Возможность проведения химиотерапии определяется по критериям Galsky. К критериям отбора пациентов для химиотерапии на основе препарата цисплатин относятся статус по шкале ECOG 0–1, скорость клубочковой фильтрации (СКФ) > 60 мл/мин/1,73 м2. При этом пациентам с сердечной недостаточностью (СН) < II функционального класса по шкале NYHA, нарушением слуха 0–II степени (в связи с вероятностью снижения слуха на 19–20 дБ и потенциальным снижением слуха до III–IV степени) или периферической нейропатией 0–I степени не рекомендована химиотерапия на основе препарата цисплатин.
— Согласно эпидемиологическим данным, в мире около 50 % пациентов первичной популяции могут перенести режим на основе цисплатина, — отмечает А.С. Калпинский. — Еще примерно 40 % может быть проведена терапия на основе карбоплатина. Оставшиеся 10 % больных — это те, кому исходно не может быть проведена никакая химиотерапия на основе препаратов платины, — ранее этим больным можно было предложить другие варианты химиотерапии, в частности на основе паклитаксела.
Однако в реальности таких пациентов намного больше, отмечает А.С. Калпинский. По мнению эксперта, многие пациенты могли бы быть подходящими для химиотерапии (в том числе на основе цисплатина), если бы получали своевременную помощь по поводу онкологического заболевания. Другие не имеют действительных противопоказаний к ней, но не получают необходимого лечения в силу избыточной осторожности врачей.
— На основании скорости клубочковой фильтрации происходит большая часть отказов от химиотерапии, в ряде случаев неоправданных, — отмечает А.С. Калпинский. — У пациента с РМП снижение СКФ может быть обусловлено в том числе распространенно- стью процесса. Связанное с блоком почки снижение СКФ может на фоне химиотерапии даже разрешаться. Однако, безусловно, учитывая намного меньшую токсичность ингибиторов иммунных контрольных точек, врач практически рефлекторно избегает не просто более токсичной химиотерапии, но любого ее варианта, предпочитая монотерапию ингибиторами иммунных контрольных точек.
В настоящее время мировое экспертное сообщество рассматривает вопрос пересмотра критериев для возможности проведения химиотерапии на основе цисплатина: в том числе обсуждается возможность снижения порогового требования относительно СКФ до 40–50 мл/мин.
— Кроме того, для многих специалистов избыточно тревожной выглядит возможность назначения химиотерапии пациенту с, например, нефростомой, — рассказывает А.С. Калпинский. — Однако при квалифицированной и своевременной помощи химиотерапия может быть проведена и таким пациентам.
По словам А.С. Калпинского, многие специалисты отказываются от химиотерапии или ее наиболее эффективных схем не в силу объективных противопоказаний, а из-за желания остаться в зоне комфорта. И эта тенденция общемировая, имеющая место даже в рамках международных клинических протоколов.
— Например, в исследовании ImVigor более 60 % подходили для проведения терапии на основе цисплатина, однако получили ее лишь 30 %, остальные больные были пролечены с использованием карбоплатина, — отмечает А.С. Калпинский. — И здесь важную роль сыграло в том числе личное предпочтение химиотерапевта.
Для ХТ-подходящих
Ингибиторы иммунных контрольных точек, одобренные для применения при РМП, в первую очередь изменили возможности пациентов, которые не могут получить химиотерапию.
— Еще десять лет назад 5‑летняя выживаемость больных метастатическим РМП составляла не более 6 %, — подчеркивает А.С. Калпинский. — Пациентам, не подходящим для проведения химиотерапии, по сути, мы могли предложить только ожидание конца.
Новые схемы, одобренные в течение последнего года, предполагают применение ингибиторов иммунных контрольных точек уже в первой линии у пациентов, которые могут получить химиотерапию. Атезолизумаб может быть применен в комбинации с химиотерапией, авелумаб — в поддерживающем режиме сразу после завершения курса химиотерапии в случае наличия ответа на нее.
В настоящий момент схема, подразумевающая одновременное применение химиотерапии и атезолизумаба, зарегистрирована Минздравом РФ, планируется ее включение в отечественные рекомендации. В международных же рекомендациях пока что атезолизумаб сохраняет свое положение в качестве препарата монотерапии, предназначенного для лечения при прогрессировании заболевания на фоне платиносодержащей химиотерапии (прогрессирование на первой линии). Как и пембролизумаб, он может быть применен в первой линии терапии у пациентов с высоким уровнем экспрессии PD‐L1, не подходящих для терапии на основе цисплатина. Атезолизумаб может быть назначен без определения статуса PD‐L1 пациентам, которым не может быть назначена химиотерапия на основе препаратов платины.
Авелумаб в составе поддерживающей терапии уже вошел в международные рекомендации, и с августа 2021 года настоящее показание зарегистрировано и в РФ. Ожидается и включение новой схемы в отечественные стандарты.
На конгрессе EAU, прошедшем в июле текущего года, Enrique Grande поднял вопрос: может ли иммунотерапия быть назначена каждому пациенту уже в первой линии? И должна ли она назначаться каждому больному уже в начале лечения?
Однозначного ответа на этот вопрос нет. Эксперты полагают, что есть очень небольшая когорта пациентов, которые могут подождать.
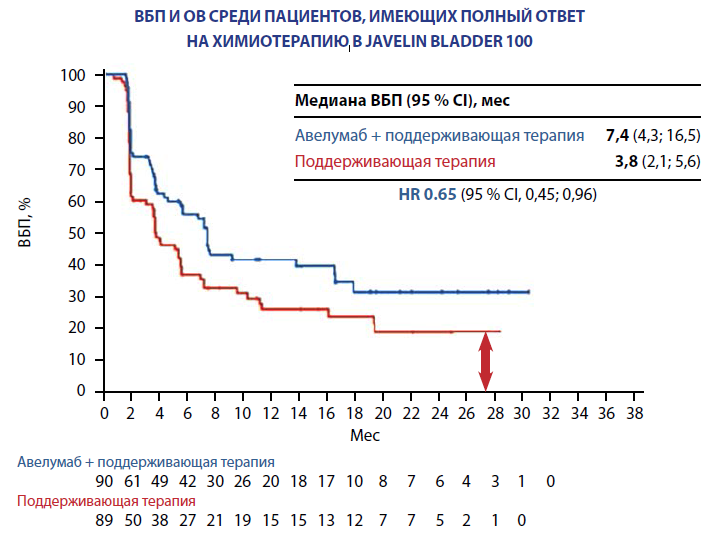
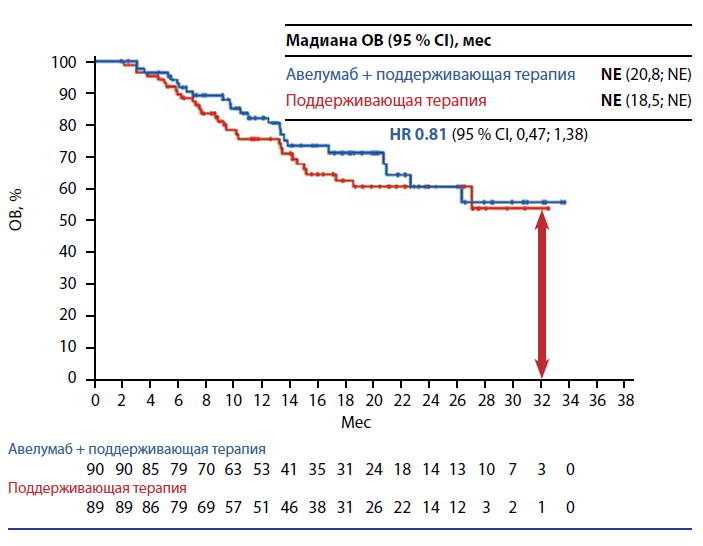
— По исследованию Javelin Bladder 100 проведен подгрупповой анализ среди пациентов, имевших на фоне химиотерапии полный ответ, частичный ответ и стабилизацию, — рассказывает А.С. Калпинский. — Интересно, что в группе с полным ответом при наличии статистически достоверных различий по ВБП (3,8 и 7,4 месяца без применения авелумаба и с его назначением в поддерживающем режиме соответственно) достоверных различий по ОВ в настоящий момент не зарегистрировано. Эти данные пока незрелые, но эта тенденция на отсутствие преимущества в ОВ уже заметна.
А.С. Калпинский отмечает, что несправедливым будет утверждение, что в группе больных, дающих полный ответ на химиотерапию, ингибиторы иммунных контрольных точек не работают. Эти данные говорят лишь о том, что есть пациенты, которые могут некоторое время находиться без лечения и продолжить терапию уже при прогрессии.
— Всем остальным я считаю необходимым назначать иммунотерапию немедленно, — отмечает эксперт.
Аналогичное мнение было высказано и в ходе конгресса EAU.
— Мы знаем, что примерно 10 % пациентов среди тех, кто отвечает на химиотерапию на основе цисплатина, имеют по-настоящему длительную продолжительность жизни, более 80 месяцев, — отметил E. Grande. — Шанс попасть в эту долю несколько больше у пациентов без висцеральных метастазов и с хорошим соматическим статусом, более точно выделить данную категорию больных мы не можем. Но мы видим, что те пациенты, которые имели полный ответ на химиотерапию, действительно не нуждаются в немедленном назначении иммунотерапии.
— Эта группа пациентов требует более глубокого внимания со стороны врачей и исследователей, более тщательного изучения, — подытоживает А.С. Калпинский.
Эксперт отмечает, что в общем-то логично оставить пациента под наблюдением в случае полного ответа на химиотерапию и назначить иммунотерапию только при прогрессии.
— Но если достигнут частичный ответ или стабилизация, совершенно логично выглядит необходимость продолжить лечение, — говорит А.С. Калпинский. — Выглядит странным предложение пациенту, имеющему метастазы, продолжить терапию при усугублении ситуации. Поэтому, учитывая новые возможности терапии, каждому, кто имеет неполный ответ на химиотерапию, должна быть предложена иммунотерапия в поддерживающем режиме.
Основное в концепции поддерживающей терапии — это немедленное назначение иммунотерапии (авелумаба) сразу после завершения химиотерапии тем пациентам, у которых был ответ на проведенную химиотерапию. То есть если атезолизумаб можно назначить одновременно с химиотерапией, то авелумаб — больным, частично или полностью ответившим на химиотерапию препаратами на основе платины. Концепция поддерживающей терапии обоснована результатами исследования Javelin Bladder 100, объединившего 700 пациентов: ОВ через год составила 71,3 % в группе авелумаба и 58,4 % в контрольной группе (медиана ОВ 21,4 по сравнению с 14,3 месяца).
— Существовавшая прежде выжидательная тактика в отношении пациентов, у которых при применении химиотерапии наблюдался частичный ответ или стабилизация, выглядит неполноценно, — отмечает А.С. Калпинский. — Не лечить пациента с метастазами как-то нелепо, поэтому поддерживающая терапия — однозначно обоснованная и востребованная опция.
Незыблемая химиотерапия
А.С. Калпинский подчеркивает, что место химиотерапии остается незыблемым и каким бы ни был выбор врача (иммунотерапия в комбинации с химиотерапией или же в поддерживающем режиме), он должен стремиться провести лечение на основе цисплатина
— В оба протокола, по результатам ко- торых было одобрено применение атезолизумаба в комбинации с химиотерапией и авелумаба в поддерживающем режиме (ImVigor130 и Javelin Bladder 100 соответственно), были включены пациенты, получающие лечение на основе и цисплатина, и карбоплатина, — отмечает А.С. Калпинский. — И хотя в обеих подгруппах эффективность терапии была увеличена, наибольшие преимущества оставались за группой больных, которые получали лечение на основе цисплатина.
Так, в исследовании Javelin Bladder 100 в группе GemCis медиана ОВ составила 25,3 и 16,5 месяца при применении поддерживающего режима авелумаба и без него. В группе GemCar этот показатель составил 19,9 и 12,9 месяца соответственно. Эти данные были доложены P. Grivas c соавт. в 2020 году на ESMO.
Химиотерапия сохраняет свою позицию, в том числе в периоперационном периоде.
— При МИРМП распространение процесса происходит быстрее, поэтому мы не можем гарантировать излечение только проведением ТУР, — подчеркивает А.С. Калпинский. — Химиотерапия остается необходимой перед цистэктомией, она снижает риск смерти и увеличивает показатели 5‑летней выживаемости на 5–8 %. Неоадъювантная химиотерапия приводит к высокой частоте полных ответов (около 30 %), что, однако, не является показанием для отказа от РЦЭ.
Если перед операцией не удалось провести химиотерапию, то при наличии заключения о распространении опухолевого процесса в региональные ЛУ рекомендовано проводить адъювантную химиотерапию.
— Я думаю, что в ближайшем будущем мы достигнем результатов, аналогичных тем, которые получены при лечении почечно-клеточного рака, — отмечает А.С. Калпинский. — Но совершенно точно это будет сделано не благодаря одной какой-то лекарственной опции, а благодаря комплексному вниманию, персонифицированному подходу и комбинированным схемам лечения.
Химиотерапия вообще и на основе цисплатина в частности должна быть использована в том числе для увеличения эффективности иммунотерапии, подытоживает эксперт.
При подготовке материала использованы следующие источники:
- T. Powles, et al., Avelumab Maintenance Therapy for Advanced or Metastatic Urothelial Carcinoma. NEJM, 2020. https://www.nejm.org/doi/full/10.1056/ NEJMoa2002788.
- P. Grivas, S.H. Park, et al. 704MO — Avelumab first-line (1L) maintenance + best supportive care (BSC) vs BSC alone with 1L chemotherapy (CTx) for advanced urothelial carcinoma (UC): Subgroup analyses from JAVELIN Bladder 100.
- NCCN Guidelines Bladder V3 2021.
- M. Galsky et al. Atezolizumab with or without chemotherapy in metastatic urothelial cancer (IMvigor130): a multicentre, randomised, placebo-controlled phase 3 trial. The Lancet, 2020. https://www. t h e l a n c e t . c o m / j o u r n a l s / l a n c e t / a r t i c l e / PIIS0140–6736(20)30230–0/fulltext.
С экспертом и материалами конгресса работала Алла Солодова
Материал предоставлен РООУ
Читайте также
- Иммунитет и модуляция предшественников миелопоэза
- Большие возможности малоинвазивной хирургии
- EAU: новое в диагностике рака мочевого пузыря
- Рак мочевого пузыря и рак почки при беременности
- Осложнения после биопсии, которые можно предотвратить
- Ретроградное и чрескожное удаление камней — единство и борьба противоположностей
- COVID-19 и тестостерон
- Ф.И. Синицын — основатель отечественной андрологии

















