Статьи
Роль врожденных факторов иммунитета плода, микробиома и инфекций матери в формировании перинатальной патологии новорожденных
Защита и иммунный контроль организма эмбриона, плода и новорожденного критически зависят от врожденного иммунитета. Эмбрион развивается из одноклеточной зиготы в бластоцисту и в процессе последовательных митотических делений проходит через гаструляцию и органогенез.
В бластоцисте клетки пространственно перестраиваются, образуя три зародышевых листка: эктодерму, энтодерму и мезодерму. Эти листки дифференцируются в различные типы тканей или органов во время органогенеза. Органогенез начинается на третьей и заканчивается на восьмой неделе гестации (в эмбриональном периоде развития плода).
Эмбриональное кроветворение, представленное примитивными эритроидными и макрофагальными предшественниками, развивается до гаструляции из внезародышевой ткани, то есть в момент старта плацентарного кровообращения. Именно плацента является ключевым посредником, регулирующим способность иммунной системы матери поддерживать локальный гомеостаз в месте имплантации оплодотворенной яйцеклетки. Граница между матерью и плодом представлена трофобластами последнего и децидуальными стромальными клетками, а также, что очень важно, децидуальными иммунными клетками (макрофаги, дендритные клетки и естественные киллеры—NK). От момента имплантации до родов инвазивные трофобласты плода находятся в тесном контакте с децидуальными иммунными клетками матери.
В течение первых 8–12 недель вторичные лимфоидные ткани (тимус, костный мозг) отсутствуют, в связи с чем клетки врожденного иммунитета развиваются на территории желточного мешка и печени плода с минимальным воздействием внешних факторов или патогенов in utero, обеспечивая в первую очередь толерантность развивающегося организма к материнской среде. Именно внутриутробная среда модулирует развитие врожденного иммунитета, что имеет значение для неонатальных исходов.
Клиническое значение фетоматеринского микрохимеризма нельзя переоценить. Именно иммунологическое взаимодействие между плодом и матерью определяет эффективное вынашивание беременности и обеспечивает развитие толерантности к микробиому и хроническим инфекциям будущей мамы. Нарушение взаимоотношений плода и матери способно приводить к осложнениям беременности, ее невынашиванию и преждевременным родам.
В развитии осложнений беременности и родов, рождении детей с низкой и экстремально низкой массой тела и формировании перинатальной патологии новорожденных участвуют не только клетки, но и внеклеточные ростовые факторы и цитокины, продуцируемые иммунными клетками плода. Это значит, что ключевым звеном в паре «мать — плод» является плод, способный с 18‑й недели внутриутробного развития включать в процесс взаимодействий и адаптивный иммунный ответ. Ответ этот еще незрелый и включается в полном объеме, как правило, после родов за счет контактов с внешними патогенами, в связи с чем важнейшее значение во внутриутробных отношениях с мамой имеет врожденный иммунитет плода и ребенка.
ИММУНИТЕТ ПЛОДА
Клетки мезодермы желточного мешка и внезародышевой ткани служат источником формирования эндотелия сосудов, соединительной и кроветворной ткани, первоначально представленной эритроцитами, снабжающими развивающийся эмбрион кислородом. Уже к третьей неделе в желточном мешке появляется кровообращение, вместе с примитивными эритробластами возникают мегакариоциты и макрофаги. С четырех недель беременности кроветворение и иммуногенез развиваются в нескольких независимых источниках: стенке дорсальной аорты и других крупных сосудах, сердце и плаценте (предшественники стволовых клеток, NK, макрофаги, тучные и врожденные лимфоидные клетки — ВЛК).
Предшественники макрофагов имеют организованную дифференцировку по органам и системам (мозг, печень, легкие, эпидермис и т.д.). ВЛК представлены пятью классами: NK, лимфоидные клетки—индукторы формирования лимфатической системы и ее коллекторов — лимфатических узлов (LTi) и три группы ВЛК (ILC‑1, ILC‑2 и ILC‑3), классифицированные на основе факторов транскрипции, необходимых для созревания ВЛК.
В отличие от адаптивных лимфоцитов ВЛК колонизируют участки лимфоидной и барьерной ткани во время развития плода, не подвергаются соматической рекомбинации и не экспрессируют антиген-специфические рецепторы. Помимо формирования лимфоидных органов ВЛК прежде всего инфильтрируют барьерные ткани, выстланные бокаловидными клетками, такие как желудочно-кишечный тракт (ЖКТ), дыхательные пути и кожа, то есть органы, контактирующие с внешней средой. ВЛК считаются тканерезидентными клетками, но недавние исследования показывают, что они могут мигрировать через лимфатическую систему и за счет сброса лимфы через ductus thoracicus попадать в верхнюю полую вену при инфекции и воспалении.
ILC1 зависят от транскрипционных факторов T-box и T-bet, продуцируют гамма-интерферон (INF-γ), белок рецептора интерлейкина 7 (ИЛ‑7) и CD127 у людей и CD200R у мышей; природный рецептор цитотоксичности NKp46 (также известный как NCR1) экспрессируется у обоих видов. Увеличение секреции IFN-γ ILC1 связано с патогенезом воспалительных заболеваний кишечника и ревматоидного артрита.
ILC2 представляют собой наиболее однородный класс ВЛК, зависящих от фактора транскрипции GATA‑3 и продуцирующих цитокины 2‑го типа, главным образом ИЛ‑4, ИЛ‑5, ИЛ‑9, ИЛ‑13. В основном они обнаруживаются в жировой ткани и легких. Повышенная активация ILC2, как предполагается, играет важную роль при аллергических заболеваниях кожи и слизистых. ILC2 участвуют в иммунных ответах на паразитарную инфекцию. У людей они экспрессируют молекулу, гомологичную рецептору хемоаттрактанта в клетках TH2 (CRTH2), и высокие уровни CD161, тогда как большинство мышиных ILC2 экспрессируют ST2 (из семейства рецепторов ИЛ‑1).
Развитие и функция ILC3 зависят исключительно от транскрипционного фактора RORγt (ретиноид-связанный сиротский рецептор γt), в основном эти клетки обнаруживаются в кишечнике и коже. ILC3 как человека, так и мыши могут продуцировать колониестимулирующий фактор гранулоцитов-макрофагов (GM– CSF), ИЛ‑17 и/или ИЛ‑22. У людей можно выделить две основные подгруппы ILC3 на основе экспрессии природного рецептора цитотоксичности NKp44 (также известного как NCR2). Оба типа могут продуцировать ИЛ‑17, участвующий в воспалении, но продукция ИЛ‑22, которая имеет решающее значение для восстановления тканей и гомеостаза, в основном ограничивается NKp44+ ILC3. Увеличение ILC3, продуцирующих ИЛ‑17A, связано с развитием воспалительных заболеваний кишечника, рассеянного склероза и некротического энтероколита (НЭК), в то время как их уменьшение связано с развитием сепсиса.
Обширные исследования посвящены расшифровке роли ILCs в обеспечении поддержания тканевого гомеостаза и иммунной защиты. Показано, что ILCs экспрессируют определенные наборы рецепторов тканеспецифичным образом, что позволяет обнаруживать сигналы, полученные от хозяина (в том числе от аларминов, нейрональных медиаторов, микробов и антигенов диеты). Интеграция этих эндогенных сигналов необходима для поддержания тканевого гомеостаза, поэтому нарушение регуляции ответов ВЛК приводит к воспалению и расстройствам клеточной регуляции и обмена веществ.
ВЛК в основном участвуют в ранней защите от вирусов и бактерий, но их ответ на нарушение регуляции местной продукции провоспалительных цитокинов в жировой ткани приводит к развитию метаболических нарушений и ожирения. ИЛ‑5 и ИЛ‑13, продуцируемые ILC2, индуцируют дифференцировку бокаловидных клеток и рекрутирование эозинофилов, базофилов и тучных клеток, которые участвуют в защите от заражения гельминтами и вирусами, но при отсутствии контроля эти клетки вызывают аллергические реакции и метаболические нарушения. Более того, истощение ILC2 у экспериментальных моделей предполагает роль этих клеток в развитии атопического дерматита и астмы.
ILC3 широко распространены в тканях слизистой оболочки, и было доказано, что NCR2+ ILC3s необходимы для регулирования баланса между комменсальными и патогенными бактериями посредством продукции ИЛ‑22. Напротив, NCR2 ILC3 могут способствовать развитию колита на модели воспалительного заболевания кишечника. Отсутствие иммунодефицита у пациентов с дефицитом ВЛК привело к появлению гипотезы, что ВЛК необязательны при наличии функциональных Т- и B-клеток. Однако недавние исследования подтверждают идею о том, что ВЛК нельзя рассматривать как клетки, обладающие функциями, которые только дублируют таковые адаптивной иммунной системы.
В дополнение к работам, показывающим важную роль клеток LTi в формировании вторичных лимфоидных органов во время эмбриогенеза и в постнатальном развитии кишечных лимфоидных кластеров, недавние исследования также предоставили доказательства того, что подмножества ВЛК экспрессируют множество факторов, которые модулируют адаптивный иммунный ответ в здоровом состоянии и при болезни. В частности, ответ Т-клеток модулируют ILC2 и ILC3. Исследования на мышах показывают, что в здоровом кишечнике ILC3 экспрессируют молекулы главного комплекса гистосовместимости (MHC) класса II, но не экспрессируют костимулирующие молекулы. Следовательно, они ингибируют специфичные для микробиоты реакции Т-клеток, тем самым предотвращая воспаление кишечника. Это объясняет механизмы развития толерантности плода к микробиоте матери. По-видимому, взаимодействие между ILC3 и фолликулярными Т-хелперными клетками (TFH) ограничивает секрецию ИЛ‑4 и продукцию IgA B-лимфоцитами слизистой оболочки.
ВАЖНОЕ ВЗАИМОДЕЙСТВИЕ
Поговорим о взаимодействии врожденной иммунной системы и микробиома матери. Известно, что беременные не стерильны, не стерильны и околоплодные воды, служащие питательной средой для эмбриона. Но почему плод не отвечает на микробиом матери? Убедительный ответ на этот вопрос был дан в недавнем экспериментальном исследовании. Авторы колонизировали стерильных мышей штаммом Escherichia coli, который не мог сохраняться в кишечнике, но эффект воздействия бактерий отсутствовал при родах. А вот потомство наблюдаемых до восьми недель мышей (что сопоставимо со взрослым возрастом человека) имело и сохранило иммунную память ILC‑3. Следовательно, именно благодаря ВЛК ребенок воспринимает материнский микробиом как свой, по существу делает его своим базовым, что сопровождает его в течение жизни. По-видимому, это может касаться и хронических материнских инфекций или бактерионосительства в первом триместре беременности, то есть эти патогены могут восприниматься плодом как свои, несмотря на цитопатическое воздействие на развивающиеся ткани во время органогенеза.
Важно отметить, что у безмикробных мышей функции ILC‑3 нарушены, что сопровождается снижением ILC‑3, продуцирующих ИЛ‑22, то есть функционирование и разнообразие ILC‑3 зависят от микробиома матери.
РОЛЬ В ПАТОГЕНЕЗЕ
Рассмотрим роль ВЛК в патогенезе заболеваний плода и новорожденного. Новорожденные, в частности недоношенные, подвержены развитию НЭК со значительной заболеваемостью и смертностью. Патогенез НЭК предполагает сочетание незрелого иммунного ответа с дисбактериозом или, точнее, с иммунологическим нарушением взаимоотношений плода и микробиоты матери. Роль ILC3 в патогенезе НЭК недавно была изучена в исследованиях как на мышах, так и на людях. Cho и соавт. исследовали роль мышиного ILC3 в патогенезе НЭК и обнаружили в своей модели, что NKp46 (лиганд-активатор нормальных клеток-киллеров) ILC3 увеличен. Авторы также показали, что экспрессия образцов кишечной ткани от детей с НЭК увеличила ИЛ‑17RA (рецептор ИЛ‑17A) и снизила ИЛ‑22 по сравнению со здоровой кишечной тканью от младенцев без НЭК. Исследователи не обнаружили разницы в экспрессии цитокина ИЛ‑17A. Снижение ИЛ‑22 и увеличение NKp46 ILC3 предполагает, что дисбаланс в соотношении подтипов ИЛ‑17A и ИЛ‑22 ILC3 может быть вовлечен в патогенез НЭК.
Babu и соавт. в исследовании на мышах продемонстрировали, что потомство, рожденное от матерей, питавшихся едой с высоким содержанием жиров, было более восприимчиво к НЭК, опосредованной увеличением NKp46 ILC3, которые производили больше ИЛ‑17, что предполагает функциональную гетерогенность ILC3 в неонатальном периоде.
Баланс подтипов ILC3 в неонатальном кишечнике также может быть важен, поскольку трансгенные мыши с повышенной экспрессией ИЛ‑23 и последующим увеличением ILC3 имеют тяжелые проявления воспаления кишечника, что приводит к неонатальной смерти. В совокупности эти данные указывают на роль ILC3 в НЭК, но их следует воспринимать с осторожностью, учитывая, что в исследовании использовалась иммуногистохимия тканей мышей, залитых парафином, а мышиные модели НЭК не являются наилучшей презентацией человеческого заболевания. Необходимы дальнейшие исследования с использованием свежей ткани пациентов с НЭК, включающие характеристику ILC3 и других типов иммунных клеток, которые были вовлечены в НЭК, включая адаптивные Т-клетки.
ILC3 также может играть важную роль в восприимчивости к постнатальному сепсису, связанному с нарушением микробиома матери или недоношенных детей антибиотиками. У новорожденных мышей восприимчивость к сепсису повышается после воздействия антибиотиков даже временно — в результате снижения ILC3, продуцирующего ИЛ‑17. Кроме того, в мышиной модели неонатальной пневмонии уровень ILC3, продуцирующего ИЛ‑22, был снижен в легких потомства, рожденного от матерей, принимавших антибиотики широкого спектра действия за 5 дней до родов, а потомство также было более восприимчиво к пневмонии, вызванной S. pneumoniae. После снижения уровень ILC3, продуцирующего ИЛ‑22, частично вернулся к норме при восстановлении потомства с нормальной бактериальной колонизацией в постнатальном периоде.
Бронхолегочная дисплазия (БЛД) — это хроническое респираторное заболевание, которое возникает у недоношенных в результате преждевременных родов, воздействия кислорода и искусственной вентиляции легких. В жидкости бронхоальвеолярного лаважа уровень ILC3 снижен у новорожденных с БЛД. У людей с мутациями RORC и нарушенной функцией ILC3 наблюдается хроническая инфекция, вызванная грибами Candida, а недоношенные имеют повышенную восприимчивость к грибковому сепсису, что также заставляет предполагать, что у недоношенных может быть нарушена функция ILC3.
Недавно дефекты ILCs были обнаружены в плацентах матерей после преждевременных родов. В исследовании, в котором оценивались децидуальные лейкоциты из плацент женщин после преждевременных и срочных родов, доля ILC2 и ILC3 была выше у мам после преждевременных родов. Авторы также обнаружили, что экспрессия цитокинов ILC3 ИЛ‑22 и ИЛ‑17A также увеличена у женщин со спонтанными преждевременными родами.
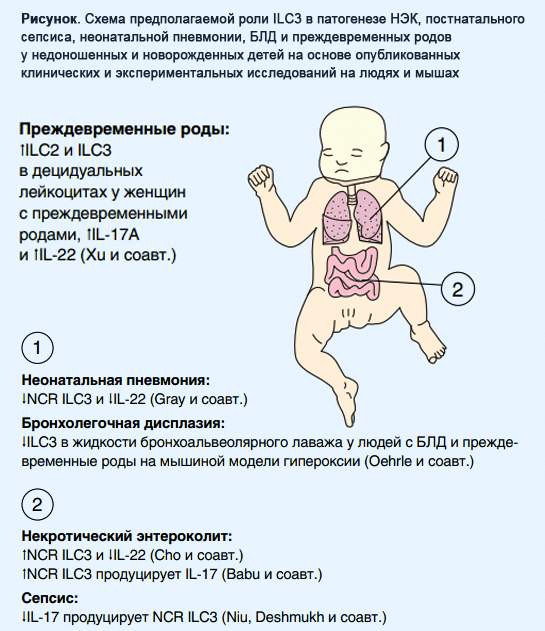
Эти результаты интригуют и требуют уточнения: каков материнский или фетальный источник ILC3 и какова потенциальная роль этих клеток в патогенезе преждевременных родов, частота которых не уменьшается, в том числе в развитых странах? Кратко изменения в подтипах ILC3, экстраполированных из неонатальных исследований, рассмотренных в статье, проиллюстрированы на рисунке.
ВЗГЛЯД В БУДУЩЕЕ
Мы только начинаем осознавать важность ВЛК, и прежде всего ILC3, в патогенезе критических заболеваний, связанных не только с недоношенными, но и с доношенными новорожденными. Функциональная гетерогенность ILC3 у этой категории пациентов нуждается в дальнейшем определении и изучении механизмов иммунного контроля с участием врожденных дефектов иммунитета и накладывающегося на него приобретенного иммунитета. Несмотря на сходство человеческого и мышиного ILC3, остаются принципиальные различия, одно из самых ярких из них — наличие TLR на человеческом ILC3. Кроме того, функция подтипов ILC3 у плода в неонатальных и взрослых моделях, по-видимому, различается. Также традиционно считается, что NCR ILC3 в первую очередь продуцируют цитокин ИЛ-22, но у новорожденных мышей этот подтип, по-видимому, имеет значительную продукцию ИЛ-17A, связанную с восприимчивостью к НЭК и сепсису. Бремя НЭК, БЛД и сепсиса у недоношенных значительно, поэтому потенциал терапевтических вмешательств, нацеленных на функцию ILC3, для улучшения результатов является привлекательным. Механизмы, определяющие, как материнский микробиом и диета модулируют ILC3 плода,— это еще одна возможность, способная привести к достижению терапевтических целей.
Будущие направления исследований в области врожденного иммунитета плода и новорожденного должны включать:
а) разработку и внедрение в практику тестов, характеризующих функциональную активность факторов врожденного иммунитета у плода, новорожденных и детей раннего возраста в норме и при патологии;
б) иммуногистохимический и молекулярно-генетический анализ биоптата свежей кишечной ткани недоношенных и новорожденных при воспалительных состояниях (например, НЭК) для определения онтогенеза ILC3 и выявления подтипов ILC3, присутствующих у этой группы больных;
в) уточнение клеточного состава врожденных иммунных факторов у абортируемых по медицинским показаниям плодов с акцентом на материнские экологические, микробные и диетические факторы, которые влияют на количество и функциональные показатели линии ВЛК; г) постнатальные исследования ВЛК у недоношенных и доношенных новорожденных, которые помогут идентифицировать пути вовлечения и приверженность линии различных ВЛК в неонатальном периоде, включая изучение того, как местные тканевые факторы и микробная колонизация направляют гетерогенность и функцию ВЛК.
Учитывая множащиеся доказательства важности ВЛК в неонатальном периоде, эти исследования имеют потенциал выявления уникальных микробных, диетических и фармакологических воздействий для медицинского контроля врожденного иммунитета новорожденных путем воздействия на беременных и кормящих женщин или недоношенных детей.
Список литературы находится в редакции

















