Статьи
Статистика: от теории — к реальности
В прошлых выпусках «Современной Кардиологии» мы в деталях разбирали описательную статистику — способы передать характеристики данных максимально информативно, при этом не загружая читателя массивами «сырых» цифр. Но одно дело — просто описать данные, и совсем другое — получить из них какие-то совершенно новые знания, например о взаимосвязи двух переменных (условно говоря, влияние приема статина на уровень липопротеинов низкой плотности). Обычно именно это и хотят узнать от статистика исследователи и читатели статей. Методы установления таких фактов — в сегодняшней и дальнейших публикациях нашей рубрики. Но прежде чем двинуться дальше, нам придется слегка отойти от математики и поговорить о том, как вообще исследователь получает нужные данные.
Интуитивно понятно, что просто взяв 20 пациентов из очереди у кабинета и раздав им таблетки, какие-то сведения собрать можно, но будет ли в них содержаться достоверная информация? Чтобы подтвердить некое предположение, в первую очередь надо грамотно спланировать исследование, иначе говоря, сформулировать его дизайн. Почти все наверняка встречали в статьях устойчивые словосочетания по типу «проспективное рандомизированное контролируемое тройное слепое». Звучит очень сложно, но мы начнем наше обсуждение с самых простых вариантов и постараемся в итоге понять, что же все это значит.
Держа в голове наш пример со статинами, давайте попробуем спланировать свое исследование. Для начала у нас есть фундаментальный выбор между наблюдением и экспериментом. Разница между ними довольно очевидна, но все же мы ее обсудим. При наблюдении исследователь не вносит никаких дополнительных факторов в изучаемое явление. Такая методика хороша для обнаружения естественных зависимостей между разными факторами и для исследований, в которых выявляется частота возникновения разных заболеваний и факторы риска их развития. Классическим примером такого исследования, например, является Фремингемское. В его рамках уже более полувека ведется наблюдение за несколькими тысячами жителей одного города для выявления таких знакомых всем факторов риска развития сердечно- сосудистых заболеваний, как курение, повышенное артериальное давление, высокий уровень ЛПНП и низкий уровень физической активности. Конечно, в случае наблюдательного исследования рациональнее всего минимизировать влияние наблюдателя на испытуемых. Так, просить пациентов каждый день приходить на прием для измерения давления — не лучшая идея, способная исказить получаемый результат. А вот обучить их технике самостоятельных измерений и попросить делать это раз в неделю (для здоровых людей) — вполне приемлемо. Такая практика и устранит возможность влияния «гипертонии белого халата», и не нарушит привычного образа жизни наблюдаемых.
В экспериментальном исследовании мы, наоборот, специально вносим новый фактор, влияние которого хотим изучить. Этим фактором может быть способ лечения, изменение образа жизни, техника проведения операции — все что угодно. Практически всегда клинические исследования, которые требуются для регистрации новых препаратов, являются экспериментальными.
Так и наше гипотетическое исследование статина должно, конечно, стать экспериментом: мы ведь хотим проверить, как именно данное лекарство влияет на ЛПНП у пациентов. При этом в идеальной ситуации мы хотим добавить только один фактор и ничего больше. На первый взгляд, это довольно просто, но проблемы, как всегда, кроются в деталях. Так, когда мы даем человеку лекарство в таблетке, на него влияет не только действующее вещество, но и сам факт того, что его лечит опытный врач, да еще и новым, суперэффективным средством. И когда ему станет лучше, исследователю будет довольно сложно понять, что именно все-таки сработало. Собственно, здесь мы описали очень известный эффект плацебо, но и кроме него в экспериментальном исследовании может быть много подводных камней. Мы вернемся к этим проблемам и способам их решения чуть позже, а пока обсудим еще одну разницу между экспериментальными и наблюдательными исследованиями.
В эксперименте мы будем наблюдать за событиями, которые произошли после нашего вмешательства. То есть мы начали лечить пациента новым лекарством и проверяем, к какому результату через неделю, месяц или несколько лет это привело. В наблюдательном исследовании у нас есть выбор — мы можем пойти в архив и по историям болезни описать, что же происходило с интересующими нас пациентами. Либо мы можем выбрать группу и наблюдать за ней в течение какого-то периода времени. Таким образом, направление наблюдения — это еще один важный элемент его дизайна. Наблюдение с «откатом назад» называется ретроспективным, «вперед идущее» — проспективным исследованием.
Проспективное исследование обычно подразумевает группу пациентов или когорту, за которыми наблюдают «в ожидании» появления заболевания или, наоборот, проявления эффекта от получаемого лечения. В данном случае ученый получает больший объем информации и лучший контроль над ходом процесса. Расплата за такие преимущества — более высокая затратность такого способа.
Поговорив о наблюдательных исследованиях, вернемся к экспериментам и проблеме плацебо, о которой мы уже упоминали. Наша задача заключается в том, чтобы минимизировать влияние всех сопутствующих факторов, которые помешают получить нам желаемый ответ: как влияет новый статин на уровень ЛПНП? Мы уже задумались о том, что сам факт лечения, независимо от лекарства, может влиять на состояние пациента, но немного забыли о том, что даже без лечения могут произойти какие-то изменения. И конечно, отнести эти случайные изменения, которые мы не можем контролировать, к экспериментальному вмешательству — совсем неправильно.
При этой проблеме нас выручают различные сравнения. Так, чтобы понять, было ли изменение ЛПНП вызвано препаратом или случайными факторами, можно сравнить две группы пациентов: первую, в которой пациенты получали препарат, и вторую, в которой не было никакого гиполипидемического лечения. Если изменения, какими бы они ни были, в обеих группах будут сопоставимы, то, скорее всего, препарат тут ни при чем.
С эффектом плацебо ситуация очень похожа: нам также потребуется вторая группа пациентов для сравнения, но теперь группа сравнения будет все-таки получать таблетки, хоть и без действующего вещества. Таким образом в исследовании «обманывают» эффект плацебо, позволяя ему в равной степени проявиться в обеих группах и не влиять на разницу между ними. Этот дизайн сравнения хорош тем, что позволяет максимально показать действенность лекарства. Однако у него тоже есть очевидная проблема: часть пациентов вынуждена заведомо получать неработающее лекарство! Это, согласитесь, не очень этично. Поэтому чаще используется сравнение не с плацебо, а с так называемой стандартной терапией, то есть, например, со старым, уже известным статином. Такие исследования и будут называть «контролируемыми».
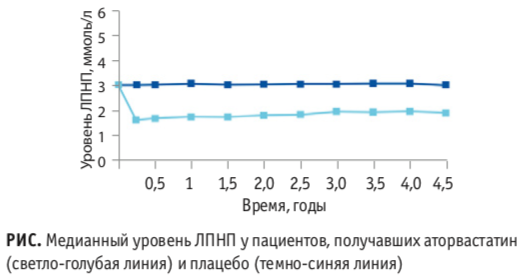
Давайте в качестве наглядного примера обсудим исследование CARDS, в котором оценивалось влияние 10 мг аторвастатина на риски развития сердечно-сосудистых событий у пациентов с сахарным диабетом 2 типа (СД2). Для этого в исследование было включено более чем три тысячи пациентов. Поскольку задачей работы была оценка влияния одного фактора — аторвастатина — то, разумеется, был выбран экспериментальный проспективный дизайн. Касательно группы сравнения, на тот период времени у организаторов исследования не было убедительных данных в пользу необходимости и эффективности применения статинов у пациентов с СД2, поэтому применение плацебо было допустимо и не предполагало заведомой «дискриминации» части пациентов.
В результате исследование было прекращено досрочно из-за значительной разницы в эффективности между аторвастатином и плацебо. Исследователи получили убедительные доказательства преимущества препарата и перестали подвергать ненужному риску лишенных его испытуемых. Из полученных результатов мы обратим внимание на уровень ЛПНП у пациентов в обеих группах, поскольку он выражен как медиана, которую мы уже хорошо знаем как показатель в описательной статистике.
На графике даже не вооруженным статистикой глазом видно, что аторвастатин снижал ЛПНП на 40 % относительно плацебо. Достаточно убедительное подтверждение корректного выбора дизайна в исследовании. Кроме очевидного вывода об эффективности аторвастатина, он позволяет утвердиться во мнении, что проводить дальнейшие исследования, сравнивая этот препарат с плацебо — скорее всего, излишне, ведь мы уже знаем о его превосходящей эффективности.
Иные примеры, когда сравнения проводились уже не с плацебо, мы рассмотрим в следующем выпуске, вместе с другими параметрами дизайна — «ослеплением» и рандомизацией. А кроме того, постараемся понять, чем знание о дизайнах исследования может помочь врачу, который не ведет самостоятельную исследовательскую работу, а только хочет делать корректные выводы о применимости опубликованных результатов для своей практической деятельности.


















