Статьи
Таргетная терапия детей с мультиморбидным атопическим фенотипом
 В мире наблюдается неинфекционная эпидемия аллергических заболеваний (АЗ). Для борьбы с ними разрабатываются генно-инженерные биологические препараты (ГИБП), воздействующие на различные таргетные точки аллергического воспаления и способные привести к достижению контроля над АЗ. Терапия ГИБП открыла новую эру в лечении больных с мультиморбидным атопическим фенотипом.
В мире наблюдается неинфекционная эпидемия аллергических заболеваний (АЗ). Для борьбы с ними разрабатываются генно-инженерные биологические препараты (ГИБП), воздействующие на различные таргетные точки аллергического воспаления и способные привести к достижению контроля над АЗ. Терапия ГИБП открыла новую эру в лечении больных с мультиморбидным атопическим фенотипом.
ПОПАДАНИЕ В ЦЕЛЬ
В мире наблюдается неинфекционная эпидемия аллергических заболеваний (АЗ). Для борьбы с ними разрабатываются генно-инженерные биологические препараты (ГИБП), воздействующие на различные таргетные точки аллергического воспаления и способные привести к достижению контроля над АЗ. Терапия ГИБП открыла новую эру в лечении больных с мультиморбидным атопическим фенотипом.
- к иммуноглобулину Е (омализумаб);
- антагонист альфа-субъединицы рецептора интерлейкинов (П) 4 и 13 (дупи- лумаб);
- к П-5 (меполизумаб), анти-Т5БР-МАТ (тезепелумаб), блокатор малых молекул — селективный обратимый ингибитор Янус-киназы (упадацитиниб) и другие.
Одна из важнейших задач детской аллергологии и иммунологии — добиться максимально раннего достижения полного и долгосрочного контроля над АЗ с использованием новых медицинских
технологий, в том числе МАТ. Рассмотрим возможности ее реализации на примере АтД как одного из самых распространенных хронических воспалительных заболеваний кожи у детей во всем мире. АтД охватывает до 20 % детской популяции, причем у 80 % пациентов манифестация болезни отмечается в первые годы жизни.
Уточнение особенностей этиологии, патогенеза и клинических проявлений привело к современному пониманию АтД как мультифакторного системного генетически детерминированного воспалительного заболевания кожи с признаками полиорганной патологии, характеризующегося зудом, хроническим рецидивирующим течением, возрастными особенностями локализации и морфологии очагов поражения. Заболевание характеризуется повторными эпизодами обострений и ремиссий, а хроническое воспаление кожи при АтД сопровождается интенсивным мучительным зудом, что негативно сказывается на качестве жизни ребенка и всей семьи в целом.
АТОПИЧЕСКИЙ МАРШ
Хотя в последние десятилетия появилось много новых опций лечения детей с АтД, актуальной проблемой остается отсутствие контроля над заболеванием у значительного числа из них. По мнению экспертов, АтД, как и пищевая аллергия (ПА), представляет собой этап так называемого атопического марша, который при отсутствии или неэффективности профилактики и лечения приводит к расширению спектра сенсибилизации, реализации следующих закономерных шагов патологического процесса и развитию таких заболеваний, как БА и АР. Учитывая сходство их патогенетических механизмов и идентичность медиаторов, по прогнозам, доля детей с АтД, у которых в будущем сформируется мультиморбидный фенотип без возможности излечиться, доходит до 71,3 %.
К факторам риска развития атопического марша (атопической мультиморбидности) у детей с АтД относятся тяжесть, длительность и возраст дебюта болезни, отягощенная наследственность по атопии, мутация в гене филаггрина FLG, поливалентная сенсибилизация, проживание в городе.
АтД характеризуется клиническими фенотипами с разными траекториями течения. Часть пациентов не реагируют или отвечают не полностью на доступные методы лечения, что создает риск побочных эффектов у больных с плохим клиническим ответом при более частом и длительном применении топических противовоспалительных препаратов высокой активности (например, глюкокортикоидов, сокращенно — ГК).
ОПТИМАЛЬНЫЙ ВЫБОР
А можно ли предотвратить развитие атопического марша? Да, при оптимальном индивидуальном выборе ГИБП, который зависит от особенностей проявлений мультиморбидного атопического фенотипа конкретного пациента, а также от прогноза эффективности, безопасности и оптимальной длительности курса лечения. Однако эти вопросы у детей требуют дополнительного изучения.
Дупилумаб — один из ведущих ГИБП в педиатрической практике — применяется у детей от 6 месяцев и старше со среднетяжелым и тяжелым АтД при недостаточном ответе на терапию топическими препаратами или когда они не рекомендуются. Данный ГИБП может использоваться:
- в монотерапии или одновременно с топическими ГК, а также для дополнительной поддерживающей терапии БА среднетяжелого и тяжелого течения у детей от 6 лет и старше с эозинофильным фенотипом или у больных с гормонозависимой БА, получающих пероральные ГК;
- для лечения ЭоЭ у пациентов 12 лет и старше;
- в качестве дополнительной поддерживающей терапии взрослых больных с плохо контролируемым тяжелым хроническим полипозным риносинуситом.
Эффективность лечения АтД, характеризующаяся достижением EASI-75 и EASI-90, на фоне терапии дупилумабом регистрировалась в 44–65 % и 30–51 % случаев соответственно, оставляя некоторых пациентов без улучшения.
Сегодня широко обсуждаются возможный болезнь-модифицирующий эффект дупилумаба и его способность предотвращать прогрессирование атопического марша, то есть формирование мультиморбидного фенотипа. Так, например, T.L. Lin и соавт. провели ретроспективный когортный анализ данных 4384 пациентов с АтД младше 18 лет, разделив их на две группы: лечения дупилумабом и стандартной терапии (по 2192 больных в каждой). Первичной конечной точкой была выбрана прогрессия атопического марша (дебют БА или АР). Его кумулятивная частота за 3 года наблюдения в группе дупилумаба оказалась значимо ниже, чем в контрольной группе (20,09 % против 27,22 %; p <0,001).
Также отмечалось снижение риска прогрессирования атопического марша, дебюта БА и АР (на 32, 40 и 31 % соответственно). Однако вероятность развития БА снизилась только у детей младше 6 лет: отношение шансов (ОШ) — 0,427; 95 % доверительного интервала (ДИ) — 0,247–0,738, а для детей школьного возраста и подростков данный эффект не был продемонстрирован. Авторы работы пришли к выводу, что дупилумаб может влиять на механизмы развития атопического марша, но для подтверждения его способности модифицировать заболевание необходимы дополнительные исследования.
В рекомендациях Европейской академии аллергологии и клинической иммунологии (European Academy of Allergy and Clinical Immunology—EAACI) отмечается, что в случае подтверждения болезньмодифицирующего эффекта дупилумаб можно рассматривать для лечения легкой формы АтД и даже для первичной профилактики у пациентов с высоким риском его развития.
Выбор терапевтической тактики ведения пациента с АтД основывается на результатах оценки характера течения патологического процесса. Для комплексной количественной оценки степени тяжести заболевания могут использоваться специальные шкалы:
- SCORAD (Scoring Atopic Dermatitis — шкала выраженности АтД), которая учитывает распространенность поражения кожи, интенсивность клинических проявлений и выраженность зуда;
- EASI (Eczema Area and Severity Index)— индекс распространенности и тяжести экземы, основанный на определении суммы показателей выраженности эритемы, инфильтрации, экскориаций и лихенификации с учетом площади поражения кожи;
- CDLQI (Children’s Dermatology Life Quality Index — индекс качества жизни детей с заболеваниями кожи) — вопросник, позволяющий оценить степень влияния АтД на качество жизни детей старше 4 лет.
При разработке новых терапевтических средств для лечения АтД основное внимание уделяется купированию симптомов и предотвращению обострений, однако зачастую без должного внимания остаются сопутствующие атопические заболевания (БА, АР и ПА). Кроме того, налицо дефицит клинических и лабораторных биомаркеров для выявления больных с высоким риском развития атопического марша.
СОБСТВЕННЫЕ ДАННЫЕ
В 2024 году на базе многопрофильного педиатрического дневного стационара КДЦ для детей НИИ педиатрии и охраны здоровья детей НКЦ № 2 «РНЦХ имени академика Б.В. Петровского» (Москва) началось проспективное исследование факторов прогнозирования индивидуального оптимального ответа на таргетную терапию детей с мультиморбидным атопическим фенотипом. Комплексно обследованы 15 больных с медианой возраста 13,3 года (Q1–5,1; Q3–15,9; min — 1,2, max — 17,2).
В связи с персистирующим тяжелым или среднетяжелым течением АтД и сохранением симптомов, несмотря на применение стандартной терапии топическими ГК, а также комбинаций препаратов, всем пациентам назначена циклическая таргетная терапия дупилумабом. Дозу подбирали в соответствии с инструкцией в зависимости от возраста и массы тела пациента. Тяжесть течения АтД оценивалась с использованием стандартных шкал (SCORAD, EASI) перед началом терапии, а также каждые 4 недели. Оценка качества жизни детей старше четырех лет проводилась в баллах по стандартизированному вопроснику CDLQI перед стартом лечения, а также каждые 4 недели (на 4, 8, 12 и 16-й неделях терапии). Сумма баллов находилась в пределах от 0 до 30: чем выше, тем сильнее заболевание влияет на жизнь ребенка.
Из 15 обследованных мальчиков было 10 (67 %). Медиана массы тела составила 46 кг (19; 52), роста — 150 см (109; 165).
Оценивались наследственные и экспосомальные факторы риска развития АЗ. Отягощенная наследственность по АЗ обнаружилась у большинства обследованных — 13 (87 %), из них у 6 (46 %) — по линии матери, 4 (31 %) — по линии отца, у 2 (23 %) детей — по линии обоих родителей. У 8 (53 %) пациентов наследственность была отягощена по поллинозу, предрасположенность к аллергии на животных выявлена у 7 (47 %) пациентов. Животные присутствовали у 4 (27 %) детей; по одному пациенту имели кошку, собаку, шиншиллу и ящерицу. У 10 (67 %) детей были симптомы риноконъюнктивального синдрома при контакте с кошкой, у 5 (33 %)—при контакте с собакой, у 3 (20 %) — симптомы БА при контакте с кошкой, у 2 (13 %) — при контакте с собакой, у 6 (40 %) — кожные проявления аллергии при контакте с кошкой и собакой.
При оценке ситуации с курением в семье выяснилось, что отцы чаще регулярно курили в период беременности матери и первые 2 года жизни ребенка (табл. 1).

Большинство детей вскармливались грудью на первом году жизни, медиана возраста введения прикорма составила 6 (5; 6) месяцев. 27 % мам получали антибактериальную терапию (АБТ) во время беременности, а большинство детей (60 %) — на первом году жизни. У большинства из них (87 %) АтД дебютировал в возрасте до 6 месяцев. Все дети имели мультиморбидный атопический фенотип (2 и более АЗ).
АтД тяжелого течения был диагностирован у 7 (47 %), среднетяжелого— у 8 (53 %), сезонный аллергический ринит (САР) как проявление поллиноза— у 11 (73 %) пациентов. При этом 9 (60 %) детей жаловались на сезонные проявления аллергии весной, двое — на симптомы поллиноза в июне и июле, пятеро — в июле и августе. Больше чем у половины, а именно у 8 (53 %) пациентов, была сопутствующая БА среднетяжелого и легкого течения — 2 (25 %) и 6 (75 %) детей соответственно. Большинство больных 12 (80 %) страдали круглогодичным аллергическим ринитом (КАР). ПА на какой-либо продукт из большой восьмерки аллергенов диагностирована у 12 (80 %) участников исследования, перекрестная ПА на продукты растительного происхождения — у 9 (60 %), хроническая крапивница — у 1 (7 %), анафилаксия — у 3 (20 %) детей. В таблице 2 представлены различные сочетания диагнозов у пациентов с мультиморбидным атопическим фенотипом.

При оценке тяжести течения АтД у детей младше 7 лет медианное значение по шкале SCORAD-TIS составило 49 баллов (37; 59), средний балл — 46 с отклонением ± 15, что указывает на умеренную выраженность симптомов с диапазоном значений от 26 до 62 баллов. 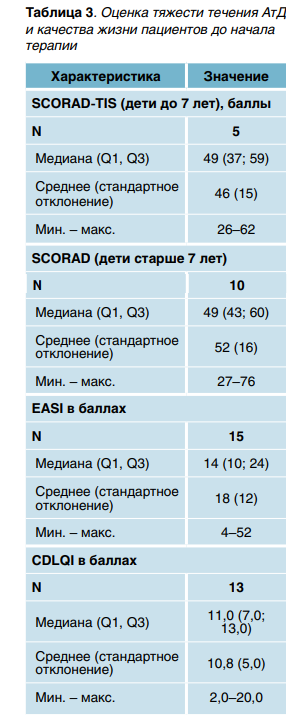
У детей старше 7 лет медиана по шкале SCORAD равнялась 49 (43; 60), а среднее — 52 с отклонением ± 16, что говорит о более выраженных симптомах с разбросом оценок от 27 до 76 баллов. При оценке по шкале EASI медиана составила 14 (10; 24) баллов, что также указывает на умеренно выраженные симптомы АтД (табл. 3).
При определении степени воздействия заболевания на повседневную активность и психологическое состояние участников исследования с использованием оценочной шкалы CDLQI медианное значение показателя составило 11,0 (7; 13) баллов, то есть большинство пациентов оценивали влияние заболевания как умеренное. Разброс баллов находился в пределах от 2,0 до 20,0, что охватывает спектр от минимального до сильного воздействия заболевания на повседневную жизнь детей. Для определения характера ответа на таргетную терапию дупилумабом в разных временных точках проанализирована динамика показателей тяжести течения АтД по шкалам SCORAD, EASI и качества жизни — по СDLQI.
ОЦЕНКА ЭФФЕКТИВНОСТИ
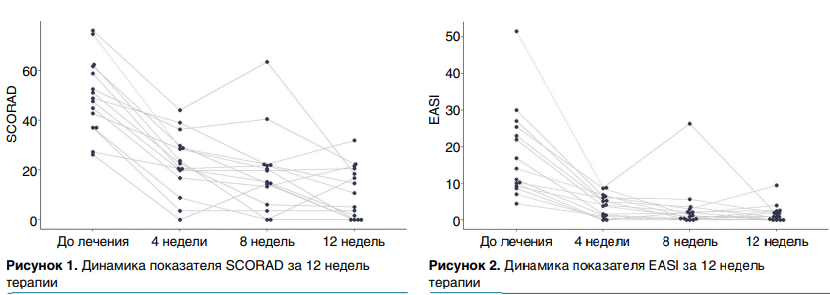
Оценка эффективности применения дупилумаба у детей с мультиморбидным атопическим фенотипом в отношении динамики показателя SCORAD (среднее ± стандартное отклонение) продемонстрировала значительное улучшение состояния пациентов на протяжении 12 недель лечения (рис. 1). Средний балл, до начала терапии составлявший 50 ± 15, уже к 4-й неделе лечения снизился до 23 ± 12, на 8-й — до 18 ± 16, указывая на заметное уменьшение симптомов, а к 12-й—до 11 ± 10, что подтверждает устойчивую эффективность лечения и значительное облегчение симптомов АтД. Значение p-value <0,001, рассчитанное по парному t-тесту, подтверждает статистическую значимость изменений после 12 недель терапии. Через 4 недели терапии оценка SCORAD снизились в среднем на 55,6 %, к 8-й неделе—на 63,5 % и к 12-й неделе— на 79,9 % относительно исходного уровня. Диапазон изменений варьировал от 19,9 до 100 % на 4-й неделе, от 16,6 до 100 % на 8-й и от 51,8 до 100 % на 12-й, что говорит о значительном и прогрессирующем уменьшении тяжести симптомов на протяжении всего периода лечения.
SCORAD-50 большинство пациентов (67 %) добились уже к 4-й неделе лечения, еще двое (13 %) — к 8-й и трое (20 %) — к 12-й неделе. Все пациенты достигли этого уровня улучшения к концу исследования. Уровень SCORAD-75 наблюдался у 20 % пациентов к 4-й неделе, у 20 % — к 8-й и у 27 % — к 12-й, тогда как 33 % не достигли снижения баллов SCORAD на 75 % к 12-й неделе терапии.
Оценка динамики результатов по шкале EASI (медиана, интерквартильный размах) также показывает значительное улучшение состояния пациентов (рис. 2). До лечения медиана составляла 14 (10; 24) баллов, к 4-й неделе значение снизилось до 4 (1; 6), на 8-й — до 1 (0; 3), и к 12-й медиана оставалась на уровне 1 (0; 2) балла. Это свидетельствует об устойчивом и прогрессирующем снижении симптомов на протяжении всего курса лечения. Значение p-value <0,001 подтверждает статистическую значимость разницы между исходным состоянием и результатами после 12 недель терапии.
Изменение оценки по EASI по сравнению с началом лечения таково: среднее снижение составило 77,7 % уже к 4-й неделе терапии, 86,2 % — к 8-й и 90,2 % — к 12-й. Диапазон изменений колебался от 41,2 до 100 % на 4-й неделе, от 45,1 до 100 % — на 8-й и от 68,7 до 100 % — на 12-й, что также указывает на устойчивое снижение выраженности соответствующих симптомов по ходу лечения.
Результата EASI-50 достигли 93 % пациентов уже к 4-й неделе лечения, и еще один (6,7 %) пришел к этому результату к 12-й неделе; ни один из пациентов не остался без улучшения. К EASI-75 пришли 73 % детей к 4-й неделе, еще 20 % достигли этого уровня к 8-й и один (6,7 %) — к 12-й. Все пациенты достигли уменьшения EASI на 75 % в течение периода наблюдения.
При оценке динамики по шкале CDLQI у 13 детей старше четырех лет медиана баллов до лечения составила 11 (7; 13), к 4-й неделе она снизилась до 2 (2; 4), а на 8-й и на 12-й осталась на уровне 2 (1; 6) и 2 (1; 4) (рис. 3). Эти значения демонстрируют устойчивое улучшение качества жизни больных после начала терапии с наиболее значительным снижением к 4-й неделе и поддержанием скорректированных показателей до конца наблюдения. При этом значение p-value = 0,003, рассчитанное с использованием критерия ранговых знаков Уилкоксона с поправкой на непрерывность, подтверждает статистическую значимость улучшений к 12-й неделе на фоне таргетной терапии.
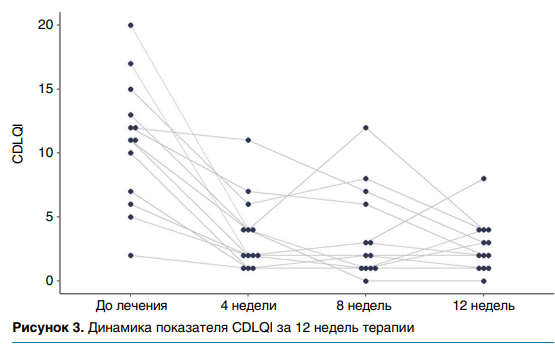
На 4-й неделе среднее снижение показателя CDLQI составило 65,02 % (диапазон— 8,3–90 %), на 8-й неделе—64,66 % (0–100 %), а к 12-й неделе — 67,95 % (33,3–100 %). Все это также демонстрирует устойчивое улучшение качества жизни пациентов в течение всего курса терапии.
Снижение на 50% по показателю CDLQI было достигнуто у большинства (85 %) пациентов к 4-й неделе, еще по одному ребенку (7,7 %) добились этого уровня на 8-й и 12-й неделях, при этом улучшение произошло у всех. Снижение показателя на 75 % наблюдалось у 38 % пациентов на 4-й неделе, у 23 % — на 8-й и у 15 % — к 12-й; но к этому сроку не достигли соответствующего уровня 23 % пациентов.
Реакции в месте инъекции дупилумаба отметили 3 пациента (13 %): двоих (14 %) беспокоила болезненность в месте инъекции, по одному (6,7 %) отмечали зуд и конъюнктивит за 12 недель терапии. Эритемы и отека в месте введения не было.
В результате проведенного исследования определена эффективность таргетной терапии дупилумабом у 15 детей с АтД среднетяжелого и тяжелого течения в сочетании с другими аллергическими болезнями, установлено среднее время ответа на таргетную терапию данным препаратом, проанализирована ее безопасность для детей с мультиморбидным атопическим фенотипом. Лечение дупилумабом значительно улучшило как клинические исходы, так и качество жизни педиатрических пациентов со среднетяжелым и тяжелым АтД, причем даже у детей с атопической мультиморбидностью. Профиль безопасности был благоприятным с небольшим количеством побочных эффектов. Планируется продолжить исследование для оптимизации стратегий лечения, идентификации предикторов и сроков оптимального ответа на терапию при среднетяжелой и тяжелой сочетанной аллергической патологии у детей, а также для формирования модели прогнозирования ответа педиатрического пациента с мультиморбидным фенотипом на таргетную терапию.
Список литературы находится в редакции

















