Статьи
Сахарный диабет и COVID-19: время перемен на поле битвы
НА ПЕРЕДОВЫХ РУБЕЖАХ
Татьяна Николаевна сообщила, что на сегодняшний день работа всех отделений ГБУЗ «ГКБ № 52» Москвы по-прежнему реорганизована для лечения пациентов с COVID-19. Перепрофилирование больницы произошло в феврале 2020 года. Дополнительно были развернуты четыре корпуса в красной зоне и организованы два временных госпиталя, где применяются инновационные методы лечения и реабилитации пациентов—новые препараты, моноклональные антитела для групп риска, терапевтический плазмообмен, терапия гелием и др. Наличие на территории больницы профильных центров аллергологии, ревматологии, эндокринологии, нефрологии позволило успешно экстраполировать и применить в кратчайшие сроки опыт лечения системных заболеваний с помощью таргетных и биологических препаратов у пациентов с COVID-19.
Отделение эндокринологии также было перепрофилировано и оказывало помощь преимущественно пациентам с новой коронавирусной инфекцией (НКИ) и эндокринной патологией. С 2020 года в больнице было внедрено лечение практически всеми препаратами против НКИ —от противовирусных средств до моноклональных антител, показанных для ранней профилактики цитокинового шторма больным из групп высокого риска, к которым в числе прочих относятся и пациенты с сахарным диабетом (СД). В период пандемии абсолютное большинство больных отделения эндокринологии ГКБ № 52 составляли пациенты с СД 2 типа. Самым непростым периодом в жизни отделения последних 3 лет спикер назвала циркуляцию дельта-штамма SARS-CoV-2. Его отличительными черты — максимальная трансмиссивность (один распространитель инфицировал около 25 человек), высокая летальность и вероятность реинфекции. Штамм омикрон также характеризуется значительной заразностью, однако частота осложнений при инфицировании им оказалась ниже. И сегодня Всемирная организация здравоохранения включает штаммы дельта и омикрон в список вызывающих беспокойство вариантов SARS-CoV-2.
Пандемия НКИ продолжается. По состоянию на начало апреля 2022 года в мире зарегистрировано более 489 млн случаев заражения SARS-CoV-2, 10 % из которых случились у больных СД. А их доля среди умерших от COVID-19 пациентов составила около 20 %. Согласно результатам метаанализа восьми исследований с участием 46 248 пациентов, СД оказался одним из самых частых коморбидных состояний при COVID-19, уступая только артериальной гипертензии (АГ). Это стало неожиданностью для врачей: предполагалось, что первые места займут бронхиальная астма и другая патология органов дыхания. Татьяна Николаевна сослалась на собственный опыт, который показал, что тяжесть течения НКИ у пациентов с СД действительно несравнимо выше, чем у страдающих респираторными заболеваниями.
Еще один метаанализ 14 исследований показал, что распространенность СД в популяции пациентов с COVID-19 составляла 28 %. По разным данным, доля диабетиков среди заболевших COVID-19 составляет от 5,3 до 36 %. По данным метаанализа, опубликованного в 2020 году, каждый 12-й пациент с НКИ страдает СД. Среди 883 пациентов, госпитализированных в ГКБ № 52 с подтвержденным с помощью ПЦР диагнозом COVID-19 и поражением легких на КТ, распространенность СД 2 типа составила 43,3 %.
ФАКТОР ОСОБОГО РИСКА
Пациенты с СД и COVID-19 имеют высокий риск плохого прогноза. Особенно это касается пожилых пациентов, мужчин и тех, кто страдает АГ и сердечно-сосудистыми заболеваниями (ССЗ — ишемическая болезнь сердца и другие). По данным исследований, среди пациентов с СД и гипергликемией госпитальная смертность в четыре раза выше, чем у диабетиков без гипергликемии.
Опубликованный в 2021 году метаанализ подтвердил, что СД является одной из ведущих причин смертности от COVID-19 в стационаре. Хотя расчетный риск смерти от COVID-19 высок как для больных СД 1 типа, так и 2 типа, спикер отметила, что за период пандемии в стационаре ГКБ № 52 не было ни одного случая смерти пациента с СД 1 типа. Исключение составляют пациенты с СД 1 типа и терминальной стадией хронической болезни почек (ХБП), но их следует рассматривать отдельно как особо тяжелую категорию больных.
Высказывалось мнение, что СД 1 типа не ассоциирован с выраженным цитокиновым штормом и протекает легче, чем СД 2 типа, но при анализе данных из Великобритании оказалось, что смертность среди пациентов с СД 1 типа во время пандемии значительно выше, чем вне ее. Среди возможных факторов влияния пандемии на летальность при СД 1 типа, даже без учета инфицирования SARS-CoV-2, Татьяна Николаевна назвала меньшую доступность врачебных консультаций, меньший уровень назначения современных лекарственных препаратов, снижение уровня контроля эффективности и безопасности терапии.
Возвращаясь к аспектам течения COVID-19 у пациентов с СД 2 типа, спикер привела данные собственных наблюдений. Анализ факторов летального исхода у 1460 пациентов, из которых 20,6 % составляли больные СД 2 типа, показал, что смертность в когорте страдавших COVID-19 была в два раза выше, чем у инфицированных SARS-CoV-2 без СД 2 типа (18,7 и 10,6 % соответственно), независимо от циркулирующего штамма. При анализе структуры наиболее частых причин смерти больных СД 2 типа, по данным московского сегмента Федерального регистра сахарного диабета с 2013 по 2021 год, выяснилось, что одну из ведущих позиций занимает COVID-19 (24,1 %).
 МИРОВОЙ ОПЫТ
МИРОВОЙ ОПЫТ
На 81-м конгрессе Американской диабетической ассоциации (АДА) в 2021 году отдельная сессия была посвящена СД при НКИ. Эксперты пришли к выводу, что есть все признаки повреждения β-клеток поджелудочной железы вирусом SARS-CoV-2 у пациентов с СД и без него, но у диабетиков наблюдается более агрессивный цитокиновый шторм. Все вышеперечисленное приводит к нарушениям углеводного обмена, отсюда вытекают гипергликемия, наблюдаемая при всех поступлениях в стационар по поводу COVID-19, ухудшение метаболического контроля у пациентов с СД и трудность достижения компенсации углеводного обмена, а также дебют впервые возникшего СД на фоне НКИ. Пациенты характеризуются такими клиническими признаками, как ожирение, высокая активность системного воспаления, гипергликемия, диабетический кетоацидоз, гиперкоагуляция. С учетом того, что многие из них принадлежат к старшей возрастной группе и страдают АГ, ССЗ, ХБП, понятен высокий процент тяжелых исходов COVID-19 у диабетиков. Эксперты АДА сообщают, что вакцина против COVID-19 защищает от развития тяжелой НКИ у пациентов с СД, а потому больные диабетом должны быть отнесены к категории высокого риска и получить широкий доступ к соответствующей вакцине. В период циркуляции дельта-штамма Центр по контролю и профилактике заболеваний опубликовал данные, согласно которым невакцинированные пациенты с СД умирали от COVID-19 в 11 раз чаще, чем привитые по полной схеме. Вакцинированные люди в 10 раз реже госпитализировались и в 5 раз реже инфицировались COVID-19 по сравнению с непривитыми гражданами. В связи с осложнившейся эпидемиологической ситуацией российские алгоритмы специализированной помощи больным СД также были дополнены. В них появился отдельный раздел, в котором подчеркнута важность плановой вакцинации для пациентов с СД.
ОТЕЧЕСТВЕННЫЕ ДАННЫЕ
Изучение повреждения β-клеток поджелудочной железы вирусом SARS-CoV-2 началось после того, как было замечено, что у пациентов, которые не страдали ранее СД, а только имели факторы риска, на фоне COVID-19 развивался диабет. Также пациенты, которые получали ранее пероральные сахароснижающие препараты (ПССП), вынуждены были перейти на инсулинотерапию. Известно, что для проникновения внутрь клетки SARS-CoV-2 использует рецептор ангиотензинпревращающего фермента (рАПФ), который экспрессируется на мембране клеток целого ряда органов и тканей, в том числе β-клеток поджелудочной железы. Вирус нарушает образование гранул инсулина, функционирование митохондрий и АТФ, в результате чего происходит абсолютное снижение уровня инсулина. У пациентов, которые уже страдают СД, наблюдается исходное повышение провоспалительного фона, на который накладывается НКИ, что приводит к еще более выраженному повышению уровней таких провоспалительных цитокинов, как интерлейкин-6, фактор некроза опухолей альфа, а также к гиперкоагуляции и более обширному поражению легочной ткани. Ключевыми для эндокринной системы можно считать возможность развития гипергликемии и вероятность усугубления инсулинорезистентности.
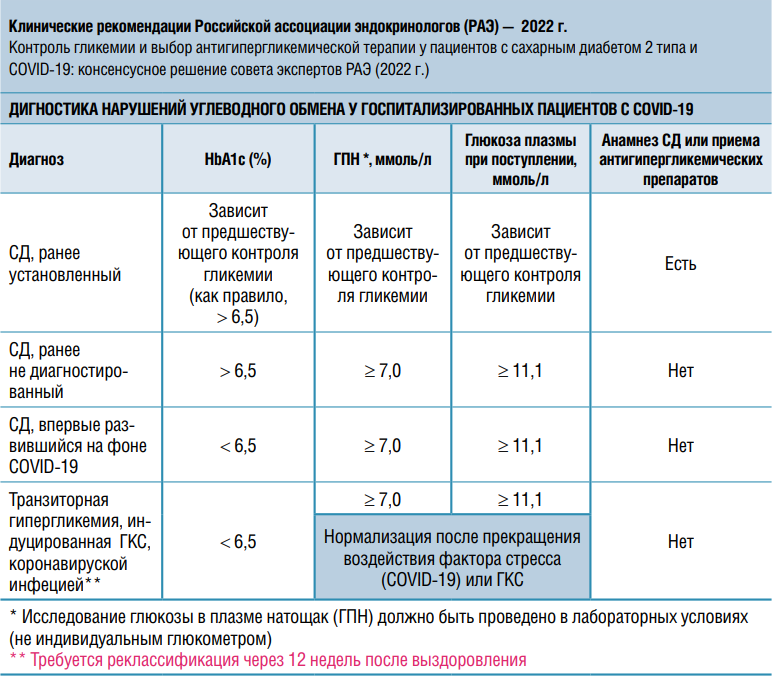
В декабре 2021 года на заседании экспертного совета Российской ассоциации эндокринологов были представлены данные о том, что 94,7 % госпитализированных по поводу COVID-19 пациентов с СД 2 типа в стационаре получали инсулин, а 22,2 % выписывались на инсулинотерапии. При этом предсказать, какая конкретно дозировка инсулина потребуется больному, практически невозможно. Это могли быть как 18 ЕД инсулина короткого действия, так и 150 ЕД базис-болюсной терапии.
«При инициации терапии на острой стадии, как правило, назначается базис-болюсный режим, — сообщила профессор Т.Н. Маркова, — но если пациент уже использует инсулинотерапию и получает современные препараты, мы оставляем базальный инсулин, добавляя при необходимости инсулин короткого действия, или увеличиваем дозы. В острой фазе не всегда есть возможность введения аналогов инсулина длительного и сверхдлительного действия, так как мы, к сожалению, не располагаем временем, необходимым для накопления дозы. Кроме того, инсулин НПХ (нейтральный протамин Хагедорна) позволяет подстраиваться под пики гликемии на фоне терапии глюкокортикостероидами, которые назначаются почти всем пациентам. При выписке мы пытаемся перевести пациентов на таблетированные препараты, но далеко не всегда удается это сделать, и многие больные вынуждены далее получать базис-болюсную инсулинотерапию».
В целом летальность среди пациентов, получающих инсулинотерапию, выше, чем при приеме пероральных противодиабетических препаратов, но это обусловлено не собственно получением инсулина, а скорее наличием дополнительных факторов неблагоприятного исхода в данной группе больных (больший стаж диабета, старший возраст, сопутствующие заболевания). Применение метформина, напротив, значимо—в 3,6 раза!—снижало риск летального исхода.
 ВЗАИМНОЕ УТЯЖЕЛЕНИЕ
ВЗАИМНОЕ УТЯЖЕЛЕНИЕ
Потребность в высоких дозах инсулина обусловлена эскалацией инсулинорезистентности на фоне COVID-19. SARS-CoV-2 способен повреждать рецептор к инсулину и нарушать их взаимное связывание. Инсулинорезистентность сама по себе запускает факторы провоспалительного фона, провоцирует нарушение пищевого поведения, отложение висцерального жира и формирование метаболического синдрома. Все это вносит вклад в развитие так называемого постковидного диабета — так проявляется взаимосвязь между СД и COVID-19. Пациенты, перенесшие НКИ в тяжелой форме, могут не вернуться к исходному состоянию здоровья. COVID-19 влияет на метаболизм и вызывает долгосрочные последствия в среднем у 80 % больных (от 5 до 96 %). Симптомы постковидного синдрома крайне неоднородны, и примерно у 4 % больных развивается СД. В обновленных версиях руководств по ведению пациентов с отдаленными последствиями COVID-19 обозначены такие значимые для эндокринологов системные состояния, как СД, гипотиреоз, дефицит витаминов D и В12, нарушения пищевого поведения. Среди заболеваний и состояний, потенцирующих тяжесть течения COVID-19 у больных диабетом, Татьяна Николаевна назвала ожирение, ХБП и АГ. Модификация этих факторов риска могла бы повлиять на течение НКИ. При этом, по собственным данным докладчика, ожирение не является фактором риска летального исхода при COVID-19: индекс массы тела (ИМТ) выше 30,0 кг/м2 не влияет на смертность от НКИ, но повышает риск тяжелого течения инфекции в 1,7 раза. Другое дело — окружность талии (ОТ). Ее величина существенно влияет на течение НКИ и летальность: при ОТ более 101,0 cм риск смерти от COVID-19 повышается в 4,9 раза, вероятность тяжелого течения инфекции — в 4,0 раза, шанс перевода в отделение реанимации и интенсивной терапии— в 5,8 раза, необходимость в искусственной вентиляции легких — в 4,3 раза. Таким образом, важно достигать не просто снижения массы тела, а именно уменьшения окружности талии. Далее спикер перешла к обсуждению контроля гликемии при СД. Доказана мощная ассоциация между уровнем гликированного гемоглобина (HbA1c) до заболевания и риском тяжелого течения НКИ. Если уровень HbA1c не превышает 6,0 %, тяжесть течения практически не усугубляется. Но уже при уровне HbA1c 8,0 % течение COVID-19 значительно утяжеляется. Докладчик напомнила, что значение HbA1c 8,0 % регистрируется у многих пациентов с СД 2 типа. Между тем длительность течения СД 10 лет и более и уровень HbA1c выше 9,0 % являются независимыми факторами увеличения риска летального исхода.
В 2020 году были опубликованы данные исследования, показавшего, что хороший контроль гликемии ниже 10 ммоль/л связан с выживаемостью 98,9 % больных. И напротив, плохой контроль гликемии выше 10 ммоль/л
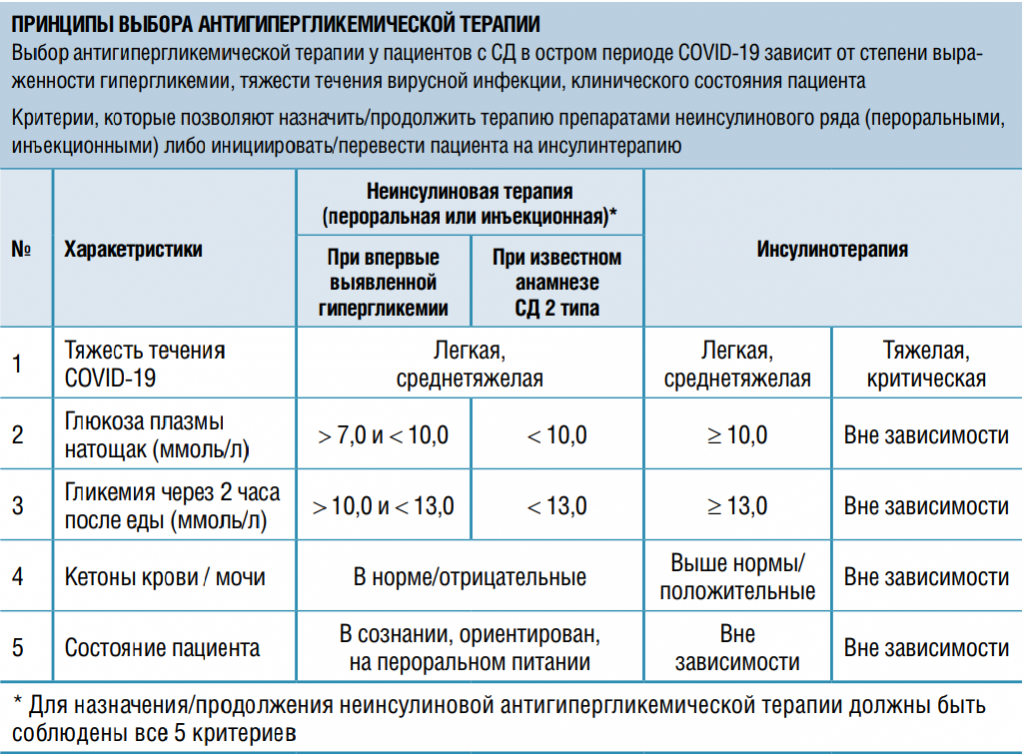
сопровождается высокой смертностью (около 11 %). Т.Н. Маркова обратилась к собственным данным, согласно которым исходный уровень гликемии при поступлении в стационар влиял на смертность как у пациентов с СД, так и без него. Эксперты из Китая считают гликемию 6,5–6,6 ммоль/л фактором развития цитокинового шторма наряду с интерлейкинами, ферритином и лактатдегидрогеназой даже у больных без СД. Кроме того, высокая вариабельность гликемии также является фактором повышенного риска неблагоприятных исходов у пациентов с СД и COVID-19, а терапия, улучшающая эти показатели гликемического контроля, может благоприятно отразиться на прогнозе. Таким образом, адекватный гликемический контроль является важным фактором снижения тяжести течения и летальности в период пандемии.
ВПЕРВЫЕ ВОЗНИКШАЯ ГИПЕРГЛИКЕМИЯ У ПАЦИЕНТОВ БЕЗ СД
Еще в 2020 году было показано, что впервые возникшая гипергликемия связана с более высоким риском смерти у госпитализированных пациентов с COVID-19, чем уже диагностированный СД. Эти данные докладчик назвала шокирующими: оказалось, что впервые выявленная гипергликемия опаснее декомпенсированного СД. Объяснения этому факту пока не нашли. Можно предположить, что на фоне хронической гипергликемии цитокиновый шторм в плане повреждения эндотелия, перекисного окисления липидов, оксидативного стресса, поражения органов-мишеней протекает менее активно, чем при впервые выявленной гипергликемии. Показано, что при отсутствии СД и при значениях HbA1c ниже 6,5 % и уровне гликемии выше 7 ммоль/л скорректированный риск смерти возрастает в 10 раз относительно нормогликемии. На уже упоминавшейся сессии АДА в 2021 году обсуждался еще один глобальный вопрос: может ли COVID-19 вызывать развитие СД? Предлагалось учесть возможное наличие у пациентов факторов риска СД, влияние стресса, применение глюкокортикостероидов, а также наличие ранее не диагностированного СД. Но существует ли также отдельная форма диабета после COVID-19, связанная с повреждением β-клеток? Пока этот вопрос остается без однозначного ответа. По собственным данным спикера, нарушения углеводного обмена по уровню HbA1c регистрировались у 41,7 % госпитализирующихся пациентов, но только у 29,2 % наблюдалось повышение уровня глюкозы плазмы крови натощак. Значения HbA1c в острую фазу не всегда адекватно отражают качество углеводного обмена. Однако при этом уровень HbA1c достоверно положительно коррелировал с факторами воспаления, такими как С-реактивный белок и цитокиновый шторм. На момент выписки практически все пациенты с исходным повышением HbA1c имели нормогликемию. Нарушения углеводного обмена у них носили транзиторный характер. Метаанализ восьми когортных исследований 2021 года продемонстрировал частоту развития впервые возникшего диабета после COVID-19 до 14,4 %. Сегодня пул информации пополнился и оказалось, что, по данным из различных источников, потенциальный риск развития СД после перенесенной коронавирусной инфекции с глюкокортикостероидной терапией существует у 30 % пациентов. После перенесенной инфекции в срок от 20 до 90 дней с момента отрицательного результата ПЦР-теста СД диагностируется в 6 % случаев.
В медицинском сообществе до сих пор нет единого мнения о сроках установления диагноза «СД после перенесенной коронавирусной инфекции», как нет и сравнительных данных с пациентами, не получавшими глюкокортикостероиды. Имеется статистика М.В. Шестаковой: по результатам наблюдения 155 пациентов в течение 6 месяцев после перенесенной НКИ, частота впервые выявленного СД в НМИЦ эндокринологии составила 5,2 %. Ретроспективный стандартизированный анализ данных реальной клинической практики в Германии с марта 2020 по июль 2021 года, охвативший 35865 пациентов с перенесенным COVID-19 и 35865 больных с перенесенной ОРВИ, показал, что среди пациентов с COVID-19 наблюдалась более высокая частота развития СД 2 типа, но ассоциации с развитием диабета других типов выявлено не было. По мнению авторов, всем пациентам, даже перенесшим COVID-19 в легкой форме, следует проводить скрининг нарушений углеводного обмена. Между тем у детей и подростков в Европе было показано увеличение частоты впервые выявленных случаев СД в весенние и летние месяцы 2020 года по сравнению с 2019-м, когда пандемия еще не была объявлена. Общее число диагностированных случаев СД 2 типа среди детей и подростков увеличилось во время пандемии на 293 %. После ее окончания следует ожидать увеличения распространенности СД, патогенез которого предстоит уточнить.
При окружности талии более 101,0 cм риск смерти от COVID-19 выше в 4,9 раза, тяжелого течения инфекции — в 4 раза, перевода в отделение реанимации и интенсивной терапии — в 5,8 раза, необходимость в ИВЛ — в 4,3 раза
НОВОЕ В ЛЕЧЕНИИ
Т.Н. Маркова привела собственные данные наблюдения за 1500 пациентами с факторами риска тяжелого течения COVID-19 (в том числе больных СД) с положительным результатом ПЦР-теста, но еще без клинических и компьютерно-томографических проявлений инфекции, которым в условиях дневного стационара вводились моноклональные антитела против SARSCoV-2. Получены хорошие результаты по предотвращению тяжелого течения и неблагоприятного исхода НКИ. Сейчас ожидается появление нового препарата из группы моноклональных антител, который вводится внутримышечно, обеспечивая защиту от инфицирования SARS-CoV-2 на протяжении года. Спикер выразила надежду, что вскоре поле битвы с НКИ зарастет травой, а мы перейдем в зону профилактики, памятуя об уроках, которые преподала нам пандемия, в частности о том, насколько важны достижение целевых показателей гликемии и своевременное выявление СД.