Статьи
Артериальная гипертензия и атеросклероз: диалог кардиолога и липидолога
На фоне «плато» в разработке антигипертензивной терапии медицинское сообщество продолжает нуждаться в периодическом подведении промежуточных итогов, по возможности под разными углами зрения. Кардиолог Антон Владимирович РОДИОНОВ и липидолог Игорь Владимирович СЕРГИЕНКО представляют именно такие взаимодополняющие взгляды на взаимосвязь артериальной гипертензии (АГ) и ее «серого кардинала», атеросклероза (АС) — одного из «молчаливых убийц» тысячелетия1.
АГ, АС и курение—неизменная триада факторов риска (ФР) развития инфаркта миокарда (ИМ), нарушения мозгового кровообращения (НМК), сердечной недостаточности (СН) и других сердечно-сосудистых (СС) осложнений (ССО). Все эти состояния объединяет присутствие эндотелиальной дисфункции (ЭД), в плане влияния на которую рассматриваются и изучаются большинство антигипертензивных препаратов (АГП).
С патофизиологических позиций перечисленные ССО представляют собой не отдельные нозологии, а закономерные варианты, «ответвления» дисфункционального процесса, включающего воспаление, фиброз и другие патологии. Задача врача —застать и «удержать» пациента на одной из этих фаз сердечно-сосудистого континуума, предпочтительно при изолированном воздействии какого-либо из ФР.
Складывается впечатление, что в ближайшее 10‑летие в фармакотерапии АГ едва ли предвидятся значительные изменения (чего нельзя сказать о лечении дислипидемий (ДЛП)). В обновлениях международных рекомендаций можно ожидать лишь уточнения стратифицированных целевых уровней (ЦУ) артериального давления (АД). Для новых же подходов во многом до сих пор отсутствует достаточная доказательная база. На первый план выходит рациональное использование имеющихся терапевтических молекул и их комбинаций.
Сейчас стало реальным достижение необходимых величин АД и холестерина (ХС) липопротеинов низкой плотности (ЛНП). Попробуем кратко охарактеризовать главные компоненты современного медикаментозного арсенала, позволяющие этого добиться.
БИТВА ЗА СОСУДЫ
У артерий эластического типа есть важнейшая функция—преобразование фазовой деятельности сердца в непрерывный, близкий к ламинарному кровоток. Это явление известно как эффект виндкесселя (резервуара, нем. Windkesseleffekt), помогающий гасить на протяжении сердечного цикла ударные волновые колебания кровяного давления и способствующий поддержанию тканевой/органной перфузии. По мере прогрессирования АС увеличивается жесткость сосудов с нарушением распространения пульсовой волны, и с этой жесткостью обязательно надо бороться.
Сосудистая терапия—совокупность гиполипидемического воздействия (фактически укрепляющего атероматозные бляшки (АТБ), снижающего риск атеротромботических/атероэмболических эпизодов, даже если в бляшках повышается содержание кальция) и лечения непосредственно АГ, также направленного на редукцию сосудистой жесткости. Антиагреганты же назначаются дополнительно не во всех случаях и не в рамках первичной профилактики (ПП).
ДОЛГИЙ ИЛИ БЫСТРЫЙ ЭФФЕКТ?
Для воздействия на течение АС посредством АГП нужны препараты, влияющие на состояние стенки эластических артерий с уменьшением ее жесткости,— в первую очередь антагонисты кальция (АК). Чем больше совокупная атеросклеротическая масса в организме, тем специфичнее характер гипертензии: течение ее может стать весьма лабильным, у пожилых возможна картина изолированной систолической АГ (ИСАГ).
Значительная вариабельность (среднесуточный разброс) систолического АД (эффект «качелей») затрудняет лечебный процесс, так как многие АГП отличаются длительным (1,0–1,5 сут) действием и не всегда рассчитаны на ситуационную коррекцию гипертонии. Кроме того, такая вариативность течения болезни достоверно ухудшает кардиоваскулярный прогноз. При этом критерий вариабельности отнюдь не чисто научный, а вполне практический, входящий в протокол холтеровского мониторирования. Во многих исследованиях, в т.ч. SPRINT, изучалась связь частоты осложнений (риски СН, НМК, смерти от любых причин) и вариабельности АД при прочих равных условиях (идентичные показатели офисного/среднесуточного АД и др.).
Не улучшает положение и избыточный самоконтроль — частые измерения АД пациентами с многочисленными попытками самостоятельного ситуационного воздействия на него. Сама боязнь высоких значений давления (как и любой стресс) приводит к его повышению. За этим обычно следует прием АГП, как правило, короткодействующих: каптоприла, моксонидина и т.п. Формируется порочный круг; с ростом АД потребность в АГП также возрастает.
На фоне же метилирования адреналина и кумуляции препаратов давление снижается, иногда до очень низких цифр (симптомная гипотония). И вместо уменьшения вариабельности пациент и врач получают ее рост. Такие больные нуждаются в обучении, тщательном, иногда многократном разъяснении сущности феномена АД и недопустимости чрезмерного его снижения «здесь и сейчас», а иногда — во вмешательстве психолога, психотерапевта и/или психиатра: описанное состояние является одним из многочисленных вариантов невротических расстройств.
Иногда терапия АГ (на любом этапе) должна осуществляться в соответствии с особыми показаниями. Так, у беременных средством 1‑й линии остается не всегда доступная сейчас метилдопа, а 2‑й — пролонгированные АК. Можно назначить β-адреноблокаторы (ББ), если ожидаемая польза превышает потенциальный риск.
ФАРМАКОЛОГИЧЕСКАЯ «ИЕРАРХИЯ»
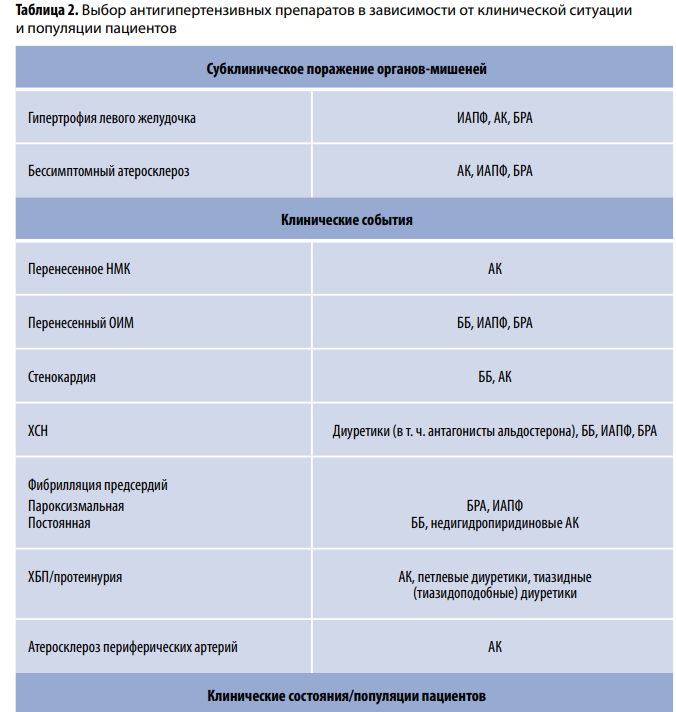
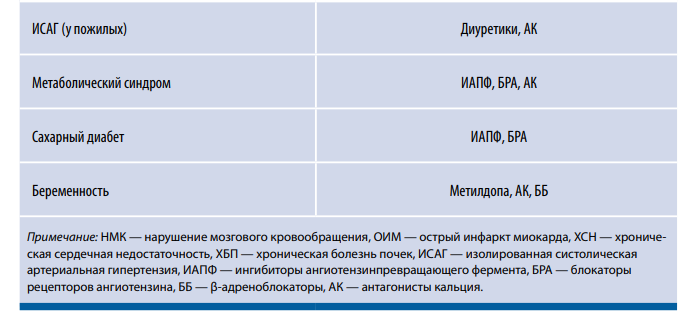
«Краеугольные камни» в лечении АГ — ингибиторы РААС (ангиотензинпревращающего фермента, ИАПФ и сартаны — блокаторы рецепторов ангиотензина (БРА)) наряду с АК и тиазидными (тиазидоподобными) диуретиками (ТД). Остальные классы АГП, включая ББ, должны рассматриваться как резерв. Что касается цереброваскулярной болезни и периферического сосудистого АС, то при их наличии эта схема не имеет принципиальных особенностей, будучи применима у большинства пациентов.
Современный рынок ингибиторов РААС разнообразен: немногим менее 10 ИАПФ и 7 (из 9 зарегистрированных в РФ) сартанов. Конечно, нельзя абсолютно точно расписать, каким пациентам дифференцированно показан тот или иной ИАПФ/БРА. Но иногда действительно хорошие лекарства исчезают из поля зрения клиницистов—об этих АГП не информируют или делают это недостаточно. При выборе нужно в целом ориентироваться на такие характеристики, как выраженность терапевтического эффекта, переносимость и др.
Первый показатель у большинства молекул относительно сопоставим; переносимость же (по выраженности кашля) у ИАПФ в общем контексте не столь значима, а для сартанов сопоставима с таковой плацебо (истинная плохая переносимость встречается в <1 % случаев назначения БРА). По частоте приема (однократно в сутки для препаратов последних поколений) ЛС этой фармгруппы также выгодно отличаются от остальных.
Существенный для пациента момент— соотношение цены и качества препарата. В большинстве ситуаций выбираются достаточно качественные и не очень дорогие дженерики. Безусловно, необходимо учитывать наличие у пациента почечной или/и печеночной недостаточности.
Наконец, важна доказательная база, показывающая, в каких клинических ситуациях те или иные АГП изучались в плане их терапевтических свойств. В этом отношении ИАПФ и БРА также идут рядом. Например, по данным исследования «лоб в лоб» ONTARGET среди больных с высоким СС риском (ССР) (в т.ч. имеющих АГ, ИМ, СН, сахарный диабет) рамиприл и телмисартан оказались равноэффективными в профилактике кардиоваскулярной заболеваемости и смертности в возрастной группе >55 лет; различий же по прогнозу между двумя медикаментами не выявлено. С учетом этого высокий ССР зарегистрирован как одно из показаний для сартанов.
АНТАГОНИСТЫ КАЛЬЦИЯ И ДИУРЕТИКИ
Следующие по значимости при умеренном/выраженном атеросклеротическом процессе—АК. И опять: чем существеннее общая атеросклеротическая масса, тем больше для них показаний. Поскольку патофизиологически АС — это во многом сосудистая жесткость, ведущая к НМК, позитивное действие АК на сосуды эластического типа и артериолы существенно. По показателю снижения риска НМК эти ЛС превосходят АГП остальных классов. Результаты исследовательского протокола PREVENT наилучшим образом подтверждают мягкий антиатеросклеротический/антиатерогенный эффект АК.
АК, как и диуретики, в большей степени нивелируют вариабельность АД по сравнению с другими препаратами. Таким образом, нуждающемуся в комбинированном лечении (КЛ) пациенту с АС целесообразно совместное назначение блокаторов РААС и АК.
Наконец, представители фармакологического класса ТД условно занимают третью позицию и могут комбинироваться с ИАПФ/ БРА и/или АК.
Многие из ЛС существуют в виде фиксированных комбинаций (ФК) — сегодня «стратегия одной таблетки» выступает одним из главных трендов в лечении АГ, СД и ДЛП.
ВАРИАБЕЛЬНОСТЬ АД
Давайте вновь обратимся к вариабельности АД как одной из лечебных мишеней, взглянув на нее с позиций длительности действия этих ЛС. Здесь большую роль играет показатель through-to-peak (through-to-peak ratio — TPR, Т/Р) — отношение остаточного/ максимального эффекта АГП на протяжении дозирования, характеризующее равномерность действия лекарства. Сохранение эффекта до следующих после приема суток в значительной мере определяет органопротективные свойства препарата. В этом отношении предпочтение следует отдавать наиболее плавно действующим телмисартану, азилсартану и кандесартану, а также амлодипину.
Иногда гипервариабельность АД оказывается результатом недостаточной или отсутствующей приверженности лечению. Для многих ЛС нет объективных критериев того, действительно ли пациент их принимает (за исключением появления брадикардии для ББ и глюкозурии — для ингибиторов натрий-глюкозного котранспортера 2 типа (ИНГТ2; SGLT2)). В работах по эффектам ББ ЧСС <70 в 1 мин зарегистрирована лишь у 90 % участников, что можно рассматривать как суррогатный показатель комплаентности. Но есть и еще одна причина избыточной вариабельности—банальный пропуск приема АГП, способный, как установлено, повышать риск СС катастроф на 40 %. Отсюда следует вывод: уверенно и объективно судить о соблюдении пациентом лечебного графика пока невозможно.
УРОВЕНЬ ХС
Безусловно, при лечении АГ нужно постоянно держать под контролем уровень ХС, что достигается в первую очередь использованием статинов. В исследовании ASCOT-LLA аторвастатин снижал риск нефатального/бессимптомного/фатального ИМ на 36 % и всех ССО — на 21 %. Правда, в качестве референтных рассматривались несколько бóльшие показатели общего ХС по сравнению с традиционно принятыми. Кроме того, не представлялось возможным установить наличие/отсутствие ишемической болезни сердца (ИБС) на момент включения каждого участника в протокол. Дело в том, что классическая картина стенокардии стала встречаться в общей популяции гораздо реже, и наряду с вероятным патоморфозом это прежде всего успехи ПП АС, который у таких людей развивается медленнее. При этом клинические проявления оказываются более стертыми, что также нужно учитывать.
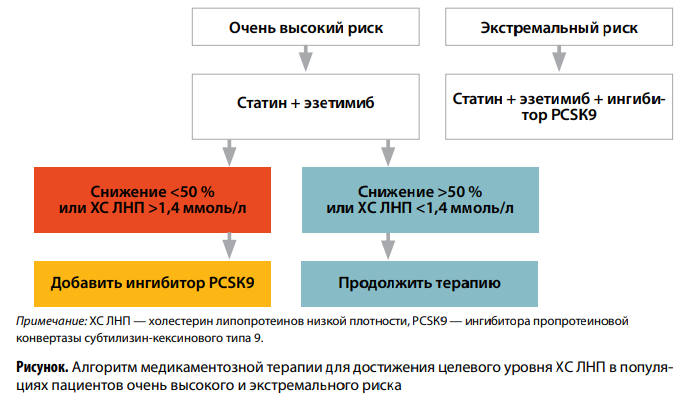
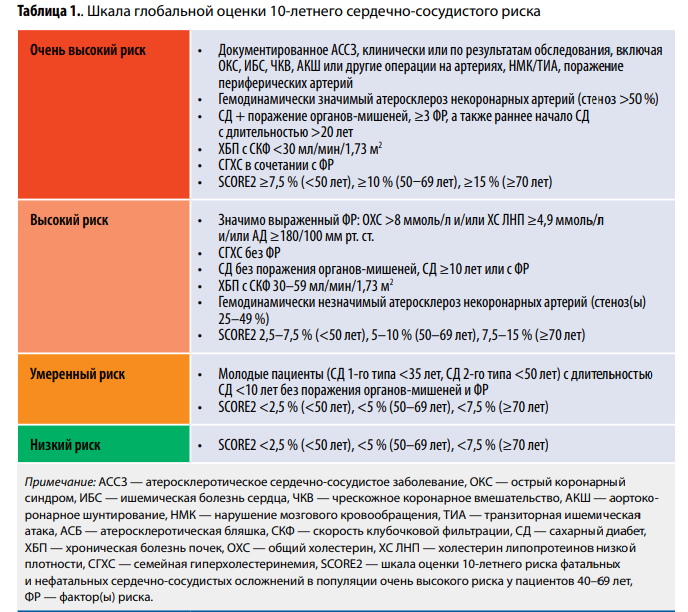
Персонификация лечебного подхода диктует необходимость рассматривать пациента именно в определенной категории риска. Только отечественные клинические рекомендации (КР) — единственные среди аналогичных документов — предусматривают выделение подгруппы экстремально высокого риска (ВР) в составе группы очень высокого риска (ОВР). Представителям последней в случае соответствующих изменений липидного профиля (ЛП) изначально показано тройное назначение статина, эзетимиба и ингибитора пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9) (алирокумаб). При ВР назначаются статин с эзетимибом по отдельности либо в ФК.
NOTA BENE!
На практике часто даже незначительное повышение активности АЛТ, АСТ, γ-ГТП априорно расценивается как противопоказание к назначению статинов. В этой связи уместно рассказать об исследовании ESSENTIAL, сравнивавшем эффективность/безопасность розувастатина и комбинации розувастатин + эзетимиб при неалкогольной жировой болезни печени (НАЖБП). В ходе протокола 70 участников получали 5 мг розувастатина либо КЛ эзетимиб 10 мг + розувастатин 5 мг. Назначение столь малых доз объяснялось повышенной (но не превышавшей 3 верхних границ нормы) активностью печеночных ферментов.
Пациентам выполнялись МРТ, определение количества жира (не структурированной жировой ткани как таковой!) в печени и МР-эластография (МРЭ) (параметр, отражающий выраженность гепатофиброза). КЛ, будучи безопасным при НАЖБП, достоверно в большей степени уменьшало количество жира в печени по сравнению с МТ. В ряде случав наблюдалось снижение умеренно повышенных показателей активности АСТ, АЛТ и γ-ГТП — как маркер эффективности, но не цель лечения. Преимущества КЛ при НАЖБП отчетливее проявлялись при ИМТ <30, саркопении, нормальных значениях индекса HOMA-IR и отсутствии изменений при МРЭ.
АС И ПОЧКИ
Напомним: при прогрессировании генерализованного АС можно наблюдать среди прочего картину вазоренальной гипертензии (ВРГ). На нее может указывать утяжеление существующей АГ с утратой эффективности проводимого лечения — иными словами, эссенциальная гипертензия трансформируется в вазоренальную. Чаще всего это происходит при атеросклеротическом (одно- или двустороннем) поражении почечной артерии. Необходимы УЗДГ брахиоцефальных, почечных артерий, УЗИ почек. Иногда на фоне приема ИАПФ или сартана возрастает концентрация креатинина, падает скорость клубочковой фильтрации (СКФ); развивается острое почечное повреждение.
При подозрении на ВРГ и нормальной картине дуплексного сканирования почечных артерий следующий шаг—МСКТ почек с контрастированием либо МРТ без контрастирования. Иногда обнаруживается добавочная почечная артерия с нормальным допплеровским спектром, в действительности имеющая выраженный стеноз.
ЦЕЛЬ ОДНА, СПОСОБОВ — МНОГО
Сейчас все в большей степени просматривается тенденция отхода от медленного титрования доз статинов, иногда способствующего снижению комплаентности. В этой связи при назначении КЛ (фиксированном или раздельном приеме препаратов) следует избегать инициальных доз розувастатина 5 мг и аторвастатина 10 мг. Аналогичная ситуация имеет место и при лечении АГ; все чаще вместо монотерапии и титрации монодозы назначаются (одновременно либо с минимальным временны́м интервалом) два АГП. Однако иногда важно именно постепенное и ступенчатое снижение АД, особенно у пожилых, хрупких пациентов, когда целесообразнее начать с МТ.
В случае адаптации к систолическому АД 180 (и даже 200) мм рт. ст. выраженное и быстрое снижение АД в течение суток (например, до систолического 110 мм рт. ст.) почти неизбежно вызовет известные проблемы иного рода: тканевую гипоперфузию, системную гипотензию и др.
Понятно, что большинство современных АГП—препараты накопительного действия. Для пациента же в идеале нужно приблизиться к ЦУ АД, по крайней мере в плане доверия к врачу, уже к следующему визиту. Поэтому если спустя 1 нед систолическое АД достигает 130–140 мм рт. ст., ситуация может быть расценена как позитивная.
Актуальные КР указывают на необходимый для достижения ЦУ АД срок, равный 3 мес. Соблюдение этих рамок позволяет также избежать штрафов страховых компаний. Однако не секрет, что врачи стационара вынуждены стабилизировать давление к моменту выписки—в соответствии с пресловутыми медико-экономическими стандартами медицинской помощи. Конечно, это не совсем правильно, особенно если перед нами пожилой человек, действительно адаптированный к существенно повышенному АД, что бывает не так редко. И тогда вполне оправдана тактика назначения двух АГП без задачи достичь быстрого снижения давления. Через 2–3 нед, если систолическое АД снизилось не очень значительно (150–160 мм рт. ст.), добавляется третье ЛС.
Обязательно следует помнить, что возможны весьма вариабельная реакция пациентов на лекарства и различное по скорости/интенсивности проявление их эффекта: здесь вступают в силу потенциальные фармакогенетические механизмы и т.п. Более того, часто стала встречаться именно перелеченность АГ как результат агрессивного терапевтического воздействия. Одним словом, нужно придерживаться «золотой середины», не забывая о необходимости правильно разговаривать с пациентом.
В свете сказанного просматривается потенциальная частота развития ИМ в результате гипертонического криза (ГК). Однако в действительности определить ее трудно. Согласно современной номенклатуре, под такой клинической ситуацией подразумевается то, что ранее именовалось осложненным ГК — например, резкое повышение давления с последующим ОКС.
Кроме того, начавшаяся терапия нивелирует многие последующие клинические феномены: ИМ как таковой может вести к выраженной гипотензии, кардиогенному шоку и др. Однако ИМ может быть спровоцирован неаккуратным и неграмотным лечением состояния, до сих пор именуемого многими «гипертонический криз».
И вновь мы возвращаемся к чрезмерному самоконтролю АД. Пациент — самостоятельно или нет — принимает большое количество короткодействующих АГП, и именно возникающая гипотония на фоне тяжелого АС может быть причиной ИМ и НМК вследствие падения периферического кровотока. В этом заключается недостаток такого применения короткодействующих ЛС при «неосложненном» ГК.
КЛИНИЧЕСКИЕ СИТУАЦИИ
1. Нередко у возрастных (>75 лет) пациентов на фоне лечения систолическое АД устойчиво снижается, в то время как диастолическое находится в пределах 55– 58–63 мм рт. ст. Так бывает, в частности, при ИСАГ. Не всегда можно уменьшить пульсовое АД, сохраняя неизменным уровень диастолического давления и снижая только систолическое. Препараты выбора здесь—преимущественно АК и диуретики. Необходимо исключить аортальную недостаточность, в чем помогут тщательная аускультация сердца, ЭхоКГ.

2. Требует ли лечения само по себе наличие у подобного пациента уровня общего ХС 7 ммоль/л без выраженной ИБС, СД, пере несенного атеротромботического/атероэмболического НМК? В плане ПП можно назначить монотерапию эзетимибом. Однако гораздо правильнее задаться вопросами: действительно ли ничего не скрывается за фасадом «изолированной» ГХС? Будет ли это именно ситуация ПП? Можем ли мы утверждать, что медикаментозное вмешательство не нужно? Дело в том, что среди пациентов все чаще встречаются равновозрастные люди обоих полов с многочисленными, но гемодинамически незначимыми АСБ, снижением СКФ. Следовательно, можно выявить тот или иной морфологический и патогенетический субстрат АС. В противном случае, вероятнее всего, общий ХС не был бы равен 7 ммоль/л.
3. Нужно ли пересматривать тактику терапии статинами при ухудшении показателей легочной гипертензии, если пациент получает диуретик по поводу АГ, или же предпочтительна замена последнего? Обычно диуретические препараты не увеличивают содержание ХС ЛНП, и это может быть совпадением. Описано некоторое повышение уровней липидов и ХС при назначении 100 мг гидрохлортиазида, в то время как обычно используют дозу 12,5 мг. Теоретически подобное возможно и на фоне хлорталидона — в дозе 25 мг, необходимость в которой возникает далеко не всегда. Поэтому в целом ситуация не служит показанием для замены ТД: можно при необходимости продолжить его прием либо перейти на АК.
***
Проблема взаимодействия и взаимовлияния АГ и АС в действительности неисчерпаема. Этот коварный тандем постоянно требует к себе неослабного внимания, не прощая ошибок. Записал Юрий Никулин, к.м.н.

















