Статьи
Флэш-мониторинг или традиционная глюкометрия — выбор очевиден?
По данным Всемирной организации здравоохранения, на 2018 год в мире зарегистрировано 425 млн пациентов с сахарным диабетом, что составляет около 5 % населения Земли. С увеличением продолжительности жизни растет и число таких больных.
АДЕКВАТНЫЙ КОНТРОЛЬ
Цели лечения пациентов с сахарным диабетом (СД) 2 типа зависят от ожидаемой средней продолжительности жизни, состояния сердечно-сосудистой системы, риска развития гипогликемических состояний, общего соматического статуса, способности проводить регулярный самоконтроль гликемии. При этом далеко не всегда удается достичь компенсации углеводного обмена, хотя адекватный контроль гликемии имеет первостепенное значение. По мере усложнения схем терапии правильный самоконтроль путем периодического самостоятельного измерения уровня глюкозы в крови становится решающим в достижении этой цели.
В последнее десятилетие непрерывный мониторинг глюкозы (НМГ), предоставляющий информацию о тенденциях изменения уровня глюкозы, оказывается все более востребованным. Весьма облегчает эту задачу система флэш-мониторинга FreeStyle Libre, простая в применении и дающая возможность своевременно отслеживать колебания уровня гликемии в повседневной практике. Метод флэш-мониторинга позволяет создать новую парадигму самоконтроля гликемии (СКГК).
Датчик, фиксирующий концентрацию глюкозы в интерстициальной жидкости, предоставляет числовые данные о ее показателях и направлении тренда, добавляющие контекст к статическому измерению уровня гликемии. Таким образом, пациенты могут легко следить за уровнем глюкозы в любой момент, что позволяет на раннем этапе обнаруживать и своевременно устранять отклонения от целевого диапазона, предотвращая тем самым резкие колебания данного показателя. Чтобы в полной мере воспользоваться преимуществами системы, медицинский работник, осуществляющий наблюдение, и пациент с диабетом должны осознавать необходимость тщательной интерпретации данных, полученных с помощью НМГ.
Многие пациенты с СД 1 типа продолжают иметь высокий уровень HbA1c, ассоциированный с возрастающим риском сердечно-сосудистых событий и летальностью. Использование флэш-мониторинга с помощью описываемой системы существенно улучшает у них гликемический контроль. Так, при его использовании у 92 пациентов с СД 1 типа в Великобритании уровень HbA1c снизился в среднем на 0,98 % через 3 месяца и на 1,47 % — через полгода. НМГ имеет большой потенциал как составляющая лечения СД 1 типа, улучшения метаболического контроля и качества жизни. Технология предоставляет значительно больше данных, чем результаты, полученные при традиционном периодическом измерении гликемии, которые могут не фиксировать интервалы экстремальной изменчивости, вариабельность гликемии или ночные гипогликемические события.
ИСТОРИЯ БОЛЕЗНИ
В качестве примера приведем клинический случай пациента К., 37 лет, страдающего СД 1 типа в течение 36 лет и находящегося на режиме базально-болюсной инсулинотерапии (ИТ). Контроль гликемии нерегулярный с помощью глюкометра, 4–5 раз в сутки. Перенес 4 и 3 года назад соответственно ампутацию обеих нижних конечностей по поводу диабетической гангрены, 2 года назад выполнена пересадка почки из-за развившейся терминальной почечной недостаточности. НвА1с — 14,1 %. Получает терапию аналогами инсулина детемир и аспарт, для профилактики отторжения трансплантата — такролимус, микофенолат и метилпреднизолон (препараты, оказывающие влияние в том числе на углеводный обмен). Опасается гипогликемий, которые регулярно ощущает, но редко фиксирует из-за выраженной слабости, старается придерживаться диетических рекомендаций.
Анализ данных гликемического профиля пациента проведен с использованием облачной платформы с веб-интерфейсом LibreView, с помощью которой врачи и пациенты могут создавать набор структурированных понятных отчетов и обмениваться ими. Веб-интерфейс позволяет агрегировать данные об уровне глюкозы всех пациентов, прикрепленных к медицинскому учреждению, осуществлять динамическое наблюдение и контроль. С появлением интерфейса стала доступна новая форма отчета «Амбулаторный профиль глюкозы, AGP» (от англ. ambulatory glucose profile), полностью соответствующая формату, рекомендованному Международным консенсусом по времени в целевом диапазоне. Анализ профиля гликемии пациента осуществлялся с помощью нового простого и удобного одностраничного отчета AGP, дающего ясное и четко структурированное представление о вариабельности гликемии в течение суток и степени компенсации углеводного обмена.
Отчет AGP состоит из нескольких частей. В первой, «Статистика по уровням глюкозы и целевые показатели», отражаются информация о периоде сбора данных, доли нахождения датчика в активном состоянии (аналог показателя «Доля принятых данных» в более ранней версии программного обеспечения), рекомендованные целевые показатели времени в диапазонах с распределением по уровням, средние значения уровня глюкозы, коэффициент вариабельности глюкозы (CV), а также индикатор контроля за ее уровнем, GMI (англ. glucose management indicator), показывающий вероятное значение HbA1c у пациента.
Вторая часть, «Время в диапазонах», отражает время пребывания данного пациента в целевом диапазоне, а также в зоне гипергликемии (уровень 1 со значениями глюкозы 10,1–13,9 ммоль/л и уровень 2 — более 13,9 ммоль/л), гипогликемии (уровень 1 со значениями глюкозы 3,8–3,0 ммоль/л и уровень 2 — менее 3,0 ммоль/л). Время в целевом диапазоне, а также выше и ниже него выражено в абсолютных и относительных значениях — в часах либо долях процентов времени в сутках, в течение которого пациент пребывал в указанном диапазоне значений глюкозы.
В третьей части отчета «Амбулаторный профиль глюкозы» отражается распределение значений ее концентрации с учетом их частотности. Обновленный формат отчета отображает кривые профиля глюкозы, ограниченные 5‑м и 95‑м перцентилями (вместо 10‑го и 90‑го перцентилей в предыдущей версии).
Часть отчета «Суточные профили глюкозы» представлена гликемическими кривыми за каждый из 14 последних дней наблюдения, включенных в отчет. Показатели глюкозы, превышающие верхнюю границу целевого диапазона (10 ммоль/л), выделяются в отчете желтым цветом, значения глюкозы ниже 3,9 ммоль/л — красным.
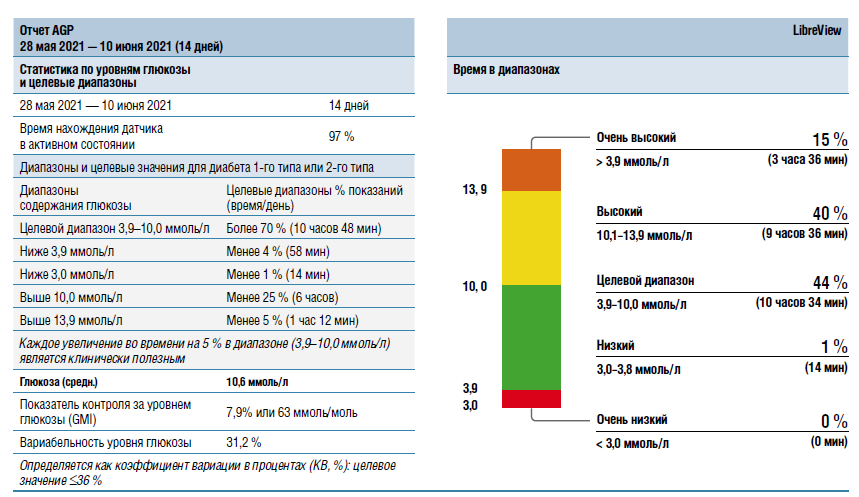
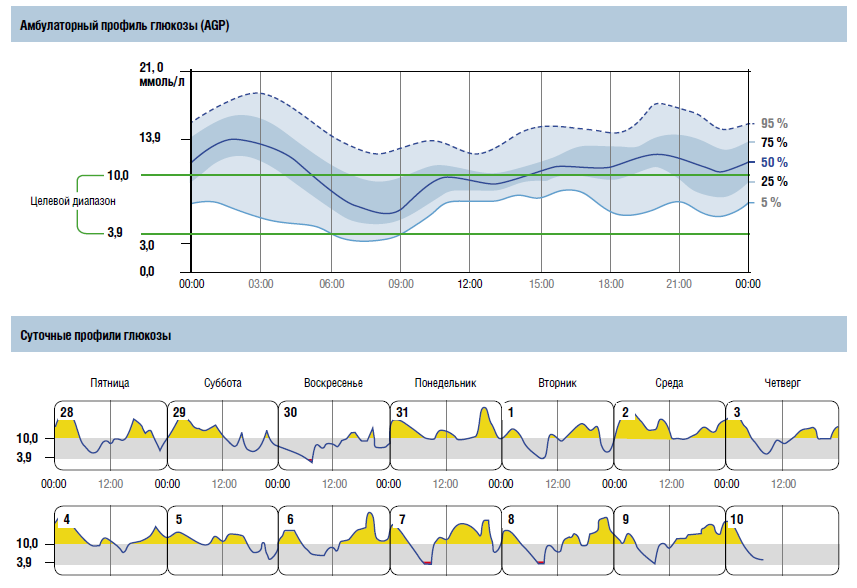
При оценке качества данных заметна высокая приверженность пациента к использованию флэш-мониторинга: принято 97 % данных датчика; период сбора данных (14 дней) полностью соответствует рекомендованному Международным консенсусом времени в целевом диапазоне. Время в целевом диапазоне 3,9–10,0 ммоль/л существенно ниже рекомендованных 44 % при желаемых значениях более 70 %. Время ниже целевого диапазона (1 %) соответствует рекомендованным консенсусом значениям (менее 4 % для значений уровня глюкозы ниже 3,9 ммоль/л и менее 1 % — ниже 3,0 ммоль/л). Обращает на себя внимание существенное превышение показателя времени выше диапазона целевых значений: уровень глюкозы выше 10,0 ммоль/л составляет 55 % при рекомендованном ниже 25 %. Время пребывания с крайне высоким уровнем глюкозы (более 13,9 ммоль/л) также превышает целевые значения. Медианная кривая практически на всем протяжении «модального дня», отраженного в разделе «Амбулаторный профиль глюкозы отчета AGP», находится выше верхней границы целевого диапазона, таким образом, основные проблемы данного пациента ассоциируются с длительным пребыванием в зоне гипергликемии.
Это подтверждается при анализе гликемических кривых в разделе отчета «Амбулаторный профиль глюкозы»: верхние границы интервалов с 95‑м и 75‑м перцентилями находятся выше границ целевого диапазона на протяжении всего времени суток. Следовательно, эпизоды гипергликемии наблюдались у данного пациента практически в любой промежуток времени и носят систематический характер. Данные особенности амбулаторного профиля глюкозы находят отражение и в суточных профилях: зоны гипергликемии, выделенные желтым цветом, выявляются в каждые из 14 дней периода наблюдения, в большей степени в ночные и ранние утренние часы. При этом с 6 до 9 утра отмечается снижение уровня глюкозы до целевых значений, а в двух из 14 дней — ниже 3,9 ммоль/л. Благодаря полученным данным пациент осознал обширность и точность измерений, объем параметров, выходящих за пределы референсных значений, полное отсутствие гипогликемий.
В связи с выявленными проблемами по результатам отчета AGP даны следующие рекомендации: увеличение дозы аналогов инсулина в зависимости от характера питания и образа жизни, коррекция гипергликемии в ночное время, учет лекарственного взаимодействия с препаратами, оказывающими влияние на углеводный обмен. Пациент начал коррекцию ИТ, усилил физическую нагрузку в пределах возможностей и упорядочил диетический режим, одновременно осуществляя дальнейший флэш-мониторинг гликемии.
ДИАБЕТИЧЕСКИЙ КЕТОАЦИДОЗ
Это острое осложнение, обусловленное неэффективной коррекцией углеводного обмена или недиагностированным диабетом, ассоциируется с высокой смертностью и значительными расходами на лечение. Проведенный ретроспективный анализ карт пациентов с СД 1 типа и рецидивирующим диабетическим кетоацидозом (ДКА), которые начали использовать вышеупомянутую систему флэш-мониторинга, показал снижение частоты событий ДКА в среднем до 0,2 случая на человека в течение 2 лет по сравнению с 2,9 эпизода за тот же срок у больных, измерявших уровень глюкозы обычным способом, а также уменьшение тяжести данного осложнения.
В эпоху современных технологий разработка интеллектуальных устройств, таких как системы НМГ, помогает пациентам с диабетом легче и чаще контролировать уровень глюкозы. При оценке эффективности использования НМГ у 67 молодых пациентов с СД 1 типа в течение 6 месяцев:
- 95,5 % указали, что применение датчика вызывает меньшую боль, чем обычный прокол пальца;
- 85,0 % ощущали больший комфорт с установленным датчиком;
- 94,0 % согласились, что небольшой его размер облегчает ношение;
- 47,8 % утверждали, что ношение датчика не привлекает внимания;
- 70,1 % сообщили об отсутствии дискомфорта под кожей;
- 80,6 % заявили, что датчик можно сканировать незаметно от окружающих;
- 89,6 % считали, что он не влияет на их повседневную деятельность;
- 91,0 % отмечали, что датчик совместим с их образом жизни;
- 79,1 % сообщили о легкости измерения уровня гликемии при сканировании;
- 76,1 % участников с удовольствием делились с другими людьми опытом использования системы. Сравнение традиционного метода самоконтроля уровня глюкозы в крови и НМГ с помощью флэш-мониторинга продемонстрировало, что последний менее болезнен, он незаметнее, удобнее, проще в применении, быстрее в измерении гликемии, более приватен и причиняет минимум неудобств.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
Поздние осложнения могут вызывать негативные психосоциальные эффекты. В проспективном когортном исследовании, проведенном в Саудовской Аравии, изучались психосоциальные преимущества, ассоциированные с 3‑месячным использованием флэш-мониторинга уровня глюкозы у 95 больных СД 1 типа. Пациенты анкетировались согласно шкале диабетического дистресса (DDS) и Питтсбургскому индексу качества сна (PSQI). У всех субъектов наблюдалось значительное снижение средних показателей DDS (3,8 против 2,5) и PSQI (8,7 против 3,9) через 3 месяца по сравнению с исходным уровнем. Кроме того, уровень HbA1c и количество подтвержденных эпизодов гипогликемии снизились по сравнению с исходными значениями (HbA1c 8,3 против 7,7 %; эпизодов гипогликемии — 3,0 против 2,3). Средняя частота измерения уровня глюкозы в крови в день, напротив, возросла по сравнению с исходным уровнем (5,2 против 2,5). Эти данные демонстрируют улучшение показателей компенсации углеводного обмена и качества сна после 3‑месячного использования НМГ у молодых пациентов с СД 1 типа.
Проведенное в Италии проспективное исследование ставило целью сравнение эффективности НМГ с помощью флэш-системы и глюкометра у взрослых пациентов с СД 2 типа, находящихся на лечении инсулином в госпитальных отделениях общего профиля. По сравнению с капиллярным измерением флэш-мониторинг продемонстрировал более низкий среднесуточный уровень гликемии и более высокую выявляемость гипогликемических событий, особенно ночных и длительных.
Интересны данные японского 90‑дневного исследования влияния НМГ с помощью описываемой системы на гликемический контроль у 94 пациентов с СД 2 типа, получавших базисно-болюсную ИТ. Первичной конечной точкой была исходная продолжительность гипогликемии (ниже 70 мг/дл) по сравнению с концом исследования. Время в состоянии гипогликемии было непродолжительным на исходном уровне (0,51 ± 0,93 часа в день) и существенно не уменьшилось в конце исследования (0,47 ± 0,63 часа в день), однако время в целевом диапазоне, в состоянии гипергликемии и расчетный НвA1c изменились по сравнению с исходным уровнем (на +1,7 ± 3 часа в день, –1,6 ± 0,4 часа в день и –0,4 ± 0,8 % соответственно). Число проколов пальца для измерения гликемии сократилось с 2,9 ± 1,3 до 1,9 ± 1,4 в день, а средняя частота сканирования составила 11,3 измерения в сутки. Средний балл удовлетворенности возрос на 11,8 ± 5,3.
Проведенное в Испании в 2020 году изучение стоимости НМГ при помощи системы FreeStyle Libre 2 с традиционным СКГК у взрослых с СД 1 типа показало снижение частоты тяжелой гипогликемии при использовании НМГ на 58,6 %. Ежедневное потребление полосок и ланцетов составляло 9 штук у пациентов с СКГК (до и после четырех ежедневных инъекций и перед сном) и 0,5 — для пользователей флэш-мониторинга. Учитывалось годовое потребление 26 датчиков флэш-мониторинга (один каждые 14 дней). Общая годовая стоимость на одного пациента составила 4437 евро для группы традиционного самоконтроля и 2526 евро — для НМГ. Использование НМГ ассоциировалось с ежегодной экономией затрат на мониторинг и лечение гипогликемических событий в размере 1911 евро на пациента в год. В гипотетической когорте из 1 тыс. пациентов с СД 1 типа на НМГ удалось избежать 4900 первичных и 93 повторных госпитализаций в год, суммарная экономия в исследуемой группе составила от 370 тыс. до 1,76 млн евро. Таким образом, использование системы НМГ уменьшает количество гипогликемических событий и приводит к экономии средств системы здравоохранения.
В литературе появились описания клинических случаев, подтверждающих необходимость использования НМГ в периоперационном периоде. Удается быстро скорректировать дозу инсулина в соответствии с уровнем глюкозы перед операцией и предотвратить длительную гипогликемию во время ее проведения и в послеоперационном периоде.
А ЕСЛИ ВАКЦИНАЦИЯ?
Сейчас во всем мире осуществляется программа вакцинации против COVID‑19, после которой часть пациентов с СД 1 типа сталкиваются с временной нестабильностью уровня глюкозы в крови в течение 2–3 дней. Появились сообщения об анализе профилей гликемии пациентов с СД 1 типа до и после вакцинации при применении упомянутого выше флэш-мониторинга глюкозы. После вакцинации в течение недели наблюдалось значительное снижение целевого уровня гликемии крови и не отмечалось значимых изменений ее вариабельности. Изменение гликемии в течение недели после вакцинации было наиболее выражено у пациентов, получавших метформин/дапаглифлозин вместе с базально-болюсным режимом ИТ (–23 %) по сравнению с получающими только инсулин (–4 %); большее снижение целевого значения гликемии регистрировалось у пожилых людей (–18 против –9 %).
Традиционный гликемический контроль не является оптимальным для многих пациентов с СД 2 типа. Хотя использование НМГ продемонстрировало снижение НвA1с у больных с СД 2 типа, получавших несколько ежедневных инъекций инсулина или его введение с помощью инсулиновой помпы, эффект данной технологии у пациентов с СД 2 типа, использующих неинтенсивные схемы лечения, изучен недостаточно. В ретроспективном наблюдательном исследовании на базе данных IBM Explorys после применения системы FreeStyle Libre для НМГ у 1034 взрослых с субоптимально контролируемым СД 2 типа, получавших неинтенсивную терапию, отмечалось значительное снижение уровня НвA1с внутри всей когорты: с 10,1 ± 1,7 до 8,6 ± 1,8 %; наибольшее снижение наблюдалось у пациентов с исходным уровнем НвA1с ≥ 12,0 % (n = 181, снижение НвA1с –3,7 %). Значительное снижение отмечалось в группах лечения базальным инсулином — на 1,1 %, пероральной терапией — на 1,6 %. Эти результаты свидетельствуют о расширении возможностей и доступа к флэш-мониторингу пациентов с СД 2 типа.
Таким образом, использование флэш-мониторинга гликемии с современной удобной и доступной облачной платформой и веб-интерфейсом весьма перспективно и требует внедрения у пациентов с СД как первого, так и второго типа. Такое внедрение меняет парадигму в сфере управления СД, координации усилий врача и больного, открывая широкие горизонты для успешной коррекции углеводного обмена и улучшения качества жизни пациентов.
Читайте также
- Новое мышление в терапии сахарного диабета 2 типа
- Диабет и вакцинация против COVID‑19: что важно не упустить из виду?
- Поиск инноваций или доверие опыту?
- Самоконтроль глюкозы крови в современных условиях
- Автономная полинейропатия — подводный айсберг диабета
- Принятие клинических решений на основе непрерывного мониторинга
- Разные проблемы — одно решение
- Николай Михайлович Иценко: у истоков нейроэндокринологии

















