Статьи
Терапия гемофилии А в XXI веке: обзор современных подходов и их эффективности
Гемофилия А — наиболее распространенная форма гемофилии — представляет собой наследственное нарушение свертываемости крови, обусловленное дефицитом или отсутствием фактора VIII (FVIII). По данным Всемирной организации здравоохранения, гемофилия А встречается у одного из 5 тысяч новорожденных мальчиков.
Из-за частых кровоизлияний пациенты страдают от хронической боли и повреждений суставов, что ограничивает их подвижность, ведет к инвалидности со значительными социальными и экономическими потерями. Хотя традиционные методы лечения, включающие регулярные инъекции фактора VIII, и эффективны, но все же они имеют ряд ограничений, таких как развитие ингибиторов и необходимость частого введения препарата. Лечение гемофилии А в наши дни претерпело значительные изменения, направленные на улучшение качества жизни пациентов.
СОВРЕМЕННЫЕ ПОДХОДЫ К ТЕРАПИИ ГЕМОФИЛИИ А
1. Заместительная факторная терапия (ЗФТ) Осуществляется препаратами FVIII в виде регулярных инфузий для предотвращения и контроля кровотечений.
Существует два типа препаратов для заместительной терапии:
• плазменные концентраты FVIII, получаемые из донорской крови;
• рекомбинантные концентраты FVIII, синтезируемые с помощью генной инженерии.
В 2014 году Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) был зарегистрирован эфмороктоког альфа—первый препарат с увеличенным периодом полувыведения. С этого момента рекомбинантные концентраты FVIII подразделяют на препараты со стандартным и пролонгированным периодом полувыведения (около 12 и 19 часов соответственно).
В 2023 году FDA зарегистрировало еще один пролонгированный препарат — эфанесоктоког альфа, молекула которого дополнительно включает фрагмент белка фон Виллебранда и полипептиды XTEN для увеличения периода полувыведения примерно до 43–48 часов у взрослых.
Несмотря на то что концентраты FVIII содержат выделенные из крови или же генетически модифицированные молекулы фактора свертывания, они не обеспечивают физиологический гемостаз. В норме концентрация факторов свертывания крови (ФСК) поддерживается на постоянном уровне благодаря механизмам обратной связи и регуляции синтеза FVIII в печени. Это обеспечивает готовность организма к быстрому реагированию на повреждения и предотвращению кровотечений.
Введение концентратов ФСК при гемофилии не позволяет поддерживать их естественный уровень: первоначально созданная высокая концентрация затем падает до критически низких значений. Вот почему ученые направили усилия на разработку методов терапии с более стабильными концентрациями препаратов в крови, чтобы обеспечить гемостаз, приближенный к физиологическому.
2. Нефакторная терапия
Нефакторные препараты представляют собой новый класс лекарств, которые не содержат FVIII, но помогают предотвращать кровотечения за счет воздействия на разные этапы гемостаза.
• Миметики FVIII
Самым первым препаратом для нефакторной терапии в целом и миметиком FVIII, в частности, стал эмицизумаб. Это биспецифическое антитело (АТ), имитирующее действие FVIII, связывает активированные факторы IX и X, что позволяет обойти дефицит FVIII. Сегодня эмицизумаб — наиболее изученный и широко применяющийся препарат нефакторной терапии — заменил в некоторых странах ЗФТ, став стандартом лечения тяжелой формы гемофилии А. Так, например, во Франции 72 % пациентов с гемофилией А без ингибиторов получают терапию эмицизумабом. В Великобритании это число достигает 67 %, Бельгии — 69 %, Австралии—85 %. В Новой Зеландии 9 из 10 пациентов с тяжелой формой гемофилии А без ингибиторов получают эмицизумаб.
Столь широкое распространение эмицизумаба обусловлено его превосходящей эффективностью при равной безопасности по сравнению с факторной терапией. В метаанализе рандомизированных клинических исследований А. Reyes и соавт. показали, что профилактика эмицизумабом на 97,8 % превосходит по эффективности препараты FVIII как со стандартным, так и пролонгированным периодом выведения.
Mim8 — второе биспецифическое АТ, имитирующее активированный FVIII и предназначенное для лечения гемофилии А. В клинических испытаниях программы FRONTIER было показано, что еженедельное и ежемесячное введение Mim8 снижает число кровотечений на 97–99 % у никогда не получавших профилактическое лечение и на 43–48 % — у проходивших ранее профилактику препаратами FVIII. В исследованиях не было зарегистрировано серьезных тромботических событий или образования антител против Mim8. Сейчас Mim8 проходит III фазу клинических испытаний.
NXT007—еще одно биспецифическое АТ с аналогичным механизмом действия— сегодня находится в разработке. В доклинических исследованиях было показано, что NXT007 способен поддерживать гемостаз, сопоставимый таковым у тех, кто не страдает гемофилией. Сейчас NXT007 проходит клинические испытания II фазы с оценкой его фармакокинетики и фармакодинамики, а также безопасности и переносимости.
• Ингибиторы пути тканевого фактора
Концизумаб и марстацизумаб — моноклональные АТ, блокирующие связывание TFPI с активированным фактором X. Исследования III фазы показали, что применение концизумаба приводит к значительному (на 86 %) снижению числа кровотечений у пациентов с ингибиторами по сравнению с теми, кто не получал профилактическое лечение. Средний годовой уровень кровотечений (ABR) у получавших концизумаб составил 1,7, тогда как у пациентов без профилактики этот показатель составил 11,8. Концизумаб зарегистрирован в Канаде для профилактики кровотечений у пациентов с ингибиторной формой гемофилии В. Марстацизумаб находится в III фазе исследований.
• Блокатор выработки антитромбина
Фитусиран —пока единственный препарат из группы экспериментальной терапии на основе малых интерферирующих РНК (siRNA). Фитусиран снижает синтез антитромбина, что способствует увеличению выработке тромбина и восстановлению гемостаза.
Исследования III фазы показали, что профилактическое лечение фитусираном значительно снижает частоту кровотечений. В работе ATLAS-A/B для пациентов без ингибиторов и ATLAS-INH — с ингибиторами применение фитусирана привело к снижению ежегодной частоты кровотечений на более чем 89 % по сравнению с контрольными группами, использовавшими лечение по требованию. У некоторых участников при применении фитусирана наблюдались повышение уровня ферментов печени (АЛТ и АСТ), учащение эпизодов инфекции верхних дыхательных путей, а также насморк, боль в животе, кашель и головная боль. Серьезных тромбоэмболических событий не зарегистрировано. Исследования фитусирана окончены, но препарат пока не зарегистрирован к применению.
3. Генная терапия гемофилии А
Это перспективное направление терапии гемофилии А. Клинические исследования показывают обнадеживающие результаты, позволяя надеяться на долгосрочное решение проблемы.
Валоктокоген роксапарвовек показал высокую начальную активность FVIII, которая, однако, со временем снизилась с медианы 23,9 % через 52 недели до медианы 8,3 % через 156 недель. Тем не менее годовая частота кровотечений значимо сократилась, что подчеркивает эффективность препарата в профилактике кровотечений. Гироктокоген фителпарвовек в ходе исследований также продемонстрировал тенденцию к снижению активности FVIII с медианы 20,1 % через 52 недели до медианы 12,5 % через 156 недель.
Дирлоктокоген самопарвовек обнаружил не столь высокую, но стабильную активность FVIII в течение всего периода наблюдения (медиана 8,0 % через 52 недели и 7,5 % — через 156 недель) и значительное снижение частоты кровотечений с медианы 8,5 % до 0,3 %, что делает его перспективным вариантом для долгосрочной терапии.
Наиболее часто встречающимися нежелательными реакциями в исследованиях генной терапии гемофилии А были повышение трансаминаз, тошнота, реакция в месте введения и головная боль. Частота реакций варьировалась в зависимости от препарата: повышение АСТ регистрировалось максимально часто при применении валоктокоген роксапарвовека — 85,6 %, в 72,7 % случаев — при применении гироктокоген фителпарвовека и в 39,0 % — при применении дирлоктокоген самопарвовека.
Из указанных препаратов генной терапии зарегистрирован к применению валоктокоген роксапарвовек, остальные находятся на разных стадиях исследований.
ОБЕСПЕЧЕНИЕ ПАЦИЕНТОВ
Россия относится к числу стран, полностью покрывающих потребности в препаратах всех пациентов с гемофилией А за счет федеральных программ. С 2006 года все больные гемофилией в РФ (и дети, и взрослые) обеспечиваются бесплатными препаратами — сначала по программе дополнительного лекарственного обеспечения, а затем в рамках государственной программы «7 нозологий», стартовавшей в 2008 году и в 2019-м расширенной до «12 нозологий».
Фонд «Круг добра», обеспечивающий потребности в терапии детей с орфанными заболеваниями, с 2023 года взял на себя соответствующие обязательства и в отношении детей с гемофилией. Это позволяет маленьким пациентам с гемофилией А получать инновационное лечение, значительно снижающее риск развития артропатии и инвалидизации, а значит, улучшить их социализацию.
Лечение гемофилии А в XXI веке должно быть направлено на обеспечение гемостаза, приближенного к физиологическому, чтобы обеспечить пациенту не только защиту от кровотечений, но и качество жизни, сравнимое с таковым в общей популяции. Список литературы находится в редакции.
ЧТО СКАЗАТЬ РОДИТЕЛЯМ
Гемофилия — генетически обусловленное орфанное заболевание, характеризующееся нарушением свертываемости крови. Гемофилия A связана с мутациями в гене, кодирующем синтез фактора свертывания крови VIII (FVIII), который еще называют антигемофильным глобулином. Ген FVIII расположен на X-хромосоме. Мутации в нем обычно передаются по наследству, но иногда возникают спонтанно, то есть без предшествующих случаев заболевания в семье. Гемофилия А встречается значительно чаще других коагулопатий (80–85 % общего числа случаев), в том числе гемофилии B, которая ассоциирована с мутацией в гене, кодирующем синтез фактора свертывания крови IX (FIX).
В качестве самостоятельного заболевания гемофилия впервые была описана американским врачом Джоном Конрадом Отто в 1803 году. Он охарактеризовал ее как врожденную патологию с сопутствующими кровотечениями, которая поражает только мужчин, передаваясь им от здоровых матерей — носителей гемофилии. Однако, хотя и крайне редко, в мировой литературе фиксируются случаи гемофилии у девочек — примерно 60 таких эпизодов за всю историю. Согласно ежегодному отчету Всемирного фонда гемофилии за 2022 год, в мире насчитывается более 250 тыс. пациентов с различными формами этого заболевания, а в России, по данным Минздрава, с таким диагнозом живут около 9 тыс. человек.
Впервые в письменных источниках о гемофилии упоминается в Вавилонском талмуде — священной книге иудеев, записанной около 1500 лет назад. В нем содержатся сведения об иудейском мальчике, которому не стали проводить обряд обрезания, поскольку оба его старших брата и трое двоюродных по материнской линии умерли от кровотечения после данной процедуры.
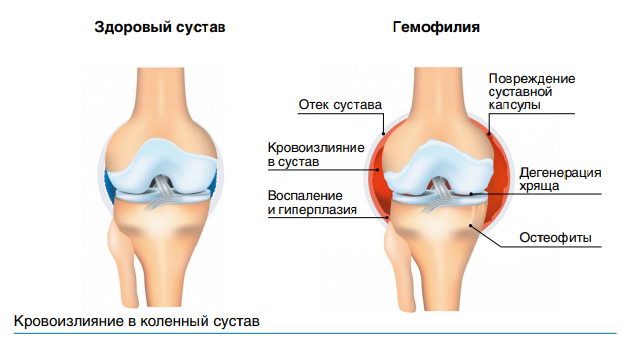
В подобных кровотечениях и состоят основной признак и опасность гемофилии. Возникающие в результате незначительных травм или же вообще без видимой причины обильные кровотечения или кровоизлияния в суставы, мягкие ткани и внутренние органы, повторяясь регулярно, могут привести к серьезным повреждениям суставов вплоть до их деформации и нарушения подвижности, а также вызывать хроническую боль, что в конечном итоге заканчивается инвалидизацией. Больному гемофилией противопоказаны хирургические вмешательства за исключением тех, что осуществляются по жизненным показаниям и при полном обеспечении препаратами, восстанавливающими свертываемость крови.
Для расширения осведомленности населения планеты об этом заболевании проводится Всемирный день гемофилии. Каждый год он проходит под разными лозунгами: «Учтите и меня», «Твоя помощь нам очень нужна», «Лечим вместе» и т.д. В этом году его девиз звучал так: «Равный доступ для всех — признание всех форм нарушений свертываемости крови». Идея состоит в том, что все люди с наследственными нарушениями свертываемости крови должны иметь равный доступ к медицинской помощи, независимо от типа этого нарушения, пола, возраста или места проживания.
Всемирный день гемофилии в России отмечается с 1996 года, а в 2000 году было создано Всероссийское общество гемофилии (ВОГ), в состав которого входят 72 региональные организации из всех федеральных округов. Распространенность заболевания в нашей стране в целом оценивается как 1:10 000 человек. Но, возможно, это лишь верхушка айсберга. По данным на 2022 год диагноз «гемофилия» в мировом масштабе был подтвержден более чем у 257 тысяч пациентов, и еще 100 тысяч человек страдали болезнью Виллебранда (раньше ее обозначали как гемофилию С) — нарушением свертываемости крови из-за недостаточной активности одноименного фактора, который участвует в адгезии тромбоцитов на коллагене и защищает FVIII от протеолиза. Однако некоторые данные позволяют считать, что гемофилия все еще недостаточно диагностирована и фактическое население мира, страдающее данным заболеванием, может составлять более 1,1 млн человек.


















