Статьи
Влияние препарата Регастим Гастро на слизистую оболочку желудка при хроническом атрофическом гастрите, ассоциированном с Helicobacter pylori
Проблема гастрита не теряет своей актуальности. Прогресс в изучении формирования самой патологии и подходов к ее лечению пока не дает окончательных ответов на существующие вопросы. Несмотря на десятилетия исследований и клинической практики, основные проблемы, связанные с эффективностью и безопасностью лечения, остаются не определенными.
Вопреки заблуждению не только пациентов, но ряда врачей о том, что гастрит является привычным воспалением слизистой оболочки желудка (СОЖ), встречающимся у большинства людей и приносящим лишь неприятные ощущения в зоне эпигастрия, сегодня установлено, что это опасное, прогрессирующее без лечения заболевание служит фактором риска развития рака желудка (РЖ).
По данным исследования GLOBOCAN — 2020, подготовленным Международным агентством по изучению рака (МАИР), общая заболеваемость злокачественными новообразованиями (ЗНО) увеличивается с каждым годом. Так, в 2020 году в мире было зарегистрировано 19,3 млн новых случаев ЗНО (18,1 млн без учета немеланомного рака кожи) и почти 10 млн случаев смерти от онкологической патологии (9,9 млн без учета немеланомного рака кожи). На РЖ приходилось 5,6 %. Ожидается, что к 2040 году мировая заболеваемость ЗНО составит 28,4 млн случаев, что на 47 % больше, чем в 2020-м. Немалая доля придется непосредственно на РЖ. Это пятый по встречаемости вид рака и третья по распространенности причина смерти от онкологических заболеваний в мире.
К хроническим гастритам относят группу заболеваний, характеризующихся воспалительным процессом в СОЖ с нарушением клеточного обновления и, как следствие, развитием атрофии, кишечной метаплазии и эпителиальной дисплазии. В связи с длительным разрушением нормальной клеточной структуры желудка вследствие воспаления уменьшение количества желез, а также дисфункция клеток желудка в конечном итоге приводят к сокращению функционально активной СОЖ.

ЭТИОЛОГИЧЕСКИЙ ФАКТОР
Этиологическим фактором самой распространенной формы гастрита является Helicobacter pylori (H. pylori) — грамотрицательная спиралевидная бактерия, колонизирующая СОЖ и выявляющаяся у подавляющего большинства взрослого населения. Инфицирование H. pylori часто происходит в раннем детстве, и при отсутствии лечения хеликобактериоз прогрессирует. По данным литературы, хотя охват поражением H. pylori и имеет очевидную тенденцию к снижению, в среднем он составляет 45 % взрослого населения (в зависимости от региона России).
Несмотря на повышенное внимание, уделяемое данной патологии, широкая распространенность H. pylori все еще остается серьезной проблемой для здравоохранения всего мира. Но в то же время она служит важным инициирующим и стимулирующим этапом в процессе желудочного канцерогенеза. У пациентов, инфицированных H. рylori, более высокий риск развития рака по сравнению с неинфицированными.
В эксперименте с монгольскими песчанками была воспроизведена модель формирования РЖ под влиянием H. pylori — каскад Корреа, включающий последовательные стадии изменений со стороны СОЖ: атрофический гастрит, кишечная метаплазия, дисплазия, неоплазия. Согласно каскаду Корреа, РЖ в своем развитии проходит через серию описанных выше изменений. Прогрессирование поверхностного гастрита и трансформация его в РЖ занимают длительное время. Это многоэтапный мутационный процесс. Клинико-патологическую модель РЖ можно охарактеризовать как множество последовательных стадий: от поверхностного до хронического атрофического гастрита (ХАГ) с формированием кишечной метаплазии СОЖ, с последующим развитием на этом фоне интраэпителиальной неоплазии, аденом желудочного и кишечного типа, РЖ. Этот процесс можно разделить на четыре этапа.
Разновидностью ХАГ является аутоиммунный атрофический гастрит (ААГ), также известный как гастрит типа А, который представляет собой органоспецифическое заболевание, приводящее к атрофии СОЖ из-за иммуноопосредованного разрушения. ААГ имеет гендерную специфику с разными клиническими проявлениями у женщин и мужчин. Например, железодефицитная анемия (ЖДА) более характерна для первых, а пернициозная анемия чаще возникает у вторых, что во многом связано с курением.
Данные длительной клинической практики лечения гастрита, вызванного H. рylori, показали, что эрадикация возбудителя снижает риск последующего развития рака. Выживание H. pylori в агрессивной среде желудка возможно благодаря действию различных факторов, влияние которых приводит к вероятности ее колонизации и формированию активной воспалительной реакции СОЖ. Со временем воспалительный процесс приводит к необратимым изменениям, сопровождающимся, как упоминалось выше, сокращением числа желез и их перерождением. В то же время тяжелая атрофия СОЖ рассматривается как точка невозврата в каскаде Корреа.
НУЖНА ЭРАДИКАЦИЯ
На ранней стадии ХАГ пациенты, как правило, не имеют специфических симптомов. Иногда больного могут беспокоить вздутие верхней части живота, болезненные ощущения, потеря аппетита и тошнота. При ХАГ, вызванном инфекцией H. pylori, также могут наблюдаться гастроэзофагеальный рефлюкс, ЖДА и другие осложнения, включая нарушения костного метаболизма. Риск развития ХАГ примерно в 2,4 раза выше у инфицированных H. pylori по сравнению с неинфицированными.
В результате появления убедительных доказательств влияния H. pylori на развитие и прогрессирование ХАГ возникла возможность терапевтического воздействия на непосредственную причину заболевания. Первостепенным в лечении хронического гастрита считается проведение эрадикационной терапии с учетом предварительного положительного тестирования на инфекцию H. pylori.
Однако после формирования атрофии СОЖ риски развития РЖ сохраняются даже после эрадикации H. рylori. Для достижения положительных результатов в лечении данной патологии необходимо максимально раннее выявление атрофии, а также применение дополнительных терапевтических подходов, способствующих восстановлению функционирования и структуры СОЖ. Несмотря на растущую распространенность ХАГ и его возрастающее влияние на глобальное здоровье человека, вопрос о поиске наиболее эффективных методов лечения все еще остается открытым. Исследования патологических характеристик ХАГ и идентификация терапевтических мишеней неуклонно продвигаются вперед.
РЕТРОСПЕКТИВНОЕ ИССЛЕДОВАНИЕ
В ретроспективном исследовании типа «случай—контроль» были отобраны 15 историй болезней пациентов с ХАГ, ассоциированным с H. рylori. Всем обследуемым выполняли видеоэзофагогастродуоденоскопию с быстрым уреазным биохимическим тестом на H. рylori, а также проводили стандартную пятиточечную диагностическую биопсию СОЖ. Образцы окрашивали гематоксилином и эозином, оценивали выраженность воспаления, активность, атрофию и систематизировали данные по классификации OLGA. При отсутствии признаков воспаления, активности и атрофии присваивали значение 0, при наличии признака — от 1 до 3 согласно методике. Выборочно, в сомнительных случаях, биоптаты окрашивали по Гимзе для уточнения наличия H. рylori. При выявлении неопластических изменений СОЖ определяли их степень согласно классификации Всемирной организации здравоохранения (ВОЗ, 2019).
На первом этапе лечения всем пациентам назначалась стандартная эрадикационная квадритерапия H. рylori с использованием препарата висмута, блокатора протонной помпы и двух антибактериальных лекарственных средств. Схемы лечения могли отличаться в зависимости от индивидуальной переносимости препаратов, сведений о ранее назначавшихся антибиотиках. В ходе второго этапа лечения всем пациентам назначался препарат Регастим Гастро (два курса по 30 дней каждый в стандартной дозировке). После лечения в интервале от 1 до 3 месяцев пациентам выполнялась контрольная эзофагогастродуоденоскопия (ЭГДС) с биопсией по описанной выше методике. Оценивались эффективность эрадикационной терапии H. рylori, динамика воспалительных и атрофических изменений СОЖ.
Наиболее частые изменения, выявленные в СОЖ пациентов, а также их динамика после лечения представлены в таблице.
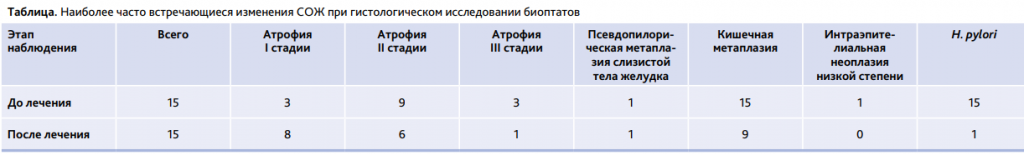
Проведенный анализ показал, что в большинстве случаев после успешной эрадикационной терапии инфекции H. рylori отмечается регресс выраженности атрофических изменений, также в некоторых случаях при повторном гистологическом исследовании не выявлялись признаки кишечной метаплазии, фиксировавшиеся ранее. Обращает на себя внимание случай атрофического гастрита с интраэпителиальной неоплазией низкой степени, который отмечался при сочетанном поражении СОЖ. В данном случае имелась как инфекция H. рylori, так и аутоиммунные нарушения, высокоспецифичными для которых является поражение слизистой оболочки тела желудка с формированием ее псевдопилорической метаплазии. При этом на фоне лечения отмечалась успешная эрадикация, однако сохранилась выраженная атрофия СОЖ III стадии. Однако имевшаяся у данного пациента интраэпителиальная неоплазия низкой степени регрессировала, что также говорит об успешности проведенной терапии. В литературе имеются разные данные об успешности лечения атрофических гастритов и устойчивости полученных положительных результатов, а также их влиянии на снижение риска формирования РЖ. Не исключено, что это зависит от особенностей канцерогенеза среди различных групп населения в разных регионах мира, а также длительности наблюдения и возможностей гастропротективной терапии.
Дальнейшие исследования должны быть посвящены расширению группы наблюдения, а также сравнению с пациентами, не получающими лечение или прошедшими только эрадикационную терапию H. рylori. Данный анализ подтвердил эффективность препарата Регастим Гастро в лечении атрофического гастрита и возможность регресса ранних интраэпителиальных неопластических изменений на фоне терапии. Совокупность научных данных об эффективности применения препарата может лечь в основу обоснования его включения в клинические рекомендации по данной нозологии.
Список литературы находится в редакции
Читайте также
- Новый международный консенсус RE.GA.IN.: диагностика и лечение гастрита в реальной клинической практике
- Хронический гастрит, ассоциированный с Helicobacter pylori
- Загадка аутоиммунного гастрита
- Серологическая диагностика хронического гастрита
- А есть ли симптомы у гастрита?
- Эозинофильный гастроэнтерит: что нам о нем известно?


















