Статьи
Загадка аутоиммунного гастрита
Диагноз «гастрит» очень часто устанавливается и в нашей стране, и во всем мире тоже. В большинстве случаев причиной воспаления в слизистой оболочке желудка (СОЖ) становится инфекция, вызываемая Helicobacter pylori. Современные схемы лечения такого гастрита крайне эффективны, понятны, достаточно безопасны. Но существуют другие причины хронического гастрита, такие как, например, аутоиммунный процесс, о котором пойдет речь в этой статье.
ЭТИОЛОГИЯ НЕИЗВЕСТНА
Аутоиммунный гастрит (АИГ) — иммуноопосредованное заболевание неизвестной этиологии, при котором вследствие аутоиммунного процесса происходят гибель кислотопродуцирующего эпителия, атрофия и метаплазия слизистой оболочки тела и дна желудка, приводящие к ахлоргидрии, нарушению продукции внутреннего фактора Касла, развитию железодефицитной и В12-дефицитной анемии, повышению риска развития нейроэндокринных опухолей и рака желудка.
Важно, что симптомы со стороны желудочно-кишечного тракта (ЖКТ) при АИГ неспецифичны или отсутствуют вовсе, а диагноз устанавливается, как правило, на запущенных стадиях заболевания, когда вследствие ахлоргидрии и отсутствия внутреннего фактора Касла развивается тяжелая, рефрактерная к лечению железодефицитная и/или В12-дефицитная анемия, а также другие проявления дефицита витамина В12.
РЕДКОЕ ЗАБОЛЕВАНИЕ
АИГ расценивается как крайне редкое заболевание, диагноз которого обычно устанавливают при выяснении причины анемии. Однако в последние годы наблюдается отчетливая тенденция к росту числа пациентов с данным диагнозом. Пока не ясно, связано ли это с истинным увеличением заболеваемости или с улучшением диагностики АИГ. Достоверных данных о частоте АИГ в популяции (в том числе в России) нет.
Считается, что истинная распространенность АИГ недооценена вследствие невыраженной клинической картины, в случае же развития анемии на фоне АИГ лечение часто проводится без выяснения причины ее возникновения. Кроме того, АИГ нередко протекает в сочетании с гастритом, ассоциированным с H. pylori, что также снижает вероятность установления диагноза. По приблизительным оценкам, распространенность АИГ в популяции составляет около 0,5–4,5 %.
Женщины страдают этой патологией в 2–3 раза чаще, чем мужчины, а пик заболеваемости приходится на периклимактерический период. Однако в последние годы наблюдается отчетливая тенденция к омоложению АИГ, нередко он манифестирует у женщин после процедур экстракорпорального оплодотворения и гормональной терапии.
КЛИНИЧЕСКАЯ КАРТИНА
Жалобы со стороны ЖКТ при АИГ крайне неспецифичны и обусловлены нарушением секреции соляной кислоты в желудке (гипои ахлоргидрия), замедлением его моторики, развитием избыточного бактериального роста. У пациентов могут наблюдаться тяжесть после еды, тошнота, отрыжка, снижение аппетита, вздутие и бурление в животе, диарея и запор.
Нередкими симптомами, побуждающими больных обращаться к врачу, являются стойкая изжога, жжение языка, ощущение горького или кислого вкуса во рту. Данные жалобы обычно расцениваются как проявление гастроэзофагеальной рефлюксной болезни (ГЭРБ), однако терапия ингибиторами протонной помпы (ИПП) у таких пациентов оказывается неэффективной. Они годами проходят обследования в поисках причин мучительных ощущений в полости рта: меняют зубные пасты и протезы, полощут рот, применяют местные анестетики, принимают антидепрессанты, но причина, как правило, кроется в парестезии — расстройстве чувствительности соответствующих нервных окончаний и волокон на фоне дефицита витамина В12.
Чаще всего пациенты с АИГ попадают на прием к врачу с жалобами, обусловленными развитием тяжелой железодефицитной (ЖДА) и/или В12-дефицитной анемии. ЖДА возникает у 25–50 % больных АИГ и обычно предшествует развитию В12-дефицитной анемии. Особенностью ЖДА при АИГ является рефрактерный характер течения и резистентность к терапии пероральными формами железа. Часто пациенты годами или десятилетиями наблюдаются у врача, принимают препараты железа, обследуются, однако так и не находят причины анемии.
По современным данным, в 15–27 % случаев причиной необъяснимой и рефрактерной к лечению ЖДА является именно АИГ. Отсутствие очевидных причин анемии при ЭГДС (не выявлены эрозии, язвы, кровоточащие полипы, опухоли) должно стать поводом к серологической диагностике АИГ.
Дефицит витамина В12 при АИГ развивается вследствие гибели париетальных клеток желудка, синтезирующих соляную кислоту (без которой высвобождение витамина В12 из связи с белками пищи затруднено) и внутренний фактор Касла (без которого всасывание витамина В12 в подвздошной кишке практически невозможно).
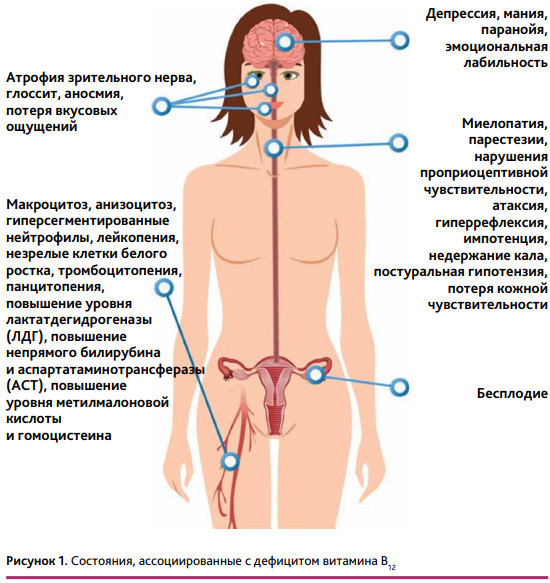
Клинически анемия при АИГ проявляется бледностью и желтушностью (при мегалобластной анемии) кожных покровов, слабостью, головокружением, мельканием мушек перед глазами, выпадением волос, ломкостью ногтей, одышкой. Необходимо помнить, что, помимо изменений в крови, дефицит витамина В12 приводит к развитию тяжелых неврологических и психоэмоциональных расстройств (рис. 1): онемению, парестезиям, нарушению проприоцептивной и вибрационной чувствительности, пошатыванию при ходьбе, синдрому беспокойных ног, нарушению обоняния, снижению концентрации внимания, памяти, астеническим, депрессивным и другим аффективным расстройствам, нарушениям сна.
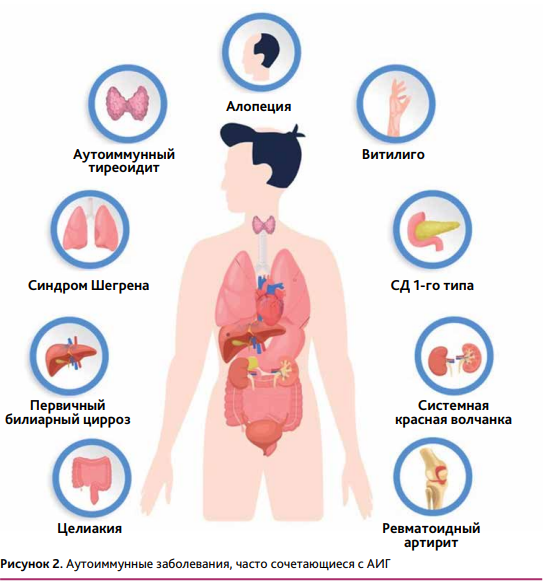
Пациенты с АИГ в более чем в половине случаев страдают другими аутоиммунными заболеваниями, такими как аутоиммунный тиреоидит, сахарный диабет (СД) 1-го типа, витилиго, синдром Шегрена, ревматоидный артрит, системные заболевания соединительной ткани, целиакия, первичный склерозирующий холангит, аутоиммунный гепатит, болезнь Аддисона и др. (рис. 2). У пациента с аутоиммунным тиреоидитом высока вероятность обнаружения АИГ, и, наоборот, если пациенту впервые установлен диагноз «аутоиммунный гастрит», рекомендуется провести скрининг (анализ крови на АТ к тиреопероксидазе и тиреоглобулину) для исключения аутоиммунного тиреоидита.
ОСОБЕННОСТИ ДИАГНОСТИКИ
При наличии клинических признаков, позволяющих заподозрить АИГ, диагноз может быть подтвержден с помощью ЭГДС с забором биоптатов из тела и антрального отдела желудка, серологических исследований (определение АТ к париетальным клеткам, внутреннему фактору Касла, уровня пепсиногена-1 и пепсиногена –2, гастрина-17).
Основными эндоскопическими признаками АИГ являются:
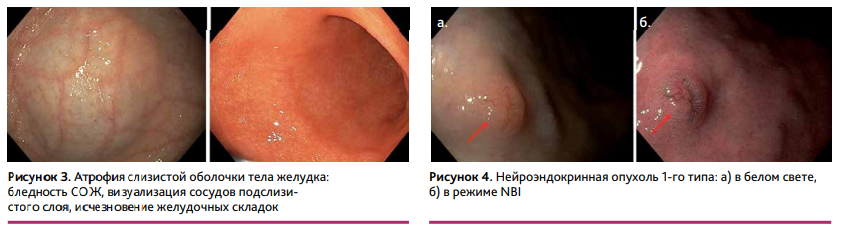
- Атрофия слизистой оболочки тела желудка: бледность СОЖ, визуализация сосудов подслизистого слоя, исчезновение желудочных складок (рис. 3). При сочетании АИГ и гастрита, ассоциированного с H. pylori, в антральном отделе могут выявляться эрозии, эритема, признаки атрофии и КМ.
- Кроме атрофии в теле желудка при АИГ выявляются самые разнообразные изменения: псевдопилорическая и кишечная метаплазия (КМ), гиперпластические полипы, фовеолярная гиперплазия, белые шаровидные и гломусоподобные образования, аденомы желудочного и кишечного типа.
- И самое важное — атрофия и метаплазия слизистой оболочки тела желудка в условиях ахлоргидрии являются опасным фоном для развития злокачественных новообразований (ЗНО), поэтому поиск эндоскописта должен быть направлен на раннее выявление аденокарциномы желудка и нейроэндокринных опухолей (рис. 4), частота развития которых при АИГ возрастает в несколько раз.
Любое эндоскопическое исследование должно заканчиваться проведением биопсии как минимум из двух отделов желудка (в два разных контейнера): два биоптата из антрального отдела по малой и большой кривизне, один биоптат из угла желудка (необязательный компонент) и два биоптата из тела желудка по малой и большой кривизне (рис. 5). При выявлении в желудке видимых патологических образований (полипов, опухолей, подозрительных на дисплазию очагов и т.п.) биопсия выполняется отдельно из каждого видимого патологического участка.
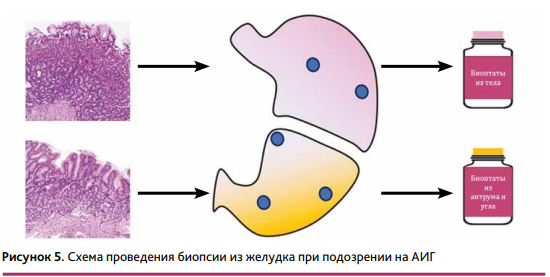
Патологоанатомическое исследование биоптатов из тела желудка при АИГ выявляет лимфоплазмоцитарную инфильтрацию с формированием базальных лимфоидных агрегатов, атрофию кислотопродуцирующего эпителия, псевдопилорическую и полную кишечную метаплазию, панкреатическую метаплазию, гиперплазию нейроэндокринных клеток. Выраженность и распространенность данных изменений зависят от стадии процесса.
Наиболее частыми серологическими изменениями при АИГ являются повышение титра АТ к париетальным клеткам желудка и внутреннему фактору Касла, снижение пепсиногена 1 и соотношения пепсиноген 1/пепсиноген 2, значительное повышение уровня сывороточного гастрина-17. Если диагноз АИГ установлен впервые, рекомендуется направить пациента для лабораторной диагностики аутоиммунного поражения щитовидной железы, поскольку примерно у трети пациентов с АИГ выявляется сопутствующий аутоиммунный тиреоидит. С этой целью используется анализ крови на АТ к тиреоглобулину (АТ-ТГ) и тиреоидной пероксидазе.
Если у пациента заподозрили или уже установили диагноз АИГ, необходимо провести исследование крови для выявления возможного дефицита витамина В12 и ЖДА. Больным с установленным диагнозом АИГ рекомендуется определить уровень витамина В12 в сыворотке крови, даже если очевидных признаков анемии нет. Диагностическим критерием дефицита витамина B12 принято считать его уровень в сыворотке крови < 200 пг/мл (<148 пмоль/л), однако формирование функционального дефицита витамина B12 (возникновение симптомов) возможно уже при уровне кобаламина < 450 пг/мл.
ЛЕЧЕНИЕ АИГ
Этиотропной терапии АИГ пока не существует. Стратегии лечения этого заболевания предполагают проведение эрадикационной терапии при обнаружении инфицирования H. pylori, профилактику и своевременную коррекцию дефицитов витамина В12 и железа, купирование симптомов диспепсии и синдрома избыточного бактериального роста. Диета не играет роли в терапии гастрита, как и применение кислых продуктов и экстрактивных веществ, направленных на повышение кислотности желудочного сока. Считается целесообразным обогащать рацион свежими овощами и фруктами, цельными злаками, питаться небольшими порциями, избегать переедания высокобелковой пищей.
Эрадикационная терапия должна проводиться пациентам с АИГ согласно современным схемам.
Профилактику развития В12-дефицитных состояний нужно начинать с момента установления диагноза АИГ, не дожидаясь развития анемии или неврологических проявлений. Критерием начала терапии препаратами витамина В12 служит снижение уровня кобаламина <450 пг/мл или наличие клинических симптомов дефицита витамина В12 независимо от его сывороточной концентрации. Профилактика и коррекция дефицита витамина В12 могут проводиться парентеральными и пероральными препаратами.
Для лечения клинически выраженного дефицита витамина В12 (уровень <200 пг/мл, анемия, неврологические нарушения) обычно используют его парентеральные формы 500 мкг/сут внутримышечно в первую неделю ежедневно (или 3 раза в неделю), далее—1 раз в неделю до коррекции анемии и регресса/уменьшения выраженности клинических проявлений. В последующем витамин В12 вводят внутримышечно по 500 мкг 1 раз в месяц длительно с профилактической целью. Однако парентеральный режим введения неудобен для пациентов, сопряжен с рисками осложнений. В связи с этим возможно применение пероральных форм витамина В12 в высоких дозах, позволяющих обеспечить пассивное всасывание витамина из просвета кишки.
Восполнение дефицита железа при АИГ— сложная задача, поскольку пероральное железо в условиях ахлоргидрии плохо усваивается из тонкой кишки. Поэтому приоритетным является парентеральное введение препаратов железа. Они назначаются однократно или многократно в соответствии с рекомендациями по применению препарата и тяжестью дефицита.
Обсуждается также возможность назначения пероральных препаратов, содержащих аскорбиновую кислоту и двухвалентное железо, уже готовое для всасывания в кишке и не требующее присутствия соляной кислоты желудочного сока.
Коррекция диспептических жалоб (тошнота, тяжесть в эпигастрии, отрыжка) осуществляется прокинетическими препаратами (Ганатон®). Если пациента беспокоит изжога или боли в эпигастрии, назначение ИПП при АИГ считается нецелесообразным, поскольку в условиях ахлоргидрии применение ИПП может усугублять гиперплазию ECL-клеток. Купирование синдрома избыточного бактериального роста возможно курсовым применением кишечных антибиотиков. Применение ферментных препаратов при АИГ не показано.
Иммуносупрессивные препараты, стероидные гормоны и биологическая терапия не используются для лечения АИГ. Связано это с большим количеством побочных эффектов данных препаратов, а также с отсутствием достаточного количества данных клинических исследований.
Ключевой мерой в ведении пациентов с АИГ считается регулярное эндоскопическое наблюдение (1 раз в год), которое позволяет своевременно выявлять предраковые изменения и состояния в слизистой оболочке желудка, удалять полипы и опухоли. НЭО 1-го типа, часто выявляемые при АИГ, отличаются благоприятным прогнозом и при своевременном удалении не влияют на снижение продолжительности жизни.
Список литературы находится в редакции
Читайте также
- Новый международный консенсус RE.GA.IN.: диагностика и лечение гастрита в реальной клинической практике
- Хронический гастрит, ассоциированный с Helicobacter pylori
- Серологическая диагностика хронического гастрита
- А есть ли симптомы у гастрита?
- Эозинофильный гастроэнтерит: что нам о нем известно?
- Влияние препарата Регастим Гастро на слизистую оболочку желудка при хроническом атрофическом гастрите, ассоциированном с Helicobacter pylori


















