Статьи
Диабетическая энцефалопатия: как правильно поставить диагноз?
НЕ ТОЛЬКО НЕРВЫ
При СД поражаются не только периферические нервы, но и структуры центральной нервной системы (ЦНС). Остро или хронически развивающиеся изменения
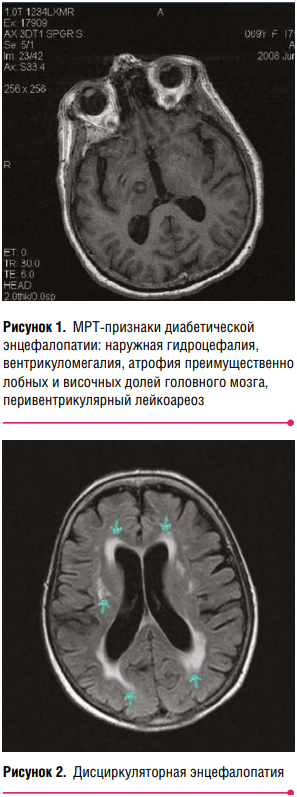
в ней вследствие как гипер-, так и гипогликемии с 1950 года по предложению R.N. de Jong называют диабетической энцефалопатией (ДЭ, рис. 1). Это одно из тяжелых микрососудистых осложнений СД, характеризующееся нарушением когнитивных функций (КФ), а также электрофизиологическими, нейрохимическими и структурными аномалиями. Под КФ, относящимися к высшим мозговым, понимают внимание, психомоторную координацию, речь, гнозис, праксис, счет, мышление, ориентацию, планирование и контроль высшей психической деятельности. Все это страдает при развитии ДЭ. Возникают также изменения психики и настроения, эмоциональная лабильность или депрессия. Частота развития ДЭ варьирует от 2,5 до 78 %, что обусловлено как неоднородными контингентами обследованных больных, так и особенностями методов диагностики данного синдрома. Выделение ДЭ при СД затруднительно, так как с течением времени заболевания прогрессируют церебральные сосудистые нарушения, вызванные развитием диабетической ангиопатии, артериальной гипертензии (АГ) и автономной нейропатии. Хроническая гипергликемия при СД приводит к формированию патологии микроциркуляторного русла, в частности атеросклероза сосудов, в том числе мозговых. АГ и атеросклеротические изменения внутримозговых сосудов ведут к ишемическому поражению головного мозга (ГМ) и дисциркуляторной энцефалопатии (рис. 2), тесно граничащей с ДЭ, но не позволяющей установить этот диагноз. То же самое касается и очаговых поражений ГМ, являющихся самостоятельной нозологической формой. Поэтому авторы публикаций о ДЭ очень осторожно проводят границу между энцефалопатией диабетической и дисциркуляторной.
МЕХАНИЗМЫ РАЗВИТИЯ
В основе развития ДЭ лежит в первую очередь непосредственное повреждение нейронов, вызванное увеличением содержания внутриклеточной глюкозы. Хронические метаболические и сосудистые изменения и апоптоз нейронов могут играть важную роль в их гибели и нарушении КФ. За апоптоз нейронов отвечают множество факторов, таких как инсулиноподобный фактор роста, гипергликемия и сам процесс старения. По мнению китайских исследователей, дефицит инсулина и С-пептида может играть ключевую роль в развитии ДЭ, а экзогенное введение С-пептида частично предотвращает апоптоз нейронов в гиппокампе диабетиков. Таким образом, применение С-пептида может рассматриваться как потенциально эффективная терапия ДЭ.
Другими механизмами, определяющими формирование ДЭ, являются активизация полиолового и гексозаминового путей метаболизма глюкозы, образование конечных продуктов избыточного гликирования белков, гиперпродукция супероксида в митохондриях. Главная причина развития полинейропатии, включая и ДЭ,—это оксидативный стресс. Низкая активность антиоксидантных ферментов определяется генетическими факторами, доказательством чего служит полиморфизм генов ферментов антиоксидантной системы, в частности супероксиддисмутазы.
Голландские исследователи показали, что периферическая и центральная нейропатия имеют разную этиологию. У 122 пациентов с СД 2 типа выполнили стандартизированное неврологическое и нейропсихологические обследование, а также МРТ головного мозга. Результаты нейропсихологических тестов оценивались в стандартизированных Z-значениях на пяти заданных когнитивных доменах, а повреждения коркового и белого вещества и атрофия подкорковых структур — по данным МРТ. Больные СД 2 типа имели более низкую производительность по результатам нейропсихологических тестов, больший объем поражения белого вещества и более выраженную атрофию мозга, чем в контрольной группе. В группе пациентов с СД ни один из показателей периферической нейропатии не ассоциировался с аномалиями на МРТ или когнитивной дисфункцией. Авторы пришли к выводу, что периферическая нейропатия у пациентов с СД не связана с когнитивной дисфункцией и ДЭ. Это значит, что центральные и периферические неврологические осложнения СД 2 типа имеют разный патогенез.
Каким же образом пытались выявить ускоренное снижение КФ у пациентов, например, с СД 2 типа? Известно, что он связан с повышенным риском развития как когнитивных нарушений, так и их крайнего проявления—деменции. Ученые из Нидерландов, сканируя мозговые структуры, попытались провести параллель между сосудистыми и метаболическими факторами риска и ускоренным развитием когнитивных нарушений у диабетиков. КФ и объем ГМ, а также метаболические и сосудистые факторы риска оценивались у 68 больных с интервалом 4 года. На 1,5-тесловом магнитно-резонансном томографе проводились измерения объема ГМ, боковых желудочков и белого вещества.
Индексы вычисляли на основе данных контрольной группы для оценки изменений КФ с поправкой на возраст, пол и расчетного коэффициента интеллекта. Объемы ГМ были сопоставлены у больных с ускоренным снижением КФ и без него. Ускоренное снижение КФ выявлено у 17 (25 %) пациентов с СД 2 типа и ассоциировалось с большим увеличением объема желудочка и белого вещества. У больных не отмечалось сосудистых или метаболических факторов риска, связанных с ускоренным снижением КФ. Этот процесс у пациентов с СД 2 типа напрямую ассоциировался с прогрессивными повреждениями церебральных сосудов и глобальной атрофией коры ГМ.
Все это приводит нас к выводу о том, что патогенез ДЭ сложен, а обоснование данного диагноза не всегда понятно. Неслучайно во всех фундаментальных руководствах, вышедших в РФ за последние 5 лет, ДЭ как осложнение СД и способы ее коррекции не рассматриваются. Помимо нарушения КФ, к тяжелым, жизнеугрожающим последствиям поражения мозговых сосудов при СД, безусловно, относится риск развития инсульта (рис. 3).
СОМНИТЕЛЬНОЕ ПРИЗНАНИЕ
ДЭ лишь недавно признана осложнением СД 1 типа, утверждают американские исследователи, подчеркивая очевидность отсутствия инсулина и С-пептида как негативных факторов, приводящих к дисрегуляции нейротрофических изменений. Дефицит инсулина оказывает негативное воздействие на синаптогенез, ведет к дегенерации нервных волокон и отклонениям поведенческих реакций. Этот каскад событий приводит к гибели нейронов и снижению плотности белого вещества миелинизирующих клеток. Все это выливается в еще более глубокий дефицит поведенческих и когнитивных функций.
Такие изменения, вероятно, лежат в основе атрофии серого и белого вещества у пациентов с СД 1 типа и в значительной степени нивелируются введением C-пептида. Терапия С-пептидом благотворно влияет на многочисленные патогенетические механизмы, предотвращая гибель нейронов и олигодендроглиальных клеток, а также существенно улучшая нейроповеденческие и когнитивные функции. Апоптоз нейронов гиппокампа сопровождался нарушениями КФ. Немаловажную роль в процессе апоптоза нейронов играют дефицит инсулина и гипергликемия, которые и обусловливают развитие первичной ДЭ.
ДЭ при СД 1 типа обычно развивается исподволь, у молодых ее проявления усугубляются последствиями перенесенных острых кетоацидотических и гипогликемических эпизодов. Как и при других метаболических энцефалопатиях, клинические проявления ДЭ неспецифичны. Повреждающее воздействие на мозговую ткань оказывают и другие индуцированные патологические изменения: нарушение реологических свойств крови с расстройством микроциркуляции, микротромбообразованием и гипоксией; компенсаторное перераспределение мозгового кровотока в пользу функционально более значимых срединных структур.
Данные французских исследователей говорят о том, что весомую роль в развитие ДЭ вносят гипогликемические состояния и их тяжесть. Диабет, безусловно, может быть причиной развития сосудистой деменции, особенно у детей и пожилых пациентов, чей мозг наиболее уязвим к гипогликемическим состояниям. Экспериментальные данные и патологоанатомические наблюдения подтверждают реальность гипогликемической энцефалопатии. Однако влияние легкой гипогликемии в настоящее время является предметом обсуждения, а вот воздействие на мозг тяжелой — не оспаривается.
Ученые из Детройта (США) полагают, что рост заболеваемости болезнью Альцгеймера у пациентов с СД 2 типа связан с резистентностью к инсулину, гиперинсулинемией и гипергликемией в сочетании с гиперхолестеринемией, гипертонией и ожирением. ДЭ у пациентов с СД 1 выражается в низкой способности к обучению, недостаточном развитии интеллекта и снижении памяти. Клинически ДЭ может проявляться плохим настроением, ухудшением умственной и физической работоспособности, утомлением, нарушением ритма сна. Синдром когнитивных расстройств проявляется снижением памяти и внимания, что затрудняет процесс обучения в школе или вузе. Пароксизмальные состояния иногда дают о себе знать психовегетативными приступами по типу панических атак. Основным механизмом ДЭ в данном случае выступает дефицит инсулина с последующим его воздействием на экспрессию нейротрофических факторов, нейромедиаторов, окислительный стресс и апоптоз нейронов в еще развивающемся мозге. Экспериментальные данные подчеркивают важную роль нарушений центрального действия инсулина. Таким образом, механизмы, приводящие к развитию ДЭ, являются сложными и отличаются у пациентов с разными типами СД.
Патогенез диабетической энцефалопатии сложен, ее трудно дифференцировать от других видов энцефалопатии, нет четких критериев диагностики, обоснование диагноза не всегда понятно. Неслучайно в фундаментальных руководствах, вышедших за последние 5 лет в РФ, ДЭ и способы ее коррекции не рассматриваются
АЛГОРИТМЫ ПОИСКА
Основными клиническими признаками ДЭ являются неврозоподобные состояния, нарушение КФ и органическая неврологическая симптоматика. Развитие неврозоподобных нарушений (депрессии) обусловлено действием как соматогенных факторов (гипогликемические реакции, поражение внутренних органов), так и психогенных (необходимость постоянного соблюдения диеты и медикаментозного лечения, вероятность тяжелых инвалидизирующих осложнений, эректильная дисфункция, бесплодие). При первичном осмотре депрессивная симптоматика выявляется у 35,4 % больных. При этом о наличии депрессивных нарушений за период болезни сообщают 64,6 % больных СД. К основным факторам, предрасполагающим к развитию психических расстройств при СД, относятся акцентуации личности, психогенная природа СД, неблагоприятная микросоциальная среда, неудовлетворительная компенсация СД, длительность болезни более 10 лет, наличие инвалидизирующих осложнений. По данным литературы, в чистом виде ДЭ встречается лишь у больных СД 1 типа (в 80,7 % случаев), поскольку ее развитие обусловлено преимущественно неэффективным метаболическим контролем. Смешанная энцефалопатия диагностируется у 82,7 % больных СД 2 типа в связи с преобладающим патогенетическим влиянием дисгемических факторов (гиперлипидемия и АГ).
Российские неврологи провели комплексное изучение особенностей когнитивной сферы, депрессивной симптоматики, клинико-анамнестических характеристик и метаболического статуса больных с ДЭ. У них было установлено относительное снижение параметров памяти и внимания. Коэффициент «невербального» интеллекта при ДЭ не отличался от значения в группе больных СД без ДЭ и соответствовал уровню «хорошей нормы». Развитие ДЭ было связано с нарастанием депрессивной неудовлетворенности, утомляемости, утраты либидо, а также с интенсификацией эмоционально окрашенных жалоб, касающихся физического самочувствия, и относительным увеличением индекса атерогенности и гликемии.
Авторы вывели уравнение дискриминирующей функции, позволяющее объективизировать диагноз ДЭ по клиническим и лабораторным данным. Были разработаны предикторы ДЭ и алгоритм выявления данной патологии: F = 0,031бa + 0,143бб + 1,724бв — 1,558бг + 0,179бд — 0,207бе—3,984, где а—возраст (годы), б— индекс массы тела (кг/м2 ), в — диеновые конъюгаты, г—холестерин липопротеидов низкой плотности (ммоль/л), д—уровень сахара в крови (ммоль/л) на 23:00, е — на 07:00. Величина F больше критического значения 0,0245 свидетельствует о наличии ДЭ. Но если для диагностики используется формула, а не клинические признаки, то вопрос легитимности диагноза вызывает сомнения.
Врачи из Ирана продемонстрировали, что когнитивные расстройства у пациентов с ДЭ могут привести к ухудшению производительности труда. Ученные полагают, что в основе ДЭ лежат морфологические изменения гиппокампа, поэтому необходимо заняться поиском нейропротекторной терапии, направленной на инволюцию данных проявлений.
УСПЕХИ В ЛЕЧЕНИИ
Понятно, что лечение ДЭ должно включать нормализацию метаболических процессов, терапию ангиопатии, гиперлипидемии, АГ и симптоматическую коррекцию. Китайские ученые попытались использовать для лечения ДЭ препарат паеонол, выделенный из коры корней растения Paeonia suffruticosa. В исследовании паенол в дозах 50 и 100 мг/кг снижал массу тела, уровень гликемии и гликозилированных белков. Иммуногистохимические анализы показали значительное уменьшение содержания конечных продуктов гликирования в гиппокампе и коре головного мозга нейронов после лечения. Кроме того, паеонол значительно увеличивал концентрацию глутатиона и одновременно позитивно влиял на уровень оксида азота в гиппокампе. Это значит, что паеонол может быть перспективным препаратом для профилактики и лечения ДЭ.
В одном из последних исследований авторы предположили, что в патогенезе развития ДЭ может играть роль качество пищевых жиров, поэтому для профилактики данного осложнения не исключена разработка рекомендаций по нутритивной поддержке. Для коррекции метаболических процессов и лечения макроангиопатии используют препараты альфа-липоевой кислоты, витамины группы В, актовегин. Российские врачи показали, что актовегин, уменьшая выраженность перекисного окисления липидов, улучшает микроциркуляцию, функцию структур ЦНС и приводит к значительному улучшению состояния больных СД. Не оказывая прямого вазодилатирующего воздействия, препарат улучшает утилизацию глюкозы и кислорода клеточными структурами, в том числе периферической и центральной нервной системы. Учитывая практическое отсутствие побочных эффектов, актовегин можно применять для лечения больных пожилого возраста с СД 2 типа и когнитивными нарушениями.
Сегодня нет четких критериев диагностики ДЭ, ее сложно дифференцировать от других видов энцефалопатии, а патогенетическое лечение находится пока на стадии разработки. У таких пациентов может применяться метаболическая и сосудистая терапия, но длительность ее проведения остается предметом дискуссий.