Статьи
Контроль кровотечений с рождения
 Представленные в декабре 2022 года на конференции Американского общества гематологов промежуточные данные III фазы исследования HAVEN 7 показывают, что эмицизумаб обеспечивает значимый контроль кровотечений у детей с рождения.
Представленные в декабре 2022 года на конференции Американского общества гематологов промежуточные данные III фазы исследования HAVEN 7 показывают, что эмицизумаб обеспечивает значимый контроль кровотечений у детей с рождения.
О ГЕМОФИЛИИ A
Гемофилия — серьезное наследственное заболевание, связанное с нарушением функции свертывания крови, что приводит к неконтролируемым и часто спонтанным кровотечениям. Гемофилией А болеют приблизительно 900 тыс. людей во всем мире, у 14 и 48 % из которых наблюдаются средней тяжести и легкая формы заболевания соответственно. Однако тяжесть гемофилии А не всегда выражается в кровоточивости, поскольку у некоторых больных со среднетяжелой формой гемофилии могут наблюдаться такие же симптомы, как и при тяжелой гемофилии и им требуется профилактика.
Гемофилия А любой степени тяжести может значительно снизить качество жизни больных, а также членов их семей и тех, кто осуществляет уход за пациентом. У больных гемофилией А отсутствует или имеется в недостаточном количестве белок, участвующий в процессе свертывания крови (фактор свертывания VIII, FVIII).
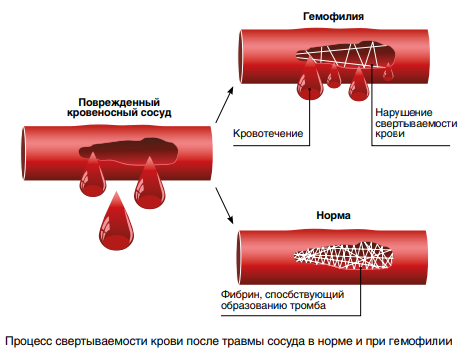
Когда кровотечение происходит у здорового человека, FVIII связывается с факторами свертывания крови IXa и X, что ведет к формированию сгустка крови и остановке кровотечения. В зависимости от тяжести заболевания, у пациентов с гемофилией А часто возникают кровотечения, в том числе кровоизлияния в суставы или мышцы, очень болезненные и приводящие к хроническому отеку, деформации, уменьшению подвижности суставов. Серьезным осложнением лечения является выработка ингибиторов к препаратам, замещающим FVIII. Ингибиторы представляют собой антитела, которые связываются с замещающим FVIII и блокируют его активность, что затрудняет или делает невозможным достижение уровня FVIII, достаточного для контроля кровотечения.
ОБНАДЕЖИВАЮЩИЕ РЕЗУЛЬТАТЫ
 Около года назад на 64-й Ежегодной конференции Американского общества гематологов (ASH) в Новом Орлеане, а затем и в Москве были представлены промежуточные результаты III фазы исследования HAVEN 7, проводившегося для дальнейшего подтверждения преимуществ профилактического лечения препаратом эмицизумаб младенцев с тяжелой формой гемофилии А без ингибиторов FVIII с рождения, ранее не получавших терапию или получавших минимальное лечение.
Около года назад на 64-й Ежегодной конференции Американского общества гематологов (ASH) в Новом Орлеане, а затем и в Москве были представлены промежуточные результаты III фазы исследования HAVEN 7, проводившегося для дальнейшего подтверждения преимуществ профилактического лечения препаратом эмицизумаб младенцев с тяжелой формой гемофилии А без ингибиторов FVIII с рождения, ранее не получавших терапию или получавших минимальное лечение.
Уход за такими детьми—непростая задача для родителей и медицинского персонала. В руководстве Всемирной федерации гемофилии стандартом лечения считается регулярная профилактика, начатая в раннем возрасте, поскольку исследования показали, что она улучшает долгосрочные результаты, снижая риск внутричерепного кровоизлияния. Однако многим детям с гемофилией А из-за высокой терапевтической нагрузки профилактику начинают только после первого года жизни. Эмицизумаб позволяет выбрать один из вариантов лечения: препарат применяется с рождения подкожно с разной частотой введения.
HAVEN 7—это многоцентровое открытое исследование III фазы, оценивающее эффективность, безопасность, фармакокинетику и фармакодинамику эмицизумаба у младенцев с тяжелой формой гемофилии А без ингибиторов к фактору VIII. Результаты промежуточного анализа, включающего данные 54 участников, показали, что у 77,8 % из них (n = 42) не было требующих лечения кровотечений, а у 42,6 % (n = 23) они вообще отсутствовали. Ни у одного из детей не зафиксировано спонтанных кровотечений, требующих терапии, а те, которые в ней нуждались, были травматическими. Всего задокументировано 77 кровотечений у 31 (57,4 %) участника, из них 88,3 % возникли из-за травм. Средняя годовая частота кровотечений на основе модели (95 % ДИ) на момент промежуточного анализа составляла 0,40 (0,23–0,65) для эпизодов, потребовавших лечения.
Профиль безопасности эмицизумаба соответствовал предыдущим исследованиям, новых сигналов в отношении безопасности не наблюдалось. Родители 9 (16,7 %) младенцев сообщили о нежелательных явлениях (НЯ), связанных с эмицизумабом, все это были локальные реакции в месте инъекции. У 8 (14,8 %) детей обнаружились 12 серьезных НЯ, не связанных с введением эмицизумаба. Случаев смерти, тромбоэмболических явлений или тромботической микроангиопатии не наблюдалось, что подтверждает благоприятный профиль безопасности эмицизумаба. Внутричерепных кровоизлияний также не было.
Первичный анализ намечен к проведению на 52-й неделе. У исследования есть дополнительный семилетний период последующего наблюдения для сбора долгосрочных данных о безопасности и исходах в отношении состояния суставов, что поможет показать преимущества эмицизумаба для этой популяции пациентов.
БАЗА ДАННЫХ EUHASS
Сведения из базы данных Европейской программы наблюдения за безопасностью пациентов с гемофилией (EUHASS) подтверждают, что профиль безопасности эмицизумаба для пациентов с гемофилией А является благоприятным и соответствует данным клинических исследований.
Результаты исследования ATHN 7, в котором изучается эффективность эмицизумаба у женщин с гемофилией А, показали, что у двух из трех участниц не было кровотечений; у третьей было одно требующее лечения кровотечение, связанное со стоматологическим вмешательством, и одно не требующее лечения, связанное с менструацией. Непрерывная оценка жизненно важна для дальнейшего понимания профиля безопасности и эффективности препарата эмицизумаб в этой редкой и недостаточно представленной популяции.
Эмицизумаб одобрен для лечения пациентов с гемофилией А с ингибиторами к фактору VIII в более чем 110 странах и без ингибиторов к фактору VIII—в более чем 100 странах, включая Россию.
О ПРЕПАРАТЕ ЭМИЦИЗУМАБ
Эмицизумаб — это биспецифическое антитело к факторам IXa и X. Он связывает факторы IXa и X, белки, участвующие в естественном каскаде коагуляции, и восстанавливает процесс свертывания крови у пациентов с гемофилией А.Эмицизумаб представляет собой профилактический препарат в форме готового раствора, который можно вводить подкожно раз в неделю, каждые две или четыре недели (после начальной дозы раз в неделю в течение первых четырех недель). В России эмицизумаб зарегистрирован с октября 2018 года (рег. уд. № ЛП-005110–151018). Препарат включен в клинические рекомендации Всемирной федерации гемофилии. Общее число пациентов, получивших эмицизумаб в клинических исследованиях и клинической практике во всем мире, к началу 2023 года превысило 24 тыс. человек.
Читайте также
- Викторианское наследие
- Лечение ингибиторной гемофилии А у пациента с неэффективной индукцией иммунной толерантности
- Терапевтическая опция для самых маленьких пациентов с гемофилией А
- Резолюция совета экспертов по вопросу определения критериев тяжелого фенотипа кровотечений у пациентов со среднетяжелой формой гемофилии А
- РЕЗОЛЮЦИЯ-2021 совета экспертов по вопросу применения препарата эмицизумаб у пациентов с гемофилией А

















