Статьи
Что может дать кардиологу внеклеточная ДНК?
Среди направлений медицинской науки последних лет важное место занимает адаптация для клинического применения различных биомаркеров, изменения которых характерны для тех или иных заболеваний. Одна из наиболее перспективных в этом отношении молекул — свободно циркулирующая, или внеклеточная ДНК (сцДНК)1 . В этом материале рассказывается о ее роли при сердечно-сосудистой патологии.
ЧТО ПРЕДСТАВЛЯЕТ СОБОЙ сцДНК
Наличие сцДНК в крови впервые установили французские ученые П. Мандель (P.Mandel) и П.Метэ (P.Métais) в 1948 г.—еще до открытия химической структуры нуклеиновых кислот. Это сильно фрагментированная двухцепочечная ДНК, присутствующая во внеклеточных средах: плазме/сыворотке, моче, слюне, ликворе, синовиальной и перитонеальной жидкостях. Такие фрагменты существуют в составе внеклеточных органелл (включая экзосомы), комплексов с другими веществами, а также в свободном виде. Понятие «внеклеточная ДНК» может также включать циркулирующую митохондриальную ДНК. Сходная с бактериальной молекулой, при нарушении аутофагии она может выступать провоспалительным фактором. Имеются данные о ее существенной роли в повреждении кардиомиоцитов.
Значительная часть сцДНК является результатом клеточной гибели. При апоптозе ядерная ДНК расщепляется ферментом ДНКазой, и в дальнейшем фрагменты нуклеиновой кислоты не подвергаются воздействию макрофагов. Некроз в норме вносит меньший вклад в количество сцДНК, увеличивая его при интенсивных продолжительных стрессах, тяжелых травмах. «Некротическая» сцДНК обнаруживается в виде более длинных—>10 тыс. пар нуклеотидов (т.п.н.)—участков в отличие от «апоптотической» (~150 п.н.). Дифференцировать их можно в полимеразной цепной реакции (ПЦР).
Существуют и другие пути высвобождения внеклеточной ДНК. Так, при нетозе нейтрофилы формируют внеклеточные нейтрофильные ловушки (англ. neutrophil extracellular trap, NET; отсюда название NETosis) —сетеподобные структуры, задача которых состоит в дезактивации экзогенных патогенов. Последующая гибель нейтрофилов сопровождается выбросом ДНК, гистонов, ферментов и других белков во внеклеточное пространство. Нетоз может иметь патологический характер, способствуя возникновению тромбоза, кардиоваскулярных и других (в т.ч. онкологических) заболеваний.
Частично сцДНК образуется в результате секреции нормальными и опухолевыми клетками. Еще в 1972 г. доказан факт активного выделения ДНК лимфоцитами во внеклеточную среду. Наконец, по мнению некоторых исследователей, вероятным источником сцДНК в крови может быть ДНК, ассоциированная с мембраной диплоидных лимфоцитов человека. Этот тип цитоплазматической ДНК, открытый в 1971 г., до сих пор изучен недостаточно. Предположительно, из таких молекул может формироваться некоторый объем сцДНК, отличающейся по своим свойствам от ядерной и митохондриальной (ТуаеваН.О., АбрамоваЗ.И., 2007).
Интенсивное высвобождение сцДНК посредством экзосом, нетоза или везикулярного транспорта связано с активацией иммунных клеток, повышением концентраций цито-, хемокинов и матриксных металлопротеиназ (ММП). В 2018 г. экспериментально установлено, что при ВИЧ-инфекции у нечеловекообразных приматов происходит гиперактивация нейтрофилов и механизмов нетоза. В результате развивается массивная гибель CD4+ и CD8+ Т-лимфоцитов, В-клеток и моноцитов, захваченных нейтрофильными сетями, и формируется сопутствующая сердечнососудистая патология.
В норме содержание внеклеточной ДНК возрастает при физических нагрузках и у пожилых лиц. На фоне заболеваний сердца и сосудов, включая артериальную гипертензию (АГ), ишемическую болезнь сердца (ИБС) (инфаркт миокарда (ИМ), острый коронарный синдром (ОКС)), хроническую сердечную недостаточность (ХСН), а также при инсульте и венозной тромбоэмболии (ВТЭ) сцДНК может высвобождаться из поврежденных тканей. До настоящего времени окончательно не ясно, в какой степени этот процесс является частью патогенеза, а в какой—служит индикатором выраженности болезни. Вероятнее всего, при каждой нозологической форме это соотношение различно.
Для сцДНК в целом характерно преобладание пар гуанин–цитозин (ГЦ), более устойчивых к разрушению нуклеазами по сравнению с аденин-тиминовыми участками. Наличие АГ, ИБС, сопровождающихся активацией клеточной гибели, ведет к увеличению содержания ГЦ-богатых маркерных последовательностей во внеклеточной ДНК в ≥10 раз. Детекция таких фрагментов и выделение подтипов сцДНК со специфическими характеристиками могут нести важную диагностическую информацию и иметь существенное прогностическое значение. 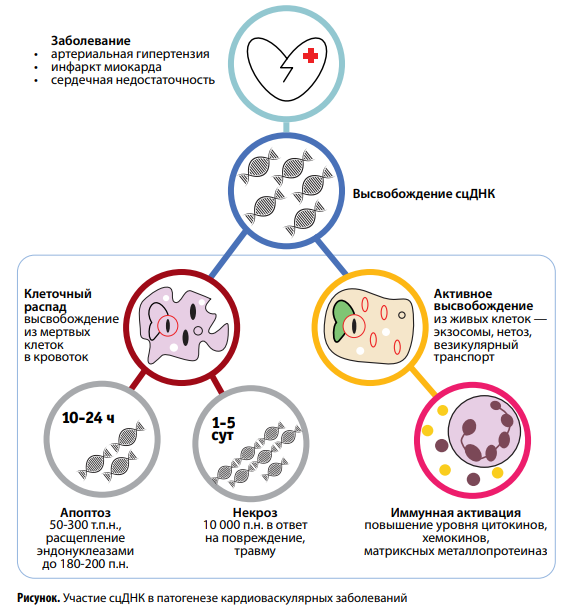
На рисунке суммированы важнейшие механизмы участия сцДНК в развитии болезней системы кровообращения.
сцДНК И АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
В ряде исследований подтверждено, что одной из независимых детерминант повышенного уровня внеклеточной ДНК выступает неоптимально контролируемая АГ. Избыток нуклеотидных фрагментов связан с множественными кардиометаболическими факторами риска. Это усиление системного неспецифического воспаления (высокие уровни С-реактивного белка (СРБ), провоспалительных цитокинов—интерлейкина (IL) 6 и фактора некроза опухоли альфа (TNF-α)), окислительный стресс, значительные концентрации холестерина липопротеинов низкой плотности и триглицеридов, а также более высокое систолическое артериальное (АД) и пульсовое давление. Повреждение геномной ДНК на фоне оксидативного стресса может способствовать увеличению общего пула сцДНК в кровотоке с последующей эндотелиальной дисфункцией (ЭД) и ростом АД.
Показано, что у пациентов с АГ, коморбидных по сахарному диабету, большие кон ́ - центрации сцДНК могут быть ассоциированы со снижением эластичности стенок артерий. У женщин в постменопаузе, не получающих заместительную гормональную терапию, избыточное содержание сцДНК также указывает на более высокие индекс артериальной жесткости, модуль упругости Юнга и меньшую податливость сонной артерии. Наряду с этим присутствуют проявления системного воспаления, нарушение метаболизма глюкозы и повышенное АД (JylhavaJ. и соавт., 2014).
В исследовании О.В. Мячиной и соавт. (2024) из 20 пациентов с АГ II стадии, 20 — III стадии и 20 условно здоровых (контрольная группа) у всех установлено наличие в плазме крови сцДНК и кислоторастворимых нуклеотидов. Среди больных с АГ II–III стадий содержание сцДНК оказалось достоверно (p <0,05) более высоким в сравнении с практически здоровыми. Эти и другие данные указывают на то, что повышенный уровень сцДНК может свидетельствовать о сохраняющейся ЭД. Таким образом, определение этого маркера может служить опцией мониторинга АГ на молекулярном уровне.
сцДНК И АТЕРОСКЛЕРОЗ
Японскими учеными (в частности, M. Ishida и соавт., 2022) продемонстрировано, что внеклеточная ДНК способствует персистированию воспалительных реакций в стенках артерий в результате опосредованного высвобождения IL-6 и TNF-α. Вследствие этого дополнительно активируется образование атеросклеротических бляшек. Кроме того, обнаружено, что увеличение содержания циркулирующих комплексов ДНК–миелопероксидаза специфично для активации нейтрофилов у страдающих тяжелым коронарным атеросклерозом (BorissoffJ.I. и соавт., 2013). Поэтому сцДНК может быть не только диагностическим маркером, но и потенциальной терапевтической целью. Одним из возможных направлений лечения может стать блокирование рецепторов, активируемых сцДНК, с последующим снижением выраженности воспаления и замедлением развития и/или прогрессирования атеросклероза.
сцДНК И ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА
Содержание сцДНК с учетом времени высвобождения значительно возрастает при ИМ в первые 2 ч после появления загрудинных болей, а у перенесших его может регистрироваться выраженный (вплоть до 50-кратного) рост концентрации внеклеточной ДНК по сравнению со здоровыми. При этом кардиотропонин обнаруживается в плазме уже через 6 ч после ИМ, а повышенный уровень этого маркера может сохраняться до 14 ч. В то же время сравнение количества тропонина и кардиоспецифической сцДНК в 57 образцах миокарда пациентов с ИМ показало сильную связь между обоими параметрами (p <0,0001). Большинство (79 %) исследованных фрагментов тканей были положительными как на тропонин, так и на кардиоспецифическую сцДНК, 7 % — отрицательными в обоих случаях; в 11 % образцов наблюдалась изолированная положительная реакция на тропонин, а в 4 %—слабоположительная реакция только на сцДНК (ZemmourH. и соавт., 2018).
У больных с ИМ показатели внеклеточной ДНК в различной степени коррелируют со значениями других биомаркеров некроза: МВ-изофермента креатинфосфокиназы (МВ-КФК), СРБ, а также с изменениями фракции выброса (ФВ). Это явление может указывать на зависимость объема высвобождаемой сцДНК от тяжести миокардиального повреждения. Тот факт, что содержание кардиоспецифической сцДНК оказывается повышенным при ИМ с нормальным (<200 мкг/л) уровнем МВ-КФК, свидетельствует о большей чувствительности рассматриваемого теста. Вероятно, внеклеточная ДНК может быть более отчетливым и информативным параметром, чем некоторые из используемых в настоящее время. При этом быстрые изменения ее концентрации (в соответствии с периодом полувыведения 4–30 мин) являются в данном случае важным для ургентной медицины преимуществом, позволяя оценивать непосредственную эффективность того или иного вмешательства в минимальном временном промежутке. ́
сцДНК И ХРОНИЧЕСКАЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ
В случае наличия ХСН, также сопровождающейся апоптозом и некрозом кардиомиоцитов, характер изменений сцДНК во многом зависит от характера основного заболевания. В настоящее время изучаются главным образом молекулярные нарушения при сердечной недостаточности на фоне ИБС (ИМ, коронарный атеросклероз). Традиционно в качестве основного лабораторного показателя ХСН рассматривается концентрация мозгового натрийуретического пептида NT-proBNP. Однако этот параметр не обладает абсолютной специфичностью и может меняться при различных состояниях: заболеваниях почек, ожирении, на фоне химиотерапии, а также с возрастом. Одновременное же использование нескольких маркеров повышает диагностическую точность исследования. T.Yokokawa и соавт. (2020) анализировали у пациентов с ХСН уровни общей сцДНК и ее кардиоспецифической фракции, содержание которой было значительно повышенным в группе больных в сравнении со здоровыми добровольцами; при этом данный показатель коррелировал с уровнем тропонина, но не NT-proBNP.
Величина ФВ также служит критерием тяжести ХСН, однако корреляция между сцДНК и NT-proBNP у лиц со сниженной ФВ демонстрирует необходимость учета сократительной способности миокарда для более точной оценки взаимосвязи лабораторных и инструментальных показателей. В проспективном наблюдательном исследовании, проведенном Е.В.Колесниковой и соавт. (2023), приняли участие 67 больных (41 мужчина, 26 женщин) с ХСН; 23 человека без диагностированных хронических заболеваний составили контрольную группу. Во всех случаях определяли характер липидного профиля, значения глюкозы и креатинина сыворотки, NT-proBNP и внеклеточной ДНК. Установлены статистически значимые различия в концентрации сцДНК в крови при разной ФВ (<40, 40–49 и >50 %). Выявлена обратная зависимость между показателями сцДНК и ФВ, с одной стороны, и уровнями NTproBNP и ФВ—с другой. Кроме того, доказано положительное влияние медикаментозного лечения на содержание сцДНК и NT-proBNP в группе с ФВ <40 %. Таким образом, прогрессирующее снижение сократительной способности сердечной мышцы сопровождалось сочетанным повышением исследуемых маркеров, что отражало тяжесть состояния больного.
сцДНК И КАРДИОТРАНСПЛАНТАЦИЯ
Изучение внеклеточной ДНК у реципиентов сердца направлено на мониторинг состояния трансплантата и раннее выявление реакций отторжения. При этом речь идет о донорспецифической сцДНК. Так, по данным О.Е. Гичкун и соавт. (2023), у 5 исследуемых с морфологическими признаками отторжения (острого клеточного, гуморального и хронического) доля донорспецифической сцДНК в плазме составила от 0,01 до 5,0 %. К более отдаленной перспективе относится ранняя диагностика посттрансплантационных осложнений инфекционного характера — инвазивных микозов, эндокардитов и др.
сцДНК И ВЕНОЗНАЯ ТРОМБОЭМБОЛИЯ
Содержание сцДНК коррелирует с параметрами коагуляции и потребления тромбоцитов, а также с маркерами клеточного повреждения и размерами ишемических поражений, что подтверждает возможное значение внеклеточной ДНК как суррогатного маркера тромбообразования. Кроме того, это позволяет предположить, что сцДНК при ВТЭ происходит не из нейтрофильных ловушек, а высвобождается из поврежденных органов (M.Jiménez-Alcázar и соавт., 2017).
В исследование Y. Zhang и соавт. (2022) вошли 107 пациентов с ВТЭ, проходивших лечение в больнице г. Шицзячжуан (КНР) с мая 2019 г. по май 2021 г. Контрольную группу составили 110 условно здоровых. Сравнивали показатели плазменной сцДНК между группами и у больных с разной степенью тяжести болезни. Уровни внеклеточной ДНК в группе заболевания были более высокими, чем в контрольной (p <0,05). Содержание сцДНК в группах умеренного и тяжелого течения превышало таковое среди участников с легким течением болезни, а концентрация внеклеточной ДНК при тяжелом течении ВТЭ была выше, чем при умеренном (p <0,05 для всех случаев). Наконец, уровень сцДНК положительно коррелировал с тяжестью ВТЭ (p <0,05). По мнению авторов, полученные данные могут служить основой для оценки тяжести течения заболевания.
сцДНК И СОСУДИСТЫЕ ПОРАЖЕНИЯ ГОЛОВНОГО МОЗГА
Установлено, что при ишемическом инсульте (ИИ) продолжающаяся гибель клеток в зоне ишемии ведет к выбросу ими молекул и фрагментов ДНК в интерстициальное пространство. Концентрация внеклеточной ДНК у таких больных достоверно (p <0,001) повышается непосредственно в день сосудистого события. Изменения уровня сцДНК позволяют статистически значимо (p <0,001) дифференцировать ИИ с инсультоподобными состояниями (судороги, осложненная мигрень и др.), при которых имеется патологическая неврологическая симптоматика (O’Connell G.C. и соавт., 2017). В экспериментах показана связь между количеством внеклеточной ДНК и объемом повреждения мозга, имеющая достоверный характер (p <0,0001) (VajpeyeeA. и соавт., 2018). Важно также, что накопление в крови сцДНК при некрозе клеток способно ухудшать состояние гемореологии и течение процессов тромболизиса.
Долгосрочные (≥3 мес) неврологические исходы коррелируют с концентрацией сцДНК после реканализации окклюзированной артерии. Нужно учитывать, что возобновление кровотока нередко приводит к реперфузионному синдрому с дополнительным повреждением ткани мозга и структур гематоэнцефалического барьера, а это, в свою очередь, может потенцировать рост содержания сцДНК в плазме.
сцДНК И ДРУГИЕ БОЛЕЗНИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
Предстоит изучить значение определения сцДНК при миокардитах и перикардитах различной этиологии, миокардиодистрофиях, пороках сердца и др., равно как и после кардиохирургических операций (в т.ч. в педиатрической практике). Достижения в этой области до настоящего времени не столь значительны и связаны преимущественно с экспериментальными исследованиями.
ПРОБЛЕМЫ ОПРЕДЕЛЕНИЯ
На сегодняшний день используется ряд методик выделения и количественной оценки внеклеточной ДНК: спектрофотометрическое/флуориметрическое определение ее концентрации, количественная ПЦР, выделение из плазмы с помощью колонок или органических растворителей. С целью повышения диагностической эффективности разработаны технологии капельной цифровой ПЦР и секвенирования нового поколения.
Тем не менее количественное определение сцДНК в клинической медицине пока используется весьма ограниченно. Имеющиеся результаты свидетельствуют о том, что внеклеточная ДНК в значительной степени сохраняет статус кандидатного биомаркера. Этому во многом способствуют разноречивые данные об условно нормальном количестве плазменной сцДНК. Приводятся значения, характеризующие содержание сцДНК по отношению к условной норме, варьирующие от нескольких нг/мл до ~1200 нг/мл. На вариабельность концентрации сцДНК влияют особенности забора биоматериала, значительная вариативность образцов на этапах экстракции и очистки, условия хранения и др. (Herman D.S. и соавт., 2017). В дополнение к этому, как уже указывалось, содержание сцДНК у здорового человека может увеличиваться в несколько раз в зависимости от физической/эмоциональной нагрузки, возвращаясь через некоторое время (~60 мин) к исходной величине. Поэтому разработка и внедрение стандартов анализа внеклеточной ДНК требуют пристального внимания исследователей. Помимо этого, непосредственный анализ сцДНК сопряжен с достаточно высокой стоимостью процедуры, и эту проблему также предстоит решать в ближайшем будущем.
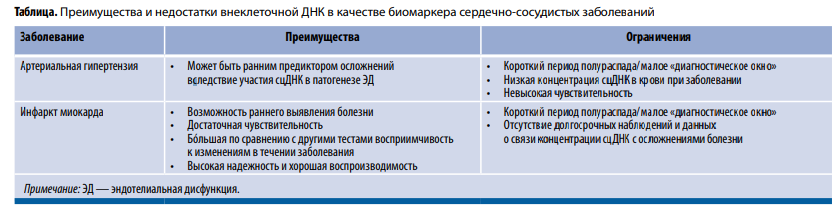
Существенным шагом может стать разработка мультимаркерной диагностической панели (в первую очередь для ИМ и ХСН), включающей наряду с определением МВ-КФК и кардиотропонина показатели сцДНК. Такой тест дополняет клиническую информацию данными о воспалительном статусе пациента. Применение подобной панели позволит также рационально использовать различия в темпах высвобождения и клиренсах этих биомолекул. При этом необходимо учитывать имеющиеся преимущества и ограничения каждой методики (таблица).
В ЗАКЛЮЧЕНИЕ
Изучение связи внеклеточной ДНК и течения сердечно-сосудистых заболеваний важно во многих отношениях, включая развитие персонализированной медицины и реализацию пациентоориентированного подхода. Дальнейшая исследовательская работа и клинические испытания должны содействовать повышению роли сцДНК как полноценного биологического маркера с соответствующей диагностической и прогностической значимостью.
Юрий Никулин, к.м.н
Список литературы находится в редакции
Читайте также
- Идиопатический рецидивирующий перикардит: распознавание, лечение, мониторинг
- «Осложнение на сердце»: миокардит и его негативные последствия
- Модификация факторов риска и профилактика развития тромбоэмболических событий при фибрилляции предсердий
- «Синдром разбитого сердца»: диагноз установлен — что дальше?
- В повседневную практику - Клиническая задача СК №4-24

















