Статьи
Персонализированный подход к некомплаентному пациенту
Сахарный диабет (СД) — хроническое заболевание, которое, помимо подбора рациональной и эффективной сахароснижающей терапии, требует изменения образа жизни пациента. Для успешного лечения необходимо соблюдение большого перечня рекомендаций врача, связанных как с планомерным приемом препаратов, так и коррекцией питания, восполнением физических нагрузок и сохранением позитивного настроя.
Множество факторов ведут к развитию постоянных гипергликемий, влияя на приверженность пациентов лечению. Проблема комплаентности — одна из самых сложных и труднорешаемых вследствие ее многофункциональности. Представленный клинический случай посвящен развитию стойкой гипергликемии у некомплаентного пациента с СД 1 типа на помповой инсулинотерапии.
В декабре 2022 года в отделение эндокринологии ГБУЗ «ГКБ имени С.П. Боткина ДЗМ» поступил пациент 22 лет с установленным в 14 лет (в 2014 году) диагнозом «СД 1 типа». С 2016 года он предпринимал неоднократные попытки установить инсулиновую помпу, однако каждый раз возвращался к использованию шприц-ручек из-за дискомфорта и декомпенсации углеводного обмена. Последняя попытка установить инсулиновую помпу в условиях стационара предпринята в апреле 2022 года. Со слов пациента, подбор индивидуальных настроек и обучение правилам пользования помпой не проводились.
За последние 3 года гликированный гемоглобин (HbA1c) измеряли 4 раза вместо рекомендованных 12. Компенсация углеводного обмена за все это время не достигнута. Неоднократно экстренно госпитализировался в больницы с диабетическим кетоацидозом.
При поступлении предъявлял жалобы на гипергликемию (до 27 ммоль/л), сухость во рту и жажду, судороги в икроножных мышцах, частые головные боли, периодическую тошноту, апатию, повышенную сонливость. Из анамнеза известно о депрессивном эпизоде средней степени тяжести. На момент госпитализации принимал препарат пароксетин (10 мг). По заключению психиатра (сентябрь 2022 года), достигнута медикаментозная редукция. Страдает хроническим панкреатитом.
При физикальном осмотре в местах установки инфузионных систем (в области плеч и в нижних квадрантах живота) определялись выраженные липодистрофические изменения подкожно-жировой клетчатки. Базальный профиль инсулиновой помпы — по 1 Ед/ч в течение всего дня. Помощником болюса пациент пользоваться не умел, в связи с чем последний был отключен. Самостоятельно осуществлял введение инсулина на все приемы пищи с использованием углеводного коэффициента (1 ХЕ: 1,5 ЕД). Измерение гликемии не всегда предшествовало инъекциям. Самоконтроль гликемии в домашних условиях нерегулярный, смену инфузионных наборов осуществляет раз в 3–4 дня. Подсчету углеводов по системе хлебных единиц (ХЕ) обучен не в полном объеме. Гипогликемические состояния с нейрогликопенической симптоматикой отмечает до двух раз в месяц при гликемии менее 3,5 ммоль/л. При обследовании в биохимическом анализе крови обнаружены дислипидемия — липопротеины низкой плотности (ЛПНП)—2,99 ммоль/л и гиперурикемия (мочевая кислота — 392 мкмоль/л), а также гипопротеинемия (общий белок — 65 г/л), которая может указывать на внешнесекреторную недостаточность поджелудочной железы. Также диагностированы диабетическая нефропатия, хроническая болезнь почек (ХБП) С1 А2, HbA1c — 12 %.
В копрограмме — умеренное количество остатков непереваренной пищи, мышечных волокон с исчерченностью и без, немного нейтрального жира, солей жирных кислот и перевариваемой растительной клетчатки. Пациенту с внешнесекреторной недостаточностью поджелудочной железы был рекомендован курс терапии полиферментными препаратами по 40000 МЕ перед приемами пищи, стандартизированный по липазе.
На 3-й день госпитализации возникла стойкая гипергликемия до 18 ммоль/л с жалобами на боли в эпигастральной области, диарею, тошноту и рвоту, повышение температуры тела до 38 ºС. По лабораторным данным, причиной неконтролируемой гипергликемии стало инфекционное заболевание.
В январе 2023 года повторно поступил в стационар для коррекции настроек инсулиновой помпы с гликемией 21 ммоль/л, а дома она доходила до 29 ммоль/л. Диагностирован диабетический кетоацидоз легкой степени (рН — 7,288, лактат — 4,1 ммоль/л, кетоновые тела в моче — 0,5 ммоль/л). В течение 2 дней проводилась инфузионная терапия, на фоне которой отмечалось снижение гликемии. Общая суточная доза инсулина на момент поступления составляла 65 ЕД. На третий день стойкая гипергликемия сохранялась. Из-за, предположительно, сниженной индивидуальной чувствительности к имеющемуся в резервуаре инсулину аспарт последний заменили на глулизин (без эффекта). Были скорректированы настройки базального профиля, однако в дальнейшем состояние ухудшилось. Гликемия колебалась от 14 до 25 ммоль/л в течение дня без особого эффекта после различных видов инсулинотерапии. Воспалительный генез гипергликемии был исключен. Инфузионный набор заменили, установив канюлю на боковую поверхность живота, без заметного эффекта. При осмотре выраженных липодистрофических изменений на боковых поверхностях живота не обнаружено, что может свидетельствовать о вероятных диффузных изменениях. За день общая суточная доза инсулина у пациента с массой тела 74 кг составила 100 ЕД. На фоне увеличения всех временных промежутков базального профиля и углеводных коэффициентов отмечалась тенденция к стабилизации показателей гликемии и стали возможны безуглеводные приемы пищи. Однако, несмотря на кажущийся успех, к концу третьего дня после замены инфузионного набора гликемия вновь поднялась до 20 ммоль/л. Инфузионный набор заменили повторно с установкой канюли на ягодицу, куда пациент ранее канюли не устанавливал и даже не знал о такой возможности. Произошло снижение гликемии. Было рекомендовано избегать установки инфузионного набора в область живота до нормализации состояния кожи и подкожно-жировой клетчатки в местах инъекций инсулина (не менее 6 месяцев). В течение следующего дня гликемия колебалась в пределах целевых значений. Финальная общая суточная доза инсулина составила 70 ЕД, что несильно отличается от суточной дозы при поступлении. Последующие колебания гликемии были связаны с неправильным самостоятельным подсчетом углеводов, отсутствием паузы между введением инсулина и приемом пищи, отсутствием белков, жиров и клетчатки в еде.
В связи с жалобами на выраженную дневную сонливость пациент осмотрен неврологом. Диагностированы энцефалопатия сложного генеза, астено-депрессивный синдром, инсомния. Рекомендована консультация сомнолога. Также проконсультирован медицинским психологом по результатам личностного опросника. В аффективноличностной сфере — высокий уровень тревожности, депрессивные тенденции, склонность к дистанцированности и отчужденности, что может приводить к нарушениям адаптации и декомпенсации. Данные изменения также можно считать одним из факторов стойкой гипергликемии, ведь подобное состояние, помимо прочего, выливалось в отсутствие желания и мотивации лечиться и учиться. Рекомендованы амбулаторная консультация психиатра и психологическая коррекционная работа. У нашего пациента опускались руки, и он неоднократно самостоятельно прерывал помповую инсулинотерапию в связи с тем, что не был в должной степени обучен тому, как надо пользоваться помпой. Основная причина постоянных гипергликемий заключалась не столько в неправильной настройке помпы, сколько в нарушении правил ее использования и неосведомленности о возможных ошибках помповой инсулинотерапии, а также в невладении навыком подсчета углеводов, коррекции терапии при интеркуррентных заболеваниях и отсутствии должного лечения сопутствующих патологий (астено-депрессивный синдром и внешнесекреторная недостаточность поджелудочной железы).
КОНЦЕПЦИЯ 5П-МЕДИЦИНЫ
На историю данного пациента стоит взглянуть через призму базовой концепции развития современного мирового и российского здравоохранения — концепцию 5П-медицины. Она основана на индивидуальном подходе к человеку с фокусом на предсказании и профилактике заболеваний и персонализированном принципе их лечения с ответственным и позитивным участием самого пациента.
В 2008 году Лерой Эдвард Худ предложил концепцию «4П-медицины» с такими характеристиками:
- предиктивная (предсказательная, прогностическая);
- предупредительная (превентивная, профилактическая, упреждающая);
- партисипативная (предусматривающая активное участие самого пациента);
- персонализированная (индивидуальное и специфичное лечение).
Спустя 7 лет к ним добавилась пятая «П» — позитивная медицина, что предполагает контроль ментального состояния для поддержания здоровья. В 2018 году вышел приказ Минздрава России «Об утверждении Концепции предиктивной, превентивной и персонализированной медицины» как базовой для развития здравоохранения и в нашей стране.
Предиктивная медицина предполагает обследование здорового населения и скрининг тех заболеваний, которые в конкретной стране становятся основной причиной инвалидности и преждевременной смерти. Врач и пациент не ждут начала болезни, а с помощью генетического типирования и других анализов проактивно ищут слабые места в организме, чтобы заранее спрогнозировать риск заболеваний. Например, программа расширенного неонатального скрининга в России с 2023 года включает обязательное обследование всех новорожденных на 36 заболеваний.
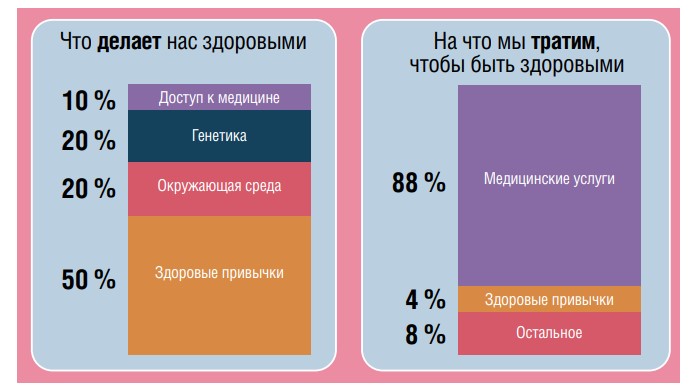
Профилактическая медицина основана на предотвращении заболеваний и устранении рисков их развития, в частности, путем снижения веса при наличии предрасположенности к СД 2 типа. Ценность предсказательной и превентивной медицины становится особенно понятной при рассмотрении структуры факторов, влияющих на здоровье (рис.). На 50 % — это наши привычки, на 20 % — влияние факторов окружающей среды, еще 20 % — генетическая детерминированность. Таким образом, 90 % факторов реализуются, по сути, еще до того, как человек заболевает. Вместе с тем наш фокус внимания и затраты почти на 90 % направлены на медицинские услуги, а не на поддержание здоровья.
При развитии заболевания важно применять персонализированный подход в подборе схем терапии с учетом индивидуального профиля больного, в том числе данных дистанционного мониторинга. Также к персонализированной медицине можно отнести такое новейшее направление, как медицина прецизионная, или точная терапия, основанная на подборе или создании лечения на основании биомаркеров конкретного человека.
Принцип партисипативной медицины основан на тесном сотрудничестве врача и пациента в разработке и выполнении плана лечения. Важно, чтобы больной брал на себя ответственность за свое лечение и становился активным участником процесса терапии. Для этого он должен знать достаточно о своем заболевании и обладать необходимыми навыками и мотивацией, чтобы с ним справляться. В контексте партисипативной медицины создаются терапевтические школы для хронических больных и ими самими ведется активный мониторинг состояния собственного здоровья, включающий, например, измерение артериального давления (АД) и гликемии.
Позитивная медицина. Критическую роль в успехе лечения заболеваний, особенно хронических, играет настрой пациента на улучшение состояния здоровья. С одной стороны, важно поддерживать хороший уровень ментального здоровья, чтобы сохранять адекватность восприятия своего состояния. С другой — иметь позитивный настрой и ресурсность для планомерного и дисциплинированного следования медицинским рекомендациям и преодоления болезни. Необходимо проведение практик благополучия (физического, ментального, эмоционального и духовного здоровья) и подключение психологов к ведению пациентов.
Концепция 5П-медицины также приобретает особую роль при анализе приверженности пациентов лечению. Влияющие на нее факторы Всемирная организация здравоохранения (ВОЗ) объединила в 5 основных групп.
1. Факторы, связанные с пациентом, например пол и возраст. Женщины аккуратнее соблюдают рекомендации, как и взрослые в целом. При этом дети и пожилые нуждаются в поддержке и сопровождении. Люди с достаточным уровнем образования часто оказываются более мотивированными.
2. Факторы, связанные с врачом и системой здравоохранения. Личность, психотип, мотивация и ресурсность врача, его умение убеждать и четкое следование клиническим рекомендациям заметно влияют на комплаентность пациента.
3. Зависит она и от факторов, связанных с заболеваниями. Важно, чем конкретно и в какой форме (острой или хронической) страдает пациент, насколько адекватно оценивает самочувствие, получает ли достаточно информации, чтобы следовать рекомендациям, и хочет ли сам справляться с лечением.
4. Имеют значение и факторы, связанные с проводимой с терапией (переносимость препаратов и нежелательные явле ния — НЯ).
5. Социально-экономический контекст, в котором существует эта система, складывается из достаточного финансирования, доступности медицинской помощи, покрытия государством расходов пациента на лекарства, возможности получать препараты в системе льготного обеспечения.
ПАЦИЕНТ В ЦЕНТРЕ
Современный взгляд на повышение качества оказания медицинской помощи базируется на пациентоцентричности. Это означает, что в фокусе внимания находятся здоровье, потребности и ожидания пациента. Мы не изучаем набор из множества общих факторов, а смотрим на них глазами конкретного пациента. Соединяя этот подход с проблемой комплаентности, приверженность лечению может складываться из ответов на четыре вопроса. Первое: знает ли пациент достаточно о своем заболевании и лечении? Второе и третье: умеет и хочет ли проводить необходимые манипуляции? Четвертое: есть ли у него для этого все необходимые возможности? Идеальная ситуация, когда пациент на эти вопросы может ответить: «Я знаю. Я умею. Я хочу. Я могу». Наш больной ответил бы иначе: «Я не все знаю про болезнь, и меня это не интересует. Я не все умею делать и не хочу учиться. Я воспринимаю свое некомпенсированное состояние как норму. У меня все есть, но мне это неважно». Ключевой способ изменения такой картины— работа с мотивацией и психологическим состоянием.
Представленный клинический случай напоминает о таких простых и на первый взгляд очевидных аспектах, как своевременная замена инфузионной системы и смена мест установки канюли, профилактика липодистрофических изменений, контроль сопутствующих заболеваний, поддержание ментального здоровья и многое другое. Суммируя эти рекомендации, мы и говорим о важности персонализированного подхода к лечению пациента с низкой степенью комплаентности. Прежде чем приступать к коррекции инсулинотерапии, необходимо удостовериться в правильности выполнения инъекций и подсчета углеводов, осведомиться о соматическом и психологическом состоянии пациента, сопутствующих заболеваниях. Помочь ему перейти в позицию «Я хочу. Я знаю. Я умею. Я могу» и стать ответственным участником лечебного процесса.
Обобщая рекомендации по повышению приверженности терапии среди пациентов, можно сфокусироваться на следующих подходах.
1. Врачу нужно максимально информировать пациента о проводимой терапии.
2. Во время консультации нужно найти факторы, которые могут снизить приверженность пациентов терапии.
3. Необходимо обратить внимание на образ жизни пациента, в частности на его трудовой график: сможет ли он принимать лекарства на работе? Путешествует ли он?
4. Следует обсудить с пациентами возможные НЯ назначенных препаратов.
5. Положительную роль способно сыграть вовлечение пациентов в процесс лечения и контроля его эффективности и безопасности, например самоконтроль АД и уровня гликемии.
6. Необходимы поощрение и поддержка со стороны семьи и друзей.
Таким образом, применение концепции 5П-медицины поможет в ведении сложных и недисциплинированных больных
Читайте также
- Город-миллионник внутри столицы
- Метаболическая память при сахарном диабете 2 типа
- Тиреотоксикоз и гипогонадизм: уже возможен надежный контроль
- Гипергликемия ургентных состояний у пациентов без сахарного диабета
- Современные возможности комплексной кардиоренальной защиты
- Алоглиптин и пиоглитазон — плодотворный союз в борьбе с сахарным диабетом 2 типа

















