Статьи
Нарушения углеводного обмена у пациентов на гемодиализе
Роли нарушений углеводного обмена в развитии терминальной хронической почечной недо‑ статочности (тХПН) посвящено немало исследований, но остается малоизученным вопрос о влиянии хронической болезни почек (ХБП) на показатели гликемии, в частности у больных на заместительной почечной терапии (ЗПТ).
Современные оригинальные исследования показывают, что не только СД, но и предиабетические состояния (нарушения гликемии натощак и толерантности к глюкозе) у больных без диабета на гемодиализе служат предрасполагающими факторами к развитию сердечно-сосудистых катастроф, ухудшающих качество жизни и повышающих смертность. Гипогликемия также становится не менее значимым фактором, угрожающим таким пациентам. Важно, во-первых, научиться вовремя распознавать подобные нарушения, а во-вторых, разработать алгоритмы их купирования. Для этого необходимо изучить особенности метаболизма глюкозы у пациентов на ЗПТ.
Ежегодно обновляющиеся цифры международных регистров ХБП свидетельствуют о неуклонном росте числа пациентов с тХПН на ЗПТ. При этом СД (в большей степени 2-го типа) продолжает занимать одну из лидирующих позиций в этиологии ХПН. Так, в ежегодном (конец 2019 года) отчете Европейской почечной ассоциации—Европейской ассоциации диализа и трансплантации (ERA-EDTA), включающем данные национальных и региональных регистров 34 стран, в среднем у 21 % европейских пациентов с ХБП, получающих лечение диализными методами, именно СД был причиной развития ХПН. При этом в США распространенность диабета среди больных ХБП 4–5-й стадий составляла около 48 %. С другой стороны, у 61 % американцев, приступивших к ЗПТ в 2019 году, именно СД стал причиной развития ХБП.
В России доля больных СД на ЗПТ значительно ниже, чем в США, однако она приближается к европейскому показателю. По данным Регистра российского диализного общества, в 2019 году 10 752 (18 %) из 59 153 пациентов, получавших ЗПТ, страдали диабетом. Как в Европе (58 %), так и в России (78 %) гемодиализ занимает лидирующие позиции в ЗПТ. Второе место в нашей стране, как и в Евросоюзе, принадлежит трансплантации почки (17 % у нас, 37 % у них), а на перитонеальный диализ в России приходится лишь 5 %. Таким образом, интерес к изучению углеводного статуса пациентов с ХБП без СД на гемодиализе возрастает параллельно с ежегодным увеличением числа таких больных. В немногочисленных исследованиях зарубежных авторов, посвященных расстройствам углеводного обмена у пациентов без СД в анамнезе, отмечается, что даже нарушения гликемии натощак или толерантности к глюкозе повышают риск смертности в краткосрочной перспективе.
ВАРИАБЕЛЬНОСТЬ ГЛИКЕМИИ
Как известно, в поддержании метаболизма глюкозы наравне с печенью ключевую роль играют почки. В их проксимальных канальцах осуществляется не только реабсорбция молекул глюкозы через натрий-глюкозные котранспортеры, но и ее образование из неуглеводных соединений. Почки также поддерживают гомеостаз глюкозы благодаря регуляции метаболизма молекул инсулина, инактивируя до 40 % из них с помощью клубочковой фильтрации или диффузии молекул из просвета перитубулярных капилляров в эпителиальные клетки. Затем инсулин разрушается под действием соответствующей протеазы и других лизосомальных ферментов. У пациентов с почечной недостаточностью снижается клиренс эндогенного инсулина, что повышает риск развития гипогликемии вследствие уменьшения потребности в инсулине из-за увеличения периода его полураспада. Снижение почечного глюконеогенеза из-за ухудшения функции почек рассматривается как дополнительный фактор риска (ФР) гипогликемии у пациентов с ХБП без СД. В исследовании при участии 243 222 пациентов с ХБП гипогликемию зафиксировали как у больных с СД, так и без него (10,72/100 и 3,4/100 пациенто-месяцев соответственно). У пациентов без СД на диализе также выявлены мощные ФР развития гипергликемии. Доказано, что инсулинорезистентность (ИР)—неотъемлемый компонент и один из ключевых ФР гипергликемии у больных с ХБП. Снижение чувствительности к инсулину и компенсаторное повышение уровня инсулина у пациентов с ХБП также могут привести к манифестации СД.
H. Xu с соавт. перечислили в обзорной статье основные причины, приводящие к ИР у пациентов с ХБП:
• анемия;
• воспаление;
• оксидативный стресс;
• дефицит витамина D;
• метаболический ацидоз;
• уремическая интоксикация и нездоровый образ жизни.
Наличие ИР у больных на гемодиализе значительно увеличивает частоту сердечнососудистых событий.
ИНСУЛИНОРЕЗИСТЕНТНОСТЬ И ХБП
M. Guthoff с соавт. изучили особенности метаболизма глюкозы у гемодиализных пациентов без СД (основная группа). Сравнение проводилось с больными, у которых были в норме и функция почек, и углеводный обмен (контрольная группа). У участников основной группы развилась выраженная ИР, была повышена секреция инсулина и фиксировались более низкие показатели гликемии натощак по сравнению с группой контроля. Некоторые авторы отмечают влияние провоспалительных маркеров в развитии ИР при ХБП. Так, в исследовании при участии 79 пациентов с тХПН без диабета выявлена положительная корреляция между уровнем провоспалительного маркера интерлейкина (ИЛ) 1β и ИР.
Часто встречающиеся метаболический синдром (МС) и ожирение у пациентов с ХБП оказываются дополнительными ФР развития гипергликемии. Причина — усугубление ИР и снижение скорости клубочковой фильтрации (СКФ). В то же время пациенты с ожирением и МС имеют на 47 % больший риск прогрессирования ХБП по сравнению с больными, у которых нет ни того ни другого. Примечательно, что риск усугубления ХБП существует и для пациентов с ожирением, но без МС. Однако и сама достаточно сложная процедура гемодиализа может вызывать как снижение, так и повышение уровня глюкозы в крови. Так, гипогликемия, связанная с диффузией молекул глюкозы в эритроциты, во время гемодиализа приводит к развитию гипергликемии из-за активации контррегуляторных гормонов. Также процедура гемодиализа — сильный стрессовый фактор, приводящий к гипергликемии из-за выброса катехоламинов в кровь. Недостаточность витамина D у больных с тХПН и ИР также вносит вклад в развитие гипергликемии.
НЕНАДЕЖНЫЙ СТАНДАРТ
В качестве золотого стандарта оценки углеводного статуса, признанного Всемирной организацией здравоохранения, выступает гликированный гемоглобин (HbA1c). В клинических рекомендациях (КР) Американской диабетической ассоциации (American Diabetes Association, ADA), а также в десятом выпуске отечественных «Алгоритмов специализированной медицинской помощи больным СД» (2021) отмечено, что при значении HbA1c ≥6,5 % в сочетании с явными симптомами острой метаболической декомпенсации больному ставится диагноз СД. Однако у гемодиализных пациентов с ХБП HbA1c может некорректно отображать реальную гликемическую картину из-за ложного снижения его значения, а следовательно, по этой же причине может уменьшаться и выявляемость СД.
Среди причин, влияющих на лабильность показателей HbA1c у пациентов с ХБП на гемодиализе, выделяют:
• анемию;
• снижение жизненного цикла эритроцита;
• накопление уремических токсинов.
M.Guthoff с соавт. обнаружили значительно пониженные уровни HbA1c у пациентов с ХБП на диализе без углеводных нарушений относительно больных с сохранной почечной функцией. Авторы пришли к выводу, что нормальные значения HbA1c не исключают наличия СД у диализных пациентов вследствие высокой лабильности данного показателя в подобной ситуации. Поэтому последние национальные КР «Лечение пациентов с ХБП 5-й стадии методами гемодиализа и гемодиафильтрации» (2017) предусматривают измерение уровня глюкозы таким больным не реже четырех раз в год. Несмотря на определенную недостоверность значений HbA1c в оценке гликемического статуса диализных пациентов, данный показатель может использоваться для оценки риска смертности у больных с ХБП. Так, S.Ok с соавт. в исследовании при участии 489 гемодиализных пациентов без СД показали, что значение HbA1c >5,04 % независимо ассоциировано как с общей, так и с сердечнососудистой смертностью. Причем худший прогноз выживаемости имели пациенты с самыми низкими (менее 4,7 %) и самыми высокими (свыше 5,0 %) показателями HbA1c.
При этом в зарубежных исследованиях имеются крайне неожиданные данные. В 2018 году P.P.Wu с соавт. установили, что процедура диализа как таковая может выступать в роли протективного механизма в развитии СД. Основанием послужило установление значительной негативной корреляции между статусом «пациент на гемодиализе» и случаями впервые выявленного СД. Также ряд исследований продемонстрировали, что гемодиализ и тХПН уменьшают риск развития СД, однако, что очень существенно, —при сохраняющемся высоком уровне смертности. Например, по результатам общенационального ретроспективного когортного исследования, проведенного на Тайване, СД был выявлен лишь у 97 из 2092 пациентов на гемодиализе (коэффициент заболеваемости— 8,69/1000 пациенто-лет). Эта цифра оказалась значительно более низкой, чем в группе сравнения (недиализные больные, коэффициент заболеваемости — 15,88/1000 пациенто-лет). Таким образом, диализная когорта имела примерно вдвое меньший риск развития СД (4,8 % против 9,8 % в группе контроля), но при этом почти настолько же более высокий уровень смертности (30,1 % против 14,03 %).
Напрашивается аналогия с так называемым выгоранием диабета (burnt-out diabetes)— обнаруженном в ряде последних исследований феномене спонтанного улучшения гликемического контроля примерно у трети пациентов с СД и предположительным диагнозом «диабетическая нефропатия», находящихся на диализе, по мере прогрессирования ХБП, потери остаточной функции почек и начала диализной терапии. Гликемический контроль улучшается спонтанно, приводя к нормализации или снижению уровня HbA1c (менее 6 %) иглюкозы порой даже ниже целевых значений. Это угрожает развитием гипогликемических состояний, ухудшает прогноз и требует уменьшения дозировки или прекращения использования инсулина и других сахароснижающих препаратов. Выгорание СД связано с вышеописанным механизмом повышения концентрации инсулина из-за снижения его деградации почками.
НЕПЛОХАЯ АЛЬТЕРНАТИВА
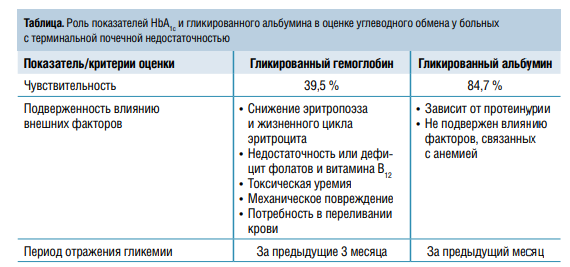
Альтернативой оценке углеводного статуса по HbA1c, по мнению F.G. Mаrtino и соавт., может служить гликированный альбумин (ГА). Авторы сравнили прогностические возможности ГА и HbA1c в выявлении гликометаболических отклонений у 160 гемодиализных пациентов. Большую прогностическую способность в обнаружении новых случаев СД показал ГА из-за более высокой чувствительности к нарушениям углеводного обмена. Исследователи считают, что в мониторинге углеводного статуса у гемодиализных пациентов целесообразно использовать оба биохимических маркера одновременно. Также ГА может выступать в качестве предиктора ухудшения почечной функции в популяции (при снижении СКФ значения ГА возрастают). Однако у пациентов с ХБП показатель ГА не лишен погрешности из-за влияния протеинурии.
Работ, в которых изучалась бы частота возникновения предиабета и впервые выявленного СД у гемодиализных пациентов с тХПН, пока мало. Большинство из них выполнено на Тайване, где есть база данных исследований, включающая сведения о диализных больных. Эти работы продемонстрировали, что гемодиализ и тХПН увеличивают риск развития СД и смертности у пациентов без данного диагноза, получающих ЗПТ. В крупном тайваньском исследовании участвовали 51487 пациентов, из них 47880 были на гемодиализе. Изучалось влияние предиабета и СД у диализных больных на риск смертности в течение 10 лет, а также исследовались заболеваемость и распространенность СД в трех группах пациентов:
1‑я — без СД (из них 20651 на диализе);
2‑я — с впервые выявленным СД (3044 на диализе);
3‑я — с ранее установленным СД (24 185 на диализе).
За 10 лет наблюдения заболеваемость СД составила 6 %, а распространенность—13 % после начала сеансов гемодиализа. Авторы отметили, что впервые выявленный СД повышает риск смертности на 10 %. Кроме того, с каждым годом наблюдения риск развития СД увеличивался у диализных пациентов с 4 % на первом году наблюдения до 21 % — на девятом. Результаты данной работы свидетельствуют о том, что вероятность развития СД у гемодиализных пациентов увеличивают следующие факторы:
• гипертензия;
• острый инфаркт миокарда;
• ишемическая болезнь сердца;
• хроническая обструктивная болезнь легких.
Другое тайваньское исследование продемонстрировало значительное повышение риска смерти в течение года после выявления нарушения гликемии натощак или толерантности к глюкозе у диализного пациента с тХБП, но без диабета. Еще в одной работе были изучены данные 59340 больных на гемодиализе. Распространенность среди них впервые выявленного СД составила 7,6 %, а частота возникновения новых случаев СД в течение трехлетнего наблюдательного периода составила 20 на тысячу пациенто-лет. Впервые выявленный СД после инициации сеансов гемодиализа на 20 % повышал риск смертности по сравнению с группой больных без СД. Способ диализа также имеет значение при развитии нарушений углеводного обмена. При сравнении пациентов без СД на гемоили перитонеальном диализе риск диабета был ниже у первых. По-видимому, это связано с использованием глюкозосодержащего диализата для проведения перитонеального диализа. Впервые выявленные нарушения углеводного обмена у гемодиализных пациентов с ХБП без предшествующего анамнеза СД повышают риск смерти. Раннее выявление подобных нарушений позволит отсрочить развитие микро- и макроваскулярных осложнений, тем самым увеличив продолжительность жизни пациентов и повысив ее качество. В связи со склонностью пациентов на гемодиализе к гипогликемии, а также некорректностью показателей HbA1c требуется поиск более чувствительных маркеров углеводных нарушений и их внедрение в рутинную практику.
Александр Рылов, к.м.н.
Читайте также
- Стратегия лечения дефицита витамина D
- Пациент с метаболически ассоциированной жировой болезнью печени на приеме у эндокринолога
- Первичный гиперпаратиреоз: новые рекомендации диагностики и лечения
- В будущее — без осложнений!
- Оптимальный контроль гликемии
- Эволюция подходов к ведению пациентов с эндогенным гиперкортицизмом
- Болезнь Иценко — Кушинга: что нового?
- Диагноз на стыке эндокринологии и кардиологии
- Самоконтроль: больше, чем кажется
- Международный консенсус экспертов по диагностике и лечению дефицита витамина B12

















